Ứng với công thức phân tử có bao nhiêu chất vừa phản ứng được với dung dịch NaOH, vừa phản ứng được với dung dịch HCl?
A. 3
B. 1
C. 2
D. 4
 Giải bởi Vietjack
Giải bởi Vietjack
Chất vừa phản ứng với NaOH và HCl; lại có số H > 2C + 3 (loại amino axit và este của amino axit)
=> chất này là muối của amoni hoặc amin
=> CTCT thỏa mãn là:
=> Có 2 CTCT thỏa mãn
Đáp án cần chọn là: C
Lý thuyết Amin
1. Khái niệm
- Khi thay thế một hay nhiều nguyên tử hiđro trong phân tử NH3 bằng một hay nhiều gốc hiđrocacbon ta được amin.
Ví dụ:
2. Phân loại
a. Theo gốc hiđrocacbon:
– Amin không thơm: CH3NH2, C2H5NH2, ...
– Amin thơm: C6H5NH2, CH3C6H4NH2, ...
– Amin dị vòng: 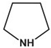
b. Theo bậc amin: là số nguyên tử H trong phân tử NH3 bị thay thế bởi gốc hiđrocacbon. Theo đó, các amin được phân loại thành:
| Amin bậc I | Amin bậc II | Amin bậc III |
|---|---|---|
| R–NH2 | R–NH–R’ | 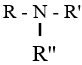 |
| R, R’ và R’’ là gốc hiđrocacbon | ||
Ví dụ:
1. Đồng phân
– Đồng phân về mạch cacbon.
– Đồng phân vị trí nhóm chức.
– Đồng phân về bậc của amin.
Ví dụ: Các đồng phân của C4H11N.
2. Danh pháp
a. Cách gọi tên theo danh pháp gốc – chức: Tên gốc hiđrocacbon + amin
Ví dụ: CH3NH2 (Metylamin), C2H5–NH2 (Etylamin), CH3CH(NH2)CH3 (Isopropylamin), …
b. Cách gọi tên theo danh pháp thay thế: Tên hiđrocacbon + vị trí + amin
Ví dụ: CH3NH2 (Metanamin), C2H5–NH2 (Etanamin), CH3CH(NH2)CH3 (Propan - 2 - amin), ...
c. Tên thông thường chỉ áp dụng với một số amin:
Tên gọi của một số amin
- Lưu ý:
– Tên các nhóm ankyl đọc theo thứ tự chữ cái a, b, c, … + amin.
– Với các amin bậc 2 và 3, chọn mạch dài nhất chứa N làm mạch chính:
+ Có 2 nhóm ankyl → thêm 1 chữ N ở đầu.
Ví dụ: CH3–NH–C2H5: N–etyl metyl amin.
+ Có 3 nhóm ankyl → thêm 2 chữ N ở đầu (nếu trong 3 nhóm thế có 2 nhóm giống nhau).
Ví dụ: CH3–N(CH3)–C2H5: N, N–etyl đimetyl amin.
+ Có 3 nhóm ankyl khác nhau → 2 chữ N cách nhau 1 tên ankyl.
Ví dụ: CH3–N(C2H5)–C3H7: N–etyl–N–metyl propyl amin.
– Khi nhóm –NH2 đóng vai trò nhóm thế thì gọi là nhóm amino.
Ví dụ: CH3CH(NH2)COOH (axit 2–aminopropanoic).
- Chất rắn, dạng tinh thể, không màu, vị hơi ngọt.
- Nhiệt độ nóng chảy cao, dễ tan trong nước vì amino axit tồn tại ở dạng ion lưỡng cực:
– Metyl–, đimetyl–, trimetyl– và etylamin là những chất khí có mùi khai khó chịu, độc, dễ tan trong nước, các amin đồng đẳng cao hơn là chất lỏng hoặc rắn.
- Anilin là chất lỏng, nhiệt độ sôi là 184oC, không màu, rất độc, ít tan trong nước, tan trong ancol và benzen.
1. Cấu tạo phân tử
- Trong phân tử amin đều có nguyên tử nitơ còn một cặp electron tự do chưa liên kết có thể tạo cho – nhận giống NH3.
⇒ Vì vậy các amin có tính bazơ giống NH3 (tức tính bazơ của amin = tính bazơ của NH3).
2. Tính chất hoá học
a. Tính bazơ
Do nguyên tử N trong phân tử amin còn cặp e chưa sử dụng có khả năng nhận proton.
* So sánh tính bazơ của các amin:
+ Nếu nguyên tử N trong phân tử amin được gắn với gốc đẩy e (gốc no: ankyl) thì tính bazơ của amin mạnh hơn so với tính bazơ của NH3. Những amin này làm cho quỳ tím chuyển thành màu xanh.
+ Nếu nguyên tử N trong phân tử amin gắn với các gốc hút e (gốc không no, gốc thơm) thì tính bazơ của amin yếu hơn so với tính bazơ của NH3. Những amin này không làm xanh quỳ tím.
+ Amin có càng nhiều gốc đẩy e thì tính bazơ càng mạnh, amin có càng nhiều gốc hút e thì tính bazơ càng yếu.
⇒ Lực bazơ: CnH2n + 1–NH2 > H–NH2 > C6H5–NH2
- Dung dịch metylamin và nhiều đồng đẳng của nó có khả năng làm xanh giấy quỳ tím hoặc làm hồng phenolphtalein.
– Amin bậc III mà gốc hiđrocacbon R, R’ và R’’ có số C ≥ 2 thì các gốc R, R’ và R’’ cản trở amin nhận proton H+ ⇒ tính bazơ yếu ⇒ dung dịch không làm đổi màu quỳ tím và phenolphtalein.
- Anilin và các amin thơm rất ít tan trong nước. Dung dịch của chúng không làm đổ màu quỳ tím và phenolphtalein.
- Tác dụng với axit: R–NH2 + HCl → R–NH3Cl
Ví dụ:
- Tác dụng dung dịch muối của các kim loại có hiđroxit kết tủa:
Ví dụ: 3CH3NH2 + FeCl3 + 3H2O → Fe(OH)3↓ + 3CH3NH3Cl
- Lưu ý: Khi cho muối của Cu2+, Zn2+, … vào dung dịch amin (dư) → hiđroxit kết tủa → kết tủa tan (tạo phức chất).
b. Phản ứng với axit nitrơ HNO2
- Amin bậc một tác dụng với axit nitrơ ở nhiệt độ thường cho ancol hoặc phenol và giải phóng nitơ.
C2H5NH2 + HONO → C2H5OH + N2↑ + H2O
- Anilin và các amin thơm bậc một tác dụng với axit nitrơ ở nhiệt độ thấp (0 - 5oC) cho muối điazoni:
c. Phản ứng ankyl hóa
Amin bậc một hoặc bậc hai tác dụng với ankyl halogenua (CH3I, …) , nguyên tử H của nhóm amin có thể bị thay thế bởi gốc ankyl:
Ví dụ: C2H5NH2 + CH3I → C2H5NHCH3 + HI
– Phản ứng này dùng để điều chế amin bậc cao từ amin bậc thấp hơn.
d. Phản ứng thế ở nhân thơm của anilin
Do ảnh hưởng của nhóm NH2 (tương tự nhóm –OH ở phenol), ba nguyên tử H ở các vị trí ortho và para so với nhóm –NH2 trong nhân thơm của anilin bị thay thế bởi ba nguyên tử brom:
Lưu ý: Phản ứng tạo ra kết tủa trắng 2, 4, 6 tribromanilin dùng nhận biết anilin.
e) Phản ứng cháy của amin no đơn chức mạch hở:
1. Ứng dụng
Các ankylamin được dùng trong tổng hợp hữu cơ, đặc biệt là các điamin được dùng để tổng hợp polime.
Anilin là nguyên liệu quan trọng trong công nghiệp phẩm nhuộm (phẩm azo, đen anilin,...), polime (nhựa anilin - fomanđehit,...), dược phẩm (streptoxit, suafaguaniđin,...)
2. Điều chế
- Thay thế nguyên tử H của phân tử amoniac
- Khử hợp chất nitro
Xem thêm một số kiến thức liên quan:
Lý thuyết Amin (mới + 15 câu trắc nghiệm) hay, chi tiết
63 câu Trắc nghiệm Hóa học 12 Chương 3 có đáp án: Amin, amino axit và protein
Hợp chất X có vòng benzen và nhóm chức este. Trong phân tử X, phần trăm khối lượng của oxi lớn hơn 29%. Lấy 1 mol X tác dụng hết với dung dịch NaOH dư, sản phẩm hữu cơ thu được chỉ là 2 mol chất Y. Cho các phát biểu sau:
(a) Chất X có 3 loại nhóm chức
(b) Chất X làm quì tím ẩm chuyển sang màu đỏ
(c) Số mol NaOH đã tham gia phản ứng là 4 mol
(d) Khi cho 1 mol X tác dụng hết với NaHCO3 (trong dung dịch) hoặc Na đều thu được 1 mol khí
(e) 1 mol chất Y tác dụng với vừa đủ 2 mol HCl
(g) Khối lượng chất Y thu được là 364g
Số phát biểu đúng là:
Hợp chất hữu cơ A mạch thẳng, CTPT là . A tác dụng với kiềm tạo khí mùi khai nhẹ hơn không khí. A tác dụng với axit tạo muối amin bậc I. Công thức cấu tạo của A là
Hỗn hợp hữu cơ X có công thức . Khi cho X tác dụng với dung dịch NaOH thu được một muối của một amino axit và một ancol đơn chức. Số công thức cấu tạo phù hợp với X là
Chất hữu cơ X là 1 muối axit có CTPT là có thể phản ứng với cả dung dịch axit và dung dịch kiềm. Khi cho X tác dụng với dung dịch NaOH dư, đun nóng, cô cạn thì phần rắn thu được chỉ toàn chất vô cơ. Số CTCT phù hợp là:
Cho hợp chất hữu cơ đơn chức X có công thức là Cho m gam X tác dụng với NaOH vừa đủ thu được 2,55 gam muối vô cơ. Giá trị của m là:
Đun nóng hợp chất hữu cơ X với NaOH thu được 2,24 lít khí Y có khả năng làm xanh giấy quỳ tím ẩm. Khối lượng muối khan thu được sau phản ứng là:
Hợp chất hữu cơ X) tác dụng với dung dịch NaOH dư, đun nóng, thu được sản phẩm hữu cơ gồm muối đinatri glutamat và ancol. Số công thức cấu tạo của X là
Hai hợp chất hữu cơ X và Y có cùng công thức phân tử là , đều là chất rắn ở điều kiện thường. Chất X phản ứng với dung dịch NaOH giải phóng khí, chất Y tham gia phản ứng trùng ngưng. Các chất X, Y lần lượt là
Chất X có công thức phân tử và là este của amino axit. Số công thức cấu tạo có thể có của X là
Đốt cháy hoàn toàn một chất hữu cơ X trong O2 thu được 1,344 lít , 0,168 lít (đktc) và 1,485 gam H2O. Khi cho X tác dụng với NaOH thu được một sản phẩm là . Công thức cấu tạo thu gọn của X là
Hai chất hữu cơ A, B có công thức . Hỗn hợp X gồm A và B cho tác dụng với NaOH dư tạo ra 2,72 gam một muối duy nhất và bay ra một hỗn hợp khí có . Hỗn hợp X có khối lượng
Hợp chất A là một muối có công thức phân tử . A tác dụng được với KOH tạo ra một amin và các chất vô cơ. Số công thức cấu tạo có thể có của A là
Hợp chất X có công thức có phản ứng tráng gương, khi phản ứng với dung dịch NaOH loãng tạo ra dung dịch Y và khí Z, khi cho Z tác dụng với dung dịch hỗn hợp gồm và HCl tạo ra khí P. Cho 11,55 gam X tác dụng với dung dịch NaOH vừa đủ, cô cạn dung dịch thu được số gam chất rắn khan là:








Bình “ga” loại 12 cân sử dụng trong hộ gia đình có chứa 12 kg khí hóa lỏng (LPG) gồm propan và butan với tỉ lệ mol tương ứng là 1 : 2. Khi được đốt cháy hoàn toàn, 1 mol propan tỏa ra lượng nhiệt là 2220 kJ và 1 mol butan tỏa ra lượng nhiệt là 2874 kJ. Trung bình mỗi ngày, một hộ gia đình cần đốt gas để cung cấp 9960 kJ nhiệt (có 20% nhiệt đốt cháy bị thất thoát ra ngoài môi trường). Sau bao nhiêu ngày hộ gia đình trên sẽ sử dụng hết bình gas 12 kg?


