Với giải Câu hỏi 5 trang 45 Hóa học lớp 10 Chân trời sáng tạo chi tiết trong Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố, thành phần và một số tính chất của hợp chất trong một chu kì và nhóm giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 10 Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố, thành phần và một số tính chất của hợp chất trong một chu kì và nhóm
Câu hỏi 5 trang 45 Hóa học 10: Giải thích sự hình thành ion Na+ và ion F-
Phương pháp giải:
- Na là kim loại, nguyên tử dễ nhường electron
- F là phi kim, nguyên tử dễ nhận electron
Lời giải:
- Na là kim loại nhóm IA => Có 1 electron ở lớp ngoài cùng => Khi tham gia liên kết dễ dàng nhường đi 1 electron để đạt cấu hình electron bền vững khí hiếm, tạo thành Na+
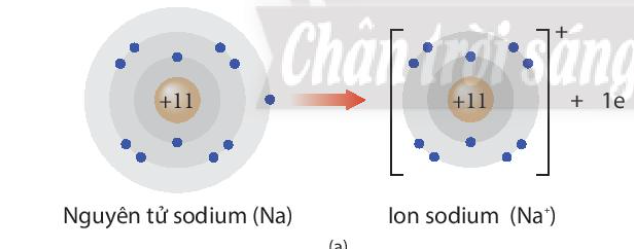
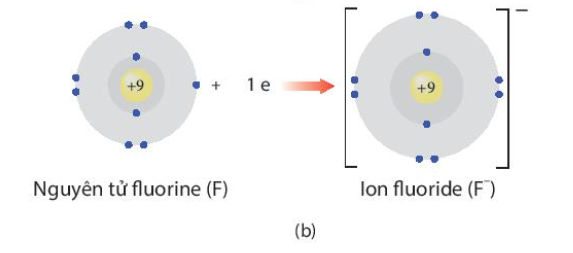
- F là phi kim nhóm VIIA => Có 7 electron ở lớp ngoài cùng => Khi tham gia liên kết dễ dàng nhận thêm 1 electron để đạt cấu hình electron bền vững của khí hiếm, tạo thành F-
Lý thuyết Tính kim loại, tính phi kim
- Tính kim loại là tính chất của một nguyên tố mà nguyên tử dễ nhường electron.
Ví dụ: Na → Na+ + 1e
- Tính phi kim là tính chất của một nguyên tố mà nguyên tử dễ nhận electron.
Ví dụ: F + 1e → F-
- Tính kim loại, tính phi kim của các nguyên tố nhóm A có xu hướng biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân:
+ Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, lực hút giữa hạt nhân với electron lớp ngoài cùng tăng. Do đó, tính kim loại của các nguyên tố giảm dần, tính phi kim tăng dần.
+ Trong một nhóm, theo chiều tăng dần của điện tích hạt nhân, lực hút giữa hạt nhân với các electron lớp ngoài cùng giảm. Do đó, tính kim loại của các nguyên tố tăng dần, tính phi kim giảm dần.
Xem thêm các bài giải Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Mở đầu trang 43 Hóa học 10: Kim loại kiềm là các kim loại nhóm IA, bao gồm: lithium (Li), sodium (Na), potassium (K), rubidium (Rb), caesium (Cs), francium (Fr). Chúng phản ứng được với nước và giải phóng khí hydrogen. Vậy khả năng phản ứng với nước của các kim loại trên có giống nhau hay không? Dựa vào bảng tuần hoàn các nguyên tố hóa học, chúng ta có thể giải thích được xu hướng biến đổi tính chất hóa học cơ bản của nguyên tử các nguyên tố không?...
Câu hỏi 1 trang 43 Hóa học 10: Quan sát Hình 6.1, cho biết bán kính nguyên tử của các nguyên tố trong mỗi chu kì và trong mỗi nhóm A biến đổi như thế nào...
Câu hỏi 2 trang 43 Hóa học 10: Xu hướng biến đổi bán kính nguyên tử của các nguyên tố trong mỗi chu kì và trong mỗi nhóm A do yếu tố nào gây ra? Giải thích...
Luyện tập trang 44 Hóa học 10: Dựa vào xu hướng biến đổi bán kính nguyên tử của các nguyên tố trong bảng tuần hoàn, em hãy sắp xếp các nguyên tố sau đây theo chiều tăng dần bán kính nguyên tử: Li, N, O, Na, K....
Câu hỏi 3 trang 44 Hóa học 10: Từ số liệu trong Bảng 6.1, nhận xét sự biến đổi giá trị độ âm điện của nguyên tử các nguyên tố trong một nhóm A và trong một chu kì. Giải thích...
Câu hỏi 4 trang 44 Hóa học 10: Hãy cho biết vì sao trong Bảng 6.1, giá trị độ âm điện của nguyên tử các nguyên tố nhóm VIIIA còn để trống...
Luyện tập trang 45 Hóa học 10:Dựa vào xu hướng biến đổi độ âm điện của nguyên tử các nguyên tố trong bảng tuần hoàn, em hãy sắp xếp các nguyên tố sau đây theo chiều tăng dần độ âm điện của nguyên tử: Na, K, Mg, Al...
Câu hỏi 6 trang 45 Hóa học 10: Khả năng nhường hoặc nhận electron hóa trị của các nguyên tử các nguyên tố nhóm A thay đổi như thế nào khi:...
Luyện tập trang 46 Hóa học 10: Dựa vào xu hướng biến đổi tính kim loại – phi kim của các nguyên tố trong bảng tuần hoàn, hãy sắp xếp các nguyên tố sau đây theo chiều giảm dần tính kim loại: sodium, magnesium và potassium...
Câu hỏi 7 trang 46 Hóa học 10: Từ các phản ứng của các oxide và hydroxide: Na2O, NaOH, Al2O3, Al(OH)3, SO3, H2SO4 với các dung dịch HCl, KOH, hãy nhận xét tính acid, base của các oxide và hydroxide trên...
Câu hỏi 8 trang 47 Hóa học 10: Quan sát Bảng 6.2, hãy liên hệ xu hướng biến đổi tính acid, tính base của oxide và hydroxide tương ứng với tính kim loại, phi kim của các nguyên tố trong chu kì...
Luyện tập trang 47 Hóa học 10: Dựa vào xu hướng biến đổi tính acid - base của oxide và hydroxide tương ứng của các nguyên tố trong bảng tuần hoàn, hãy sắp xếp các hợp chất sau đây theo chiều giảm dần tính acid của chúng: H2SiO3, HClO4, H2SO4, H3PO4...
Vận dụng trang 47 Hóa học 10: Aspartame là một chất làm ngọt nhân tạo, được sử dụng trong một số loại soda dành cho người ăn kiêng. Xác định vị trí của các nguyên tố tạo nên aspartame trong bảng tuần hoàn. Trong số các nguyên tố đó, nguyên tố nào có tính phi kim mạnh nhất?...
Bài 1 trang 47 Hóa học 10: Nguyên tử của nguyên tố nào sau đây có bán kính nhỏ nhất?...
Bài 2 trang 48 Hóa học 10: Bốn nguyên tố D, E, M, Q cùng thuộc một nhóm A trong bảng tuần hoàn, có số hiệu nguyên tử lần lượt là 9, 17, 35, 53. Các nguyên tố này được sắp xếp theo chiều tính phi kim tăng dần theo dãy nào sau đây?...
Bài 3 trang 48 Hóa học 10: Xét ba nguyên tố có cấu hình electron lần lượt:...
Bài 4 trang 48 Hóa học 10: Trong bảng tuần hoàn các nguyên tố hóa học, cho biết nguyên tố nào có tính phi kim mạnh nhất. Giải thích...
Bài 5 trang 48 Hóa học 10: Cho bảng số liệu sau:...
Xem thêm các bài giải SGK Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 5: Cấu tạo bảng tuần hoàn các nguyên tố hóa học
Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố, thành phần và một số tính chất của hợp chất trong một chu kì và nhóm
Bài 7: Định luật tuần hoàn - Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
Bài 8: Quy tắc octet
Bài 9: Liên kết ion

