Với giải Bài OT6.9 trang 74 SBT Hóa học lớp 10 Chân trời sáng tạo chi tiết trong Ôn tập chương 6 giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 10. Mời các bạn đón xem:
Giải sách bài tập Hóa học lớp 10 Ôn tập chương 6
OT6.9 trang 74 SBT Hóa học 10. Sự phân hủy H2O2 theo phương trình hóa học: , được nghiên cứu và cho kết quả tại một nhiệt độ cụ thể như sau:
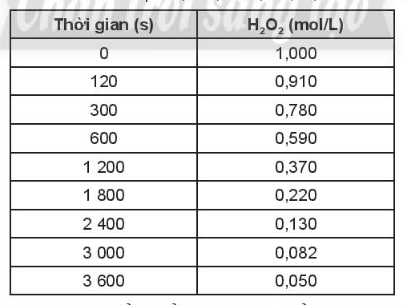
a. Tính tốc độ trung bình của phản ứng phân hủy H2O2 theo thời gian.
b. Tốc độ phản ứng thay đổi thế nào theo thời gian? Giải thích sự thay đổi đó.
Lời giải:
a) Tốc độ phản ứng phân huỷ theo thời gian
|
Thời gian (s) |
H2O2 (mol/L) |
Tốc độ phản ứng (mol/L.s) |
|
0 |
1,000 |
0 |
|
120 |
0,910 |
7,5 × 10-4 |
|
300 |
0,780 |
7,3 × 10-4 |
|
600 |
0,590 |
6,8 × 10-4 |
|
1200 |
0,370 |
5,3 × 10-4 |
|
1800 |
0,220 |
4,3 × 10-4 |
|
2400 |
0,130 |
3,6 × 10-4 |
|
3000 |
0,082 |
3,1 × 10-4 |
|
3600 |
0,050 |
2,6 × 10-4 |
b) Tốc độ phản ứng giảm dần theo thời gian. Tốc độ phản ứng phụ thuộc vào nồng độ chất tham gia, theo thời gian, nồng độ H2O2 giảm dần nên tốc độ phản ứng giảm.
Xem thêm các bài giải SBT Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
OT6.5 trang 74 SBT Hóa học 10. Cho phương trình hóa học của phản ứng:
OT6.7 trang 74 SBT Hóa học 10. Trong phản ứng: A → sản phẩm.
OT6.8 trang 74 SBT Hóa học 10. Xét phản ứng phân hủy N2O5 theo phương trình hóa học:
Xem thêm các bài giải SBT Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA