Tailieumoi.vn biên soạn và giới thiệu các kiến thức lý thuyết trọng tâm bao gồm định nghĩa, tính chất, ứng dụng và cách điều chế của ankan trong bài viết dưới đây, giúp học sinh ôn tập và bổ sung kiến thức cũng như hoàn thành tốt các bài kiểm tra môn Hóa học. Mời các bạn đón xem:
1. Định nghĩa Ankadien là gì?
Ankadien được định nghĩa là hidrocacbon mạch hở, không no. Trong phân tử hợp chất này có chứa 2 liên kết đôi và có công thức tổng quát là CnH2n-2 (với n≥ 3).
Công thức tổng quát của Ankadien liên hợp: CnH2n-2 (với n≥ 4).
Cách gọi tên Ankadien tổng quát như sau: số chỉ vị trí nhánh – tên nhánh + tên mạch chính + a – số chỉ vị trí nối đôi – dien
Dựa vào vị trí liên kết đôi, các em có thể chia Ankadien thành 3 loại:
3. Đồng phân
CnH2n - 2 có 2 loại đồng phân mạch hở.
- Đồng phân ankin (n ≥ 2)
- Đồng phân ankadien
+ Đồng phân cấu tạo: Bao gồm đồng phân vị trí liên kết đôi và đồng phân mạch C.
+ Đồng phân hình học: Bao gồm đồng phân cis và trans
4. Danh pháp của ankadien
a. Tên thông thường: Thay đuôi -an bằng đuôi -adien
Ví dụ:
CH2 = CH – CH = CH2 : butađien.
CH2 = C(CH3) – CH = CH2 : isopren.
b. Tên thay thế
Số chỉ vị trí nhánh – tên nhánh + Tên mạch chính + a + số chỉ vị trí nối đôi + dien.
Ví dụ: Từ C5H8 Viết các đồng phân cấu tạo ankadien có thể có và gọi tên
CH2 = C = CH – CH2 – CH3 : penta-1,2-dien
CH2 = CH – CH = CH – CH3: penta-1,3-dien
CH2 = CH – CH2 – CH = CH2: penta-1,4-dien
5. Tính chất vật lý của ankadien
Butađien là chất khí, isopren là chất lỏng (nhiệt độ sôi = 34oC). Cả 2 chất đều không tan trong nước, nhưng tan trong một số dung môi hữu cơ như: rượu, ete.
5. Tính chất hóa học của ankadien
Phản ứng cộng
Ankadien có 2 liên kêt đôi C=C nên ankađien có thể tham gia phản ứng cộng theo tỉ lệ mol 1:1 hoặc 1:2.
a. Cộng H2: (Điều kiện phản ứng là Ni, to) theo tỉ lệ 1:2 tạo ra hợp chất no là ankan.
CH2=CH-CH=CH2+ 2H2 → CH3-CH2-CH2-CH3
Tổng quát: CnH2n-2 + 2H2 → CnH2n+2
b. Cộng dung dịch Br2
Cộng theo tỉ lệ 1:1 (cộng vào vị trí 1,2 và 1,4) Sản phẩm cộng còn lại 1 liên kết đôi.
Ở nhiệt độ -80oC ưu tiên cộng vào vị trí 1,2
CH2=CH-CH=CH2 + Br2 → CH2Br - CHBr - CH=CH2
Ở nhiệt độ 40oC ưu tiên cộng vào vị trí 1,4
CH2=CH-CH=CH2 + Br2 → CH2Br - CH=CH - CH2Br
Cộng theo tỉ lệ 1:2 tạo ra sản phẩm no
CH2=CH-CH=CH2 + 2Br2 → CH2Br - CHBr - CHBr - CH2Br
Tổng quát: CnH2n-2+ 2Br2 → CnH2nBr4
c. Cộng hidro halogenua
Cộng theo tỉ lệ 1:1 (cộng vào vị trí 1,2 và 1,4) Sản phẩm cộng còn lại 1 liên kết đôi.
Ở nhiệt độ -80oC ưu tiên cộng vào vị trí 1,2
CH2=CH-CH=CH2 + HCl → CH3-CHCl-CH=CH2
Ở nhiệt độ 40oC ưu tiên cộng vào vị trí 1,4
CH2=CH-CH=CH2 + HCl → CH3-CH=CH-CH2Cl
Cộng theo tỉ lệ 1:2 tạo ra sản phẩm no
CH2=CH-CH=CH2 + 2HBr → CH3-CHBr-CHBr-CH3
Phản ứng trùng hợp
Các phản ứng trùng hợp chủ yếu xảy ra theo kiểu 1,4.
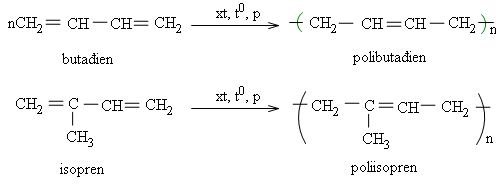
Phản ứng oxi hóa
a. Oxi hóa hoàn toàn
CnH2n-2 + (3n - 1)/2O2 → nCO2 + (n - 1)H2O
* Nhận xét: Sản phẩm đốt cháy ankađien:
nCO2 > nH2O và nCO2 - nH2O = nankađien.
b. Oxi hóa không hoàn toàn
Ankađien cũng làm mất màu dung dịch thuốc tím ở ngay nhiệt độ thường.
1. Tách H2 từ ankan tương ứng
CH3-CH2-CH2-CH3 → CH2=CH-CH=CH2 + 2H2
CH3-CH(CH3)-CH2-CH3→ CH2=C(CH3)-CH=CH2 + 2H2
2. Buta-1,3-đien
2C2H5OH → CH2=CH-CH=CH2 + 2H2O + H2 (MgO, ZnO, 4500C)
CHΞC-CH=CH2 + H2 → CH2=CH-CH=CH2 (Pd/PbCO3; t0)
Buta-1,3-đien hoặc isopren điều chế polibutađien hoặc poliisopren là những chất đàn hồi cao được dùng để sản xuất cao su (cao su buna, cao su isopren,…). Cao su buna được dùng làm lốp xe, nhựa trám thuyền,…