Với Giải hóa học lớp 10 trang 30 Cánh diều chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải hóa học 10 trang 30 Cánh diều
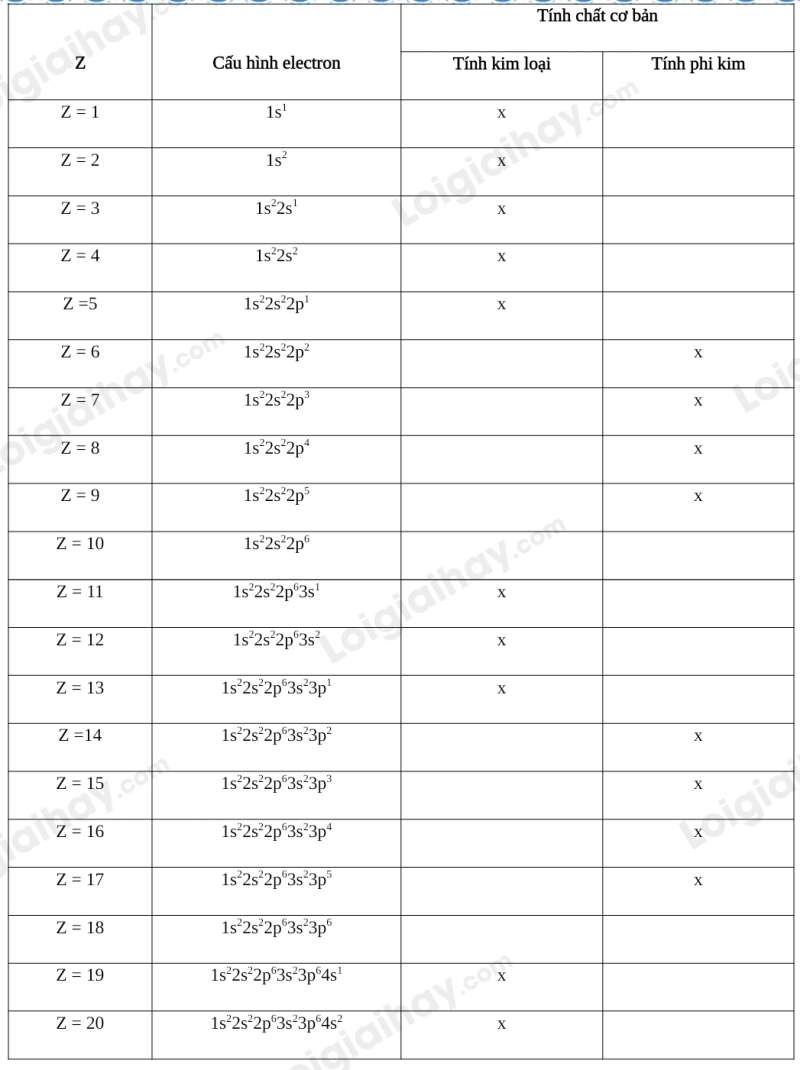
Luyện tập 4 trang 30 Hóa học 10: Dự đoán tính chất hóa học cơ bản (tính kim loại, tính phi kim) của các nguyên tố có Z từ 1 đến 20.
Phương pháp giải:
Từ cấu hình electron, có thể dự đoán các tính chất theo quy tắc sau:
Các nguyên tử có … electron ở lớp ngoài cùng
+ 1, 2, 3: nguyên tố kim loại (tính khử).
+ 5, 6, 7: nguyên tố phi kim (tính oxi hóa).
+ 8: nguyên tố khí hiếm (trừ He chỉ có 2 electron).
+ 4: nguyên tố kim loại hoặc phi kim.
Lời giải:
Bài 1 trang 30 Hóa học 10: Những phát biểu nào sau đây là đúng?
(a) Orbital 1s có dạng hình cầu, orbital 2s có dạng hình số tám nổi.
(b) Trong một nguyên tử, năng lượng của electron thuộc AO 1s thấp hơn năng lượng của electron thuộc AO 2s.
(c) Trong một nguyên tử, năng lượng của electron thuộc AO 2s thấp hơn năng lượng của electron thuộc AO 2p.
(d) Trong một nguyên tử, năng lượng của electron thuộc AO 2s gần năng lượng của electron thuộc AO 2p.
Phương pháp giải:
- AO s (AO hình cầu), AO p (AO hình số tám nổi).
- Các electron thuộc cùng một phân lớp có năng lượng bằng nhau, các electron thuộc cùng một lớp có năng lượng gần bằng nhau.
Lời giải:
(a) Sai vì AO s có dạng hình cầu.
(b) Đúng.
(c) Sai.
(d) Đúng.
Bài 2 trang 30 Hóa học 10: Nguyên tử nguyên tố X có hai lớp electron, trong đó có một electron độc thân. Vậy X có thể là những nguyên tố nào?
Lời giải:
X có hai lớp electron và có một electron độc thân
X có thể là Li (Z = 3):1s22s1 hoặc F (Z = 9): 1s22s22p5.
Bài 3 trang 30 Hóa học 10: Cấu hình electron của ion được thiết lập bằng cách thêm hoặc bớt electron, bắt đầu từ phân lớp ngoài cùng của cấu hình electron nguyên tử tương ứng.
a) Viết cấu hình electron của Na+ và Cl-.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp nào của Cl? AO đó là AO trống, chứa 1 hay 2 electron?
Lời giải:
a) Na (Z = 11) 1s22s22p63s1 ⇒ Na+: 1s22s22p6.
Cl (Z = 17) 1s22s22p63s23p5 ⇒ Cl-: 1s22s22p63s23p6.
b) Nguyên tử Cl nhận 1 electron để trở thành ion Cl-, electron này xếp vào AO thuộc phân lớp p của Cl. AO đó là AO chứa 1 electron.
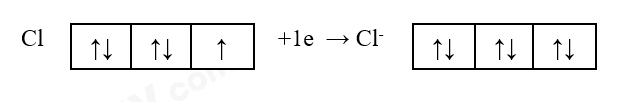
Xem thêm các bài giải Hóa học lớp 10 Cánh diều tạo hay, chi tiết khác: