Với Giải hóa học lớp 10 trang 115 Chân trời sáng tạo chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải hóa học 10 trang 115 Chân trời sáng tạo
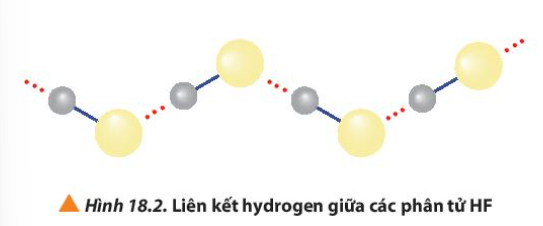
Câu hỏi 2 trang 115 Hóa học 10: Quan sát Hình 18.2, giải thích nhiệt độ sôi cao bất thường của hydrogen fluorine so với các hydrogen halide còn lại.
Phương pháp giải:
HF có liên kết hydrogen liên phân tử
Lời giải:
Các phân tử hydrogen fluoride hình thành liên kết hydrogen liên phân tử, loại liên kết này bền hơn tương tác van der Waals, nên nhiệt độ sôi của hydrogen fluoride cao bất thường so với các hydrogen halide còn lại
Luyện tập 1 trang 115 Hóa học 10: Thông tin trong Bảng 18.1 cho biết độ tan của hydrogen fluoride trong nước ở 0oC là vô hạn. Giải thích nguyên nhân dẫn đến tính chất này.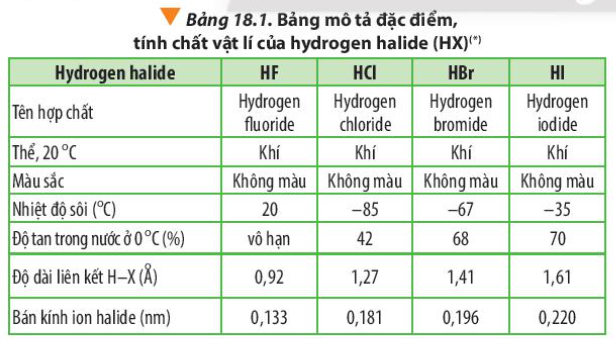
Phương pháp giải:
- HX (X là halogen) đều có liên kết hydrogen liên phân tử với H2O
- Ở 0oC: HCl, HBr, HI đều là chất khí, chỉ có HF là chất lỏng
Lời giải:
Fluorine là nguyên tố có độ âm điện lớn nhất ⇒ Liên kết H-F phân cực mạnh nhất ⇒ Tạo liên kết hydrogen bền với các phân tử H2O ⇒ hydrogen fluoride (HF) tan vô hạn trong nước.Phương pháp giải:
- Năng lượng liên kết giảm dần
- Độ dài liên kết tăng dần
- Tính acid là khả năng tách hydrogen
Lời giải:
- Đi từ HF đến HI: năng lượng liên kết giảm dần
=> Sự liên kết giữa H và X giảm dần
=> Độ dài liên kết tăng dần
=> Khả năng tách hydrogen tăng dần
=> Tính acid tăng dần
Luyện tập 2 trang 115 Hóa học 10: Hoàn thành phương trình hóa học của các phản ứng sau:(1) NaOH + HCl →
(2) Zn + HCl →
(3) CaO + HBr →
(4) K2CO3 + HI →
Lời giải:
(1) NaOH + HCl → NaCl + H2O
(2) Zn + 2HCl → ZnCl2 + H2↑
(3) CaO + 2HBr → CaBr2 + H2O
(4) K2CO3 + 2HI → 2KI + CO2 + H2O
Xem thêm các bài giải Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác: