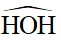Với giải Bài 4 trang 62 Chuyên đề Hóa học 10 Chân trời sáng tạo chi tiết trong Bài 9: Thực hành thí nghiệm hóa học ảo giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Chuyên đề Hóa 10. Mời các bạn đón xem:
Giải bài tập Chuyên đề Hóa học 10 Bài 9: Thực hành thí nghiệm hóa học ảo
Bài 4 trang 62 Chuyên đề Hóa học 10: Thực hành thí nghiệm “Hình dạng phân tử” bằng phần mềm PhET. Rút ra kết luận từ kết quả thu được.
Lời giải:
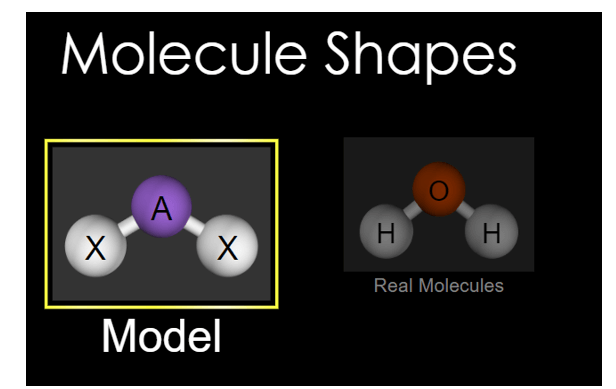
Bước 1: Bấm vào hình tam giác sẽ xuất hiện dạng mô hình (Model) và dạng phân tử thật (Real Molecules). Chọn dạng phân tử thật (Real Molecules)
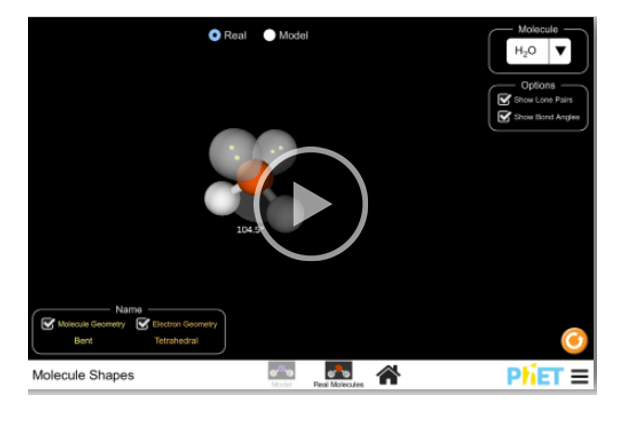
Bước 2: Sau đó hiện màn hình hiển thị mô hình phân tử.
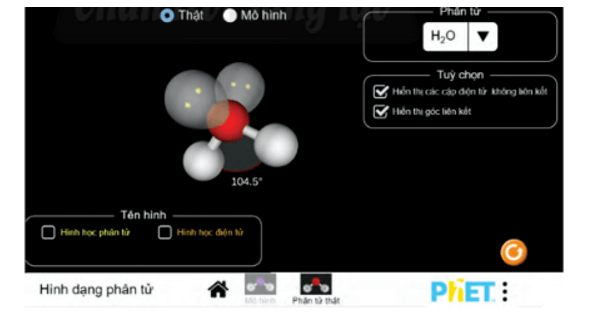
Chọn phân tử cần quan sát ở mục Molecule
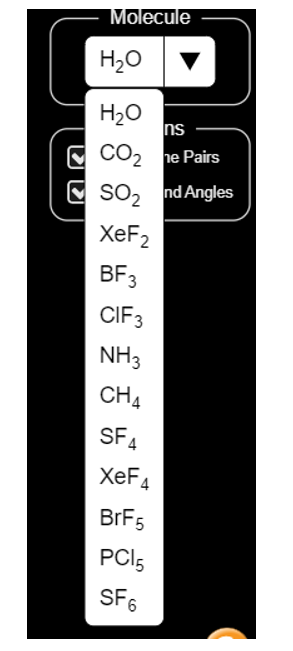
- Tích chuột vào Show Lone Pairs sẽ hiển thị các cặp electron riêng.
Tích chuột vào Show Bond Angles sẽ hiển thị góc liên kết.
Nhấn giữ chuột vào phân tử để xoay theo ý muốn.

Bước 3: Quan sát, rút ra nhận xét, kết luận.
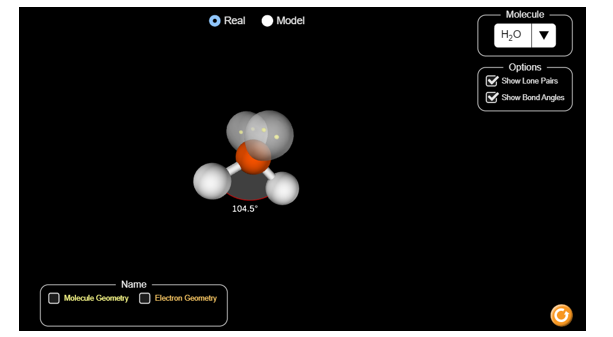
Xung quanh nguyên tử trung tâm O có hai cặp electron chưa liên kết và hai cặp electron chung với nguyên tử H. Chiếm 4 khu vực điện tích âm đẩy nhau để góc hóa trị lớn nhất là 109,5o.
Tuy nhiên, do cặp electron chưa liên kết chiếm khoảng không gian lớn hơn so với các cặp electron liên kết, tương tác đẩy giữa các cặp electron chưa liên kết lớn hơn tương tác đẩy giữa các cặp electron liên kết, nên góc liên kết 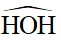 thực tế bằng 104,5o, nhỏ hơn góc hóa trị theo lí thuyết (109,5o).
thực tế bằng 104,5o, nhỏ hơn góc hóa trị theo lí thuyết (109,5o).
Phân tử có dạng góc.
Xem thêm lời giải bài tập Chuyên đề Hóa học 10 Chân trời sáng tạo hay, chi tiết khác:
Mở đầu trang 54 Chuyên đề Hóa học 10: Thí nghiệm hóa học có vai trò quan trọng đối với quá trình nhận thức và phát triển năng lực trong dạy và học môn Hóa học. Khi thiếu phương tiện, điều kiện thí nghiệm không đảm bảo hay thí nghiệm quá độc hại, tốn kém hoặc mất nhiều thời gian, chúng ta có thể thực hiện thí nghiệm hóa học ảo trên máy tính...
Câu hỏi 1 trang 55 Chuyên đề Hóa học 10: Từ giao diện của phần mềm (Hình 9.1), nêu những thành phần chính của các vùng trên giao diện phần mềm. Kho các bài thí nghiệm (open – online hay open – local) có vai trò gì cho người sử dụng?...
Câu hỏi 2 trang 55 Chuyên đề Hóa học 10: Tìm hiểu cách sử dụng các thanh công cụ trong phền mềm Yenka...
Câu hỏi 3 trang 56 Chuyên đề Hóa học 10: Từ các bước sử dụng thẻ Open – local, hãy thực hiện mô phỏng thí nghiệm “Định nghĩa tốc độ phản ứng” (Definition of reaction rate) trong mục “Tốc độ phản ứng” (Reaction Rates)...
Luyện tập trang 56 Chuyên đề Hóa học 10: Sử dụng thẻ Open – local để mô phỏng thí nghiệm “Acid and base”. Phân tích và lí giải kết quả của thí nghiệm...
Câu hỏi 4 trang 57 Chuyên đề Hóa học 10: Từ kết quả thí nghiệm “Surface area and rate” (Hình 9.5), hãy cho biết:...
Câu hỏi 5 trang 57 Chuyên đề Hóa học 10: Chọn hóa chất, dụng cụ và thực hiện thí nghiệm điều chế khi sulfur dioxide từ sulfur và oxygen...
Luyện tập trang 59 Chuyên đề Hóa học 10: Sử dụng thẻ New để mô phỏng thí nghiệm copper(II) oxide tác dụng với 10 mL dung dịch hydrochloric acid 1 M...
Luyện tập trang 61 Chuyên đề Hóa học 10: Thực hành thí nghiệm “Dung dịch acid-base” bằng phần mềm PhET...
Bài 1 trang 62 Chuyên đề Hóa học 10: Sử dụng cửa sổ Open – local của phần mềm Yenka nghiên cứu về mưa acid (theo hình hướng dẫn sau). Rút ra kết luận từ kết quả thí nghiệm...
Bài 2 trang 62 Chuyên đề Hóa học 10: Sử dụng thể Open – local của phần mềm Yenka, thực hiện thí nghiệm ảnh hưởng của nhiệt độ lên tốc độ phản ứng “Temperature and rate”. Phân tích và lí giải kết quả của thí nghiệm...
Bài 3 trang 62 Chuyên đề Hóa học 10: Hãy thiết kế thí nghiệm (thẻ New): Phản ứng của dung dịch iron(II) chloride 1M (FeCl2) với dung dịch potassium hydroxide 1 M (KOH)...