Tailieumoi.vn giới thiệu Giải sách bài tập Hóa học lớp 8 Bài 36: Nước chi tiết giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 8. Mời các bạn đón xem:
Giải SBT Hóa học 8 Bài 36: Nước
Bài 36.1 trang 48 SBT Hóa học 8: Cho các oxit: CaO ; Al2O3 ; N2O5, CuO ; Na2O ; BaO ; MgO ; P2O5 ; Fe3O4 ; K2O. Số oxit tác dụng với nước tạo ra bazơ tương ứng là
A. 3. B. 4.
C. 5. D. 2.
Lời giải:
Đó là các oxit CaO, Na2O, BaO; K2O.
=> Chọn B.
Bài 36.2 trang 49 SBT Hóa học 8: Cho các oxit: CO2 ; SO2 ; CO ; P2O5; N2O5 ; NO ; SO3; BaO, CaO. Số oxit tác dụng với nước tạo ra axit tương ứng là
A.6. B. 4. C.5 D. 8.
Lời giải:
Đó là các oxit : CO2 ; SO2 ; P2O5; N2O5 ; SO3 .
=> Chọn C.
Bài 36.3 trang 49 SBT Hóa học 8: Có ba chất gồm MgO, N2O5, K2O đựng riêng biệt trong ba lọ bị mất nhãn. Để nhận biết các chất trên, ta dùng thuốc thử là
A. nước.
B. nước và phenolphtalein.
C. dung dịch HCl.
D. dung dịch H2SO4.
Phương pháp giải:
Gợi ý: Dùng nước và phenolphtalein.
Lời giải:
MgO không tan trong nước, N2O5 tan trong nước tạo thành axit HNO3 không làm đổi màu phenolphtalein, BaO tan trong nước thành dung dịch Ba(OH)2 làm phenolphtalein chuyển thành màu hồng.
=> Chọn B.
Bài 36.4 trang 49 SBT Hóa học 8: Trong các oxit sau, oxit nào tác dụng được với nước ? Nếu có hãy viết phương trình hoá học của phản ứng và gọi tên sản phẩm tạo thành : SO3, Na2O, Al2O3, CaO, P2O5, CuO, CO2.
Phương pháp giải:
Chỉ có oxit bazơ của kim loại kiềm và kiềm thổ là tác dụng với nước. Những oxit bazơ tác dụng với nước và do đó cũng tan được trong nước là: Na2O, K2O, CaO, BaO, Li2O, Rb2O, Cs2O, SrO.
Công thức: R2On + nH2O ---> 2R(OH)n (n là hóa trị của kim loại R).
Một số oxit axit có tác dụng với nước, tạo thành dung dịch axit.
Lời giải:
- Các oxit tác dụng với nước là: SO3, Na2O, CaO, P2O5, CO2.
(axit sunfuric)
(natri hiđroxit)
(Canxi hiđroxit)
(axit photphoric)
(axit cacbonic)
- Các oxit không tác dụng với nước là: Al2O3, CuO.
Bài 36.5 trang 49 SBT Hóa học 8: Cho nổ một hỗn hợp gồm 1 mol hiđro và 14 lít khí oxi (đktc).
a) Có bao nhiêu gam nước được tạo thành ?
b) Chất khí nào còn dư và dư bao nhiêu lít ?
Phương pháp giải:
+) Tính số mol oxi theo công thức: n=V: 22,4 (mol)
+) Viết PTHH:
+) Tính theo PTHH để biết chất nào dư, sản phẩm được tính theo chất phản ứng hết
+) Trả lời yêu cầu của đề bài.
Lời giải:
a) Phương trình hóa học :
2 mol 1 mol 2 mol
Theo phương trình tỷ số mol của H2 và O2:
Vậy O2 dư, H2 hết
b) Chất dư là oxi
lít
Bài 36.6 trang 49 SBT Hóa học 8: Cho một hỗn hợp chứa 4,6 g natri và 3,9 g kali tác dụng với nước.
a) Viết phương trình hoá học.
b) Tính thể tích khí hiđro (đktc) thu được.
c) Dung dịch sau phản ứng làm đổi màu giấy quỳ tím như thế nào ?
Phương pháp giải:
+) Tính số mol natri và kali theo công thức: n = m : M (mol).
+) Viết PTHH:
+) Tính theo PTHH => số mol hiđro tạo thành => thể tích hiđro.
+) Gợi ý: Sau phản ứng chứa bazơ.
Lời giải:
a)
Phương trình hóa học :
2 mol 1 mol
0,2 mol x mol
2 mol 1 mol
0,1 mol y mol
sinh ra = (0,1+0,05) x 22,4 = 3,36(lít).
b) Dung dịch sau phản ứng là dung dịch bazơ nên làm đổi màu quỳ tím thành xanh.
Bài 36.7 trang 49 SBT Hóa học 8: Dưới đây cho một số nguyên tố hoá học :
Natri, đồng, photpho, magie, nhôm, cacbon, lưu huỳnh.
a) Viết công thức các oxit của những nguyên tố trên theo hoá trị cao nhất của chúng.
b) Viết phương trình hoá học của phản ứng giữa các oxit trên (nếu có) với nước.
c) Dung dịch nào sau phản ứng làm đổi màu giấy quỳ tím ?
Phương pháp giải:
a) Dựa vào qui tắc hóa trị để lập công thức oxit.
b) - Chỉ có oxit bazơ của kim loại kiềm và kiềm thổ là tác dụng với nước. Những oxit bazơ tác dụng với nước và do đó cũng tan được trong nước là: Na2O, K2O, CaO, BaO, Li2O, Rb2O, Cs2O, SrO.
- Đa số các oxit axit khi hoà tan vào nước sẽ tạo ra dung dịch axit trừ SiO2
c) - Dung dịch axit làm quì tím hóa đỏ.
- Dung dịch bazơ làm quì tím hóa xanh.
Lời giải:
a) Công thức các oxit theo hoá trị cao nhất của natri, đồng, photpho, magie. nhôm, cacbon, lưu huỳnh là : Na2O, CuO, P2O5, MgO, Al2O3, CO2, SO3.
b) Các oxit hoà tan vào nước : Na2O, P2O5, CO2, SO3 :
c) Các oxit không hoà tan vào nước : CuO, MgO, Al2O3.
Dung dịch sau phản ứng làm đổi màu giấy quỳ tím thành xanh : (1).
Dung dịch sau phản ứng làm đổi màu giấy quỳ tím thành đỏ : (2), (3), (4).
Bài 36.8 trang 49 SBT Hóa học 8: Cho 210 kg vôi sống (CaO) tác dụng với nước, em hãy tính lượng Ca(OH)2 thu được theo lí thuyết. Biết rằng vôi sống có 10% tạp chất không tác dụng với nước.
Phương pháp giải:
+) Tính khối lượng CaO nguyên chất.
+) PTHH:
+) Tính theo PTHH => Khối lượng thu được .
Lời giải:
Khối lượng vôi sống (CaO) nguyên chất :
Phương trình hóa học
56 kg 74 kg
189 kg x kg
Khối lượng thu được là: 249,75 kg.
Bài 36.9 trang 49 SBT Hóa học 8: Viết phương trình hoá học biểu diễn các biến hoá sau và cho biết mỗi phản ứng thuộc loại phản ứng nào.
a)
b)
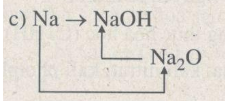
Phương pháp giải:
a) Học sinh tự viết PTHH
b) Phản ứng hóa hợp là phản ứng hóa học trong đó có một chất mới được tạo thành từ hai hay nhiều chất ban đầu.
Phản ứng phân hủy là phản ứng hóa học trong đó một chất sinh ra hai hay nhiều chất mới.
Phản ứng oxi hóa – khử là phản ứng hóa học trong đó xảy ra đồng thời sự oxi hóa và sự khử.
Phản ứng thế là phản ứng hóa học trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất.
Lời giải:
a) : Phản ứng hóa hợp
: Phản ứng hóa hợp
b) : Phản ứng hóa hợp
: Phản ứng hóa hợp
c) : Phản ứng thế
: Phản ứng hóa hợp
: Phản ứng hóa hợp
Bài 36.10* trang 50 SBT Hóa học 8: Cho sơ đồ chuyển hoá sau :
CaCO3 ------> CaO ------> Ca(OH)2 -----> CaCO3.
Viết các phương trình hoá học của phản ứng biểu diễn chuyển hoá trên.
Lời giải:
Bài 36.11 trang 50 SBT Hóa học 8: Đốt cháy 10 cm3 khí hiđro trong 10 cm3 khí oxi. Biết các thể tích khí đo cùng ở 100°C và áp suất khí quyển. Thể tích chất khí còn lại sau phản ứng là
A. 5 cm3 hiđro.
B. 10 cm3 hiđro.
C. chỉ có 10 cm3 hơi nước
D. 5 cm3 oxi.
Phương pháp giải:
+) Do cùng điều kiện nên tỉ lệ thể tích chính là tỉ lệ số mol
+) Viết PTTH:
+) Tính theo PTHH để biết chất nào dư, sản phẩm được tính theo chất phản ứng hết
+) Trả lời yêu cầu của đề bài.
Lời giải:
Phương án D.
Các thể tích khí đo ở cùng điều kiện nhiệt độ (100°C ) và áp suất (khí quyển) nên tỷ lệ thể tích bằng tỷ lệ số mol :
(khí) (Khí) (hơi)
Tỷ lệ thể tích của H2 và O2: H2 hết, O2 dư