Tailieumoi.vn xin giới thiệu phương trình 4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Magie. Mời các bạn đón xem:
Phương trình 4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
1. Phương trình phản ứng hóa học:
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
2. Cân bằng phản ứng Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
Mg0 + HN+5O3 → Mg+2(NO3)2 + N-3H4NO3 + H2O
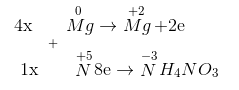
Tỉ lệ 2 muối nitrat của amoni và magiê là 1:4.
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
3. Hiện tượng nhận biết phản ứng
Kim loại tan dần tạo thành dung dịch màu không màu và không thấy có khí thoát ra.
4. Điều kiện phản ứng
Dung dịch HNO3 loãng
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của Mg (Magie)
- Trong phản ứng trên Mg là chất khử.
- Mg là chất khử mạnh tác dụng được với các axit.
5.2. Bản chất của HNO3 (Axit nitric)
- Trong phản ứng trên HNO3 là chất oxi hoá.
- Đây là một monoaxit mạnh, có tính oxi hóa mạnh có thể nitrat hóa nhiều hợp chất vô cơ.
6. Tính chất hóa học
6.1. Tính chất hóa học của Mg (Magie)
- Magie là chất khử mạnh:
Mg → Mg2+ + 2e
a. Tác dụng với phi kim
Lưu ý:
- Do Mg có ái lực lớn với oxi: 2Mg + CO2 → MgO. Vì vậy không dùng tuyết cacbonic để dập tắt đám cháy Mg.
b. Tác dụng với axit
- Với dung dịch HCl và H2SO4 loãng:
Mg + H2SO4 → MgSO4 + H2
- Với dung dịch HNO3:
4Mg + 10 HNO3 → 4 Mg(NO3)2 + NH4NO3 + 3 H2O
6.2. Tính chất hóa học của HNO3 (Axit nitric)
Axit nitric được xếp hạng trong danh sách những axit mạnh nhất. Đây là một axit khan – một monoaxit mạnh có thể nitrat hóa nhiều hợp chất vô cơ với hằng số cân bằng axit (pKa) = -2.
Axit nitric phân li hoàn toàn thành các ion H+ và NO3- trong dung dịch loãng. Dung dịch HNO3 làm quỳ tím chuyển đỏ.
HNO3 có tác dụng với oxit bazơ, bazơ và muối của axit yếu hơn tạo ra muối nitrat.
Ví dụ:
CuO + 2HNO3 → Cu(NO3)2 + H2O
CaCO3 + 2HNO3 → Ca(NO3)2 + H2O + CO2
Ba(OH)2 + 2HNO3 → Ba(NO3)2 + 2H2O
Axit nitric tác dụng với oxit bazơ, bazo, muối mà kim loại trong hợp chất này chưa lên hóa trị cao nhất:
Ví dụ:
FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O
FeCO3 + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O + CO2
Axit nitric cũng là 1 trong những axit có tính oxi hóa mạnh. Nó có thể bị khử đến các sản phẩm khác nhau của nitơ, phụ thuộc vào nồng độ axit mạnh hay yếu của chất khử. Cùng tìm hiểu tính oxi hóa của axit nitric thông qua 3 phản ứng:
Một là,Tác dụng với kim loại
Hai là, Tác dụng với phi kim
Ba là, Tác dụng với hợp chất
Tác dụng với kim loại
Axit nitric có khả năng oxi hóa hầu hết các kim loại tạo ra muối nitrat, ngay cả kim loại có tính khử yếu (Cu, Ag)…, ngoại trừ Pt và Au. Lúc này, kim loại bị oxi hóa đến mức cao nhất. Sản phẩm của phản ứng này sẽ là NO2(+4) đối với HNO3 đặc và NO(+2) đối với HNO3 loãng. Nhôm, sắt và crom thụ động với axit nitric đặc nguội vì lớp màng oxit bền được tạo ra bảo vệ chúng không bị oxy hóa tiếp. Đây cũng là lý do bình nhôm hoặc sắt được dùng để đựng HNO3 đặc.
Phương trình phản ứng:
Kim loại + HNO3 đặc → muối nitrat + NO + H2O (nhiệt độ)
Kim loại + HNO3 loãng → muối nitrat + NO + H2O
Kim loại + HNO3 loãng lạnh → muối nitrat + H2
Mg(rắn) + 2HNO3 loãng lạnh → Mg(NO3)2 + H2 (khí)
Ví dụ:
Cu + 4HNO3 đặc → Cu(NO3)2 + 2NO2(↑) + 2H2O
3Cu + 8HNO3 loãng → 3Cu(NO3)2 + 2NO (↑) + 4H2O
Tác dụng với phi kim
Khi được đun nóng, HNO3 đặc có khả năng oxi hóa được các phi kim như S, C, P… (các nguyên tố á kim, ngoại trừ halogen và silic). Sản phẩm tạo thành là nito dioxit (nếu là axit nitric đặc) và oxit nito (với axit loãng và nước).
Ví dụ:
S + 6HNO3 đặc → H2SO4 + 6NO2(↑) + 2H2O (nhiệt độ)
C + 4HNO3 đặc → 4NO2 + 2H2O + CO2
P + 5HNO3 đặc → 5NO2 + H2O + H3PO4
3C + 4HNO3 loãng → 3CO2 + 4NO + 2H2O
Tác dụng với hợp chất
Là một trong những axit cực mạnh, axit nitric (HNO3) đặc có khả năng oxi hóa – phá hủy nhiều hợp chất vô cơ, hữu cơ khác nhau.. Vải, giấy, mùn cưa,… đều bị phá hủy hoặc bốc cháy khi tiếp xúc với HNO3 đặc. Vì vậy, sẽ vô cùng nguy hiểm nếu để axit nitric (HNO3) tiếp xúc với cơ thể người.
Ví dụ:
3H2S + 2HNO3 (>5%) → 3S (↓) + 2NO + 4H2O
PbS + 8HNO3 đặc → PbSO4(↓) + 8NO2 + 4H2O
HNO3 hòa tan Ag3PO4, không tác dụng với HgS.
7. Cách thực hiện phản ứng
Cho kim loại Mg tác dụng với dung dịch axit nitric loãng dư
8. Bạn có biết
Mg tác dụng với axit HNO3 có thể tạo ra sản phẩm khử là khí NO2; NH4NO3; NO;… Trong đó chỉ có sản phẩm khử là muối amoni ở dạng dung dịch không phải dạng khí.
9. Bài tập liên quan
Ví dụ 1: Cho Mg tác dụng với axit HNO3 loãng thu được dung dịch màu vàng nâu và không thấy có khí thoát ra. Phương trình hóa học thể hiện đúng thí nghiệm trên là:
A. Mg + 4HNO3 → Mg(NO3)2 + 2NO2 + 2H2O
B. 3Mg + 8HNO3 → 3Mg(NO3)2 + 2NO + 4H2O
C. 5Mg + 12HNO3 → 5Mg(NO3)2 + N2 + 6H2O
D. 4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
Hướng dẫn giải:
Đáp án D
Sản phẩm khử của HNO3 là dung dịch muối amoni NH4NO3
Ví dụ 2: Cho 3,6 g Mg tác dụng với dụng axit HNO3 loãng thu được dung dịch muối không màu và không thấy có khí thoát ra. Khối lượng muối thu được là
A. 4,84 g
B. 2,22 g
C. 5,22 g
D. 3,02 g
Hướng dẫn giải:
Đáp án C
nMg = 0,15 mol ⇒ nMg(NO3)2 = 0,15 mol; nNH4NO3 = 0,15/4 = 0,0375 mol
m muối = mMg(NO3)2 + mNH4NO3 = 0,015.148 + 0,0375.80 = 5,44 g
Ví dụ 3: Cho sắt tác dụng axit HNO3 loãng dư thu được chất khí X là sản phẩm khử duy nhất có tỷ khối so với oxi là 1,4375. Sản phẩm khử của HNO3 là:
A.NH4NO3
B. NO
C. N2O
D. NO2
Hướng dẫn giải:
Đáp án D
MX= 1,4375.32 = 46 ⇒ X là NO2
Ví dụ 4: Cho phương trình: Mg + HNO3 → Mg(NO3)2+ NH4NO3 + H2O
Tổng hệ số cân bằng tối giản của phản ứng trên là
A. 23
B. 24
C. 18
D. 22
Hướng dẫn giải:
Đáp án D
Phương trình phản ứng hóa học
4Mg + 10HNO3 → 4Mg(NO3)2 + NH4NO3 + 3H2O
Tổng hệ số cân bằng tối giản của phản ứng trên là 22
Ví dụ 5: Cho Mg tan hoàn toàn trong dung dịch HNO3 loãng không thấy có khí thoát ra . Trong phương trình phản ứng tổng hệ số của các chất (nguyên, tối giản) là bao nhiêu?
A. 20
B. 24
C. 25
D. 22
Hướng dẫn giải:
Đáp án D
Ví dụ 6: Cho 4,8 gam Mg tác dụng với dung dịch HNO3 dư. Sau khi phản ứng xảy ra hoàn toàn thu được 1,792 lít NO (đktc) và dung dịch X. Khối lượng muối khan thu được khi cô cạn dung dịch X là
A. 13,92 gam
B. 15,60 gam
C. 16,80 gam
D. 31,20 gam
Hướng dẫn giải:
Đáp án D
Ta có:
nMg = 0,2 mol
nNO = 0,08 mol
Các quá trình trao đổi electron
Mg0 → Mg+2 + 2e
0,2 → 0,4
N+5 + 3e→ N+2
0,24 ← 0,08
Vậy còn 1 sản phẩm khử nữa là NH4NO3
N+5 + 8e → N-3
8x → x
Áp dụng bảo toàn electron ta có:
0,4 = 0,24 + 8x → a = 0,02 mol
=> mmuối = mNH4NO3 + mMg(NO3)2 = 31,2 gam
Ví dụ 7: Hòa tan hỗn hợp gồm 2,7 gam Al và 13 gam Zn bằng 500 ml dung dịch HNO3 vừa đủ, thu được dung dịch X và không thấy khí thoát ra. Cô cạn dung dịch X thu a gam muối. Giá trị của a:
A. 66,1 gam
B. 68,2 gam
C. 43,4 gam
D. 33,1 gam
Hướng dẫn giải:
Đáp án A
nAl = 2,7/27 = 0,1 mol
nZn = 13/65 = 0,2 mol
Không thấy khí thoát ra => Sản phẩm khử là NH4NO3
⇒ nNH4NO3 = (0,1.3 + 0,2.2)/8 = 0,7/8 mol
Dung dịch muối X gồm: Al(NO3)3 (0,1 mol); Zn(NO3)2 (0,2 mol), NH4NO3 (0,7/8 mol)
m = mAl(NO3)3 + mZn(NO3)2 + mNH4NO3 = 0,1.213 + 0,2.189 + (0,7/8).80 = 66,1 gam
Ví dụ 8: Cho các nhận xét dưới đây
(a) Tính chất hoá học đặc trưng của kim loại là tính khử.
(b) Đồng (Cu) không khử được muối sắt(III) (Fe3+).
(c) Ăn mòn kim loại là một quá trình hoá học trong đó kim loại bị ăn mòn bởi các axit trong môi trường không khí.
(d) Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào mặt ngoài vỏ tàu (phần chìm trong nước biển) những khối kẽm.
Số nhận định đúng là
A. 2.
B. 3.
C. 4.
D. 1.
Hướng dẫn giải:
Đáp án A
(a) Tính chất hoá học đặc trưng của kim loại là tính khử.
( d ) Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào mặt ngoài vỏ tàu (phần chìm trong nước biển) những khối kẽm .
Ví dụ 9: Cho dãy các dung dịch: MgCl2 , AlCl3 , Na 2CO 3, NaHCO3, NH4Cl, BaCl2 . Số chất trong dãy tác dụng được với dung dịch NaOH là:
A. 3
B. 5
C. 2
D. 4
Hướng dẫn giải:
Đáp án B
Điều kiện xảy ra phản ứng trao đổi ion trong dung dịch: sản phẩm có chất kết tủa hoặc chất bay hơi hoặc chất điện li yếu.
Giải chi tiết:
Có 5 dung dịch có phản ứng với NaOH:
MgCl2: MgCl2 + 2NaOH → Mg(OH)2 ↓ + 2NaCl
AlCl3: AlCl3 + 3NaOH → Αl(OH)3 ↓ + 3NaCl
Αl(OH)3 + NaOH → NaAlO2 + 2H2O
NaHCO3: NaHCO3 + NaOH → Na2CO3 + H2O
NH4Cl: NH4Cl + NaOH → NaCl + NH3 ↑ + H2O
Ví dụ 10: Cho dãy các chất sau: Al, NaHCO3, (NH4)2CO3 , NH4Cl, Al2O3 , Zn, K2CO3 , K2SO4. Có bao nhiêu chất trong dãy vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch NaOH?
A. 2
B. 3
C. 4
D. 5
Hướng dẫn giải:
Đáp án D
Chất vừa tác dụng được với axit vừa tác dụng với bazơ gồm : các kim loại Al, Zn, Sn, Be, Pb,.. và các chất lưỡng tính và các muối có khả năng tạo kết tủa...
Chất lưỡng tính:
+ Là oxit và hidroxit của các kim loại Al, Zn, Sn, Pb; Cr(OH)3 và Cr2O3.
+ Là các ion âm còn chứa H có khả năng phân li ra ion H+ của các chất điện li trung bình và yếu ( HCO3-, HPO42-, HS-…)
( chú ý : HSO4- có tính axit do đây là chất điện li mạnh)
+ Là muối chứa các ion lưỡng tính; muối tạo bởi hai ion, một ion có tính axit và một ion có tính bazơ ( (NH4)2CO3…)
Vậy ta có 5 chất thỏa mãn là : Al, NaHCO3, (NH4)2CO3 , Al2O3, Zn.
10. Một số phương trình phản ứng hoá học khác của Magie và hợp chất:
5Mg + 12HNO3 → 5Mg(NO3)2 + N2 + 6H2O
4Mg + 10HNO3 → 4Mg(NO3)2 + N2O + 5H2O
3Mg + 8HNO3 → 3Mg(NO3)2 + 2NO + 4H2O
Mg + 2H2SO4 → MgSO4 + SO2 + 2H2O
3Mg + 4H2SO4 → 3MgSO4 + S + 4H2O
4Mg + 5H2SO4 → 4MgSO4 + H2S + 4H2O
Mg + 2CH3COOH → (CH3COO)2Mg + H2