Tailieumoi.vn xin giới thiệu phương trình 2KHCO3 -to→ K2CO3 +CO2 + H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Kali. Mời các bạn đón xem:
Phương trình 2KHCO3 -to→ K2CO3 +CO2 + H2O
1. Phương trình phản ứng hóa học:
2KHCO3 -to→ K2CO3 +CO2 + H2O
2. Hiện tượng nhận biết phản ứng
- Có khí và hơi nước thoát ra.
3. Điều kiện phản ứng
- Nung nóng.
4. Tính chất hóa học
- Muối cacbonat tan tác dụng được với dung dịch bazơ tạo thành bazơ mới và muối mới
KHCO3 + Ba(OH)2 → KOH + BaCO3
- KHCO3 bền ở nhiệt độ thường, đun nóng bị phân hủy tạo muối trung hòa K2CO3:
2KHCO3 -to→ K2CO3 + H20+CO2
- Ngay trong dung dịch và ở nhiệt độ thường nó cũng bị phân hủy chậm tạo khí CO2; nếu đun nóng thì phân hủy sẽ mãnh liệt hơn.
- Tan trong nước thủy phân cho môi trường kiềm yếu → nhận biết được bằng quỳ tím chuyển xanh và metyl da cam chuyển vàng nhưng không nhận biêt được bằng phenolphthalein:
KHCO3 + H2O ⇄ K2CO3 + KOH
- Tác dụng với dung dịch kiềm (NaOH, KOH…) → phản ứng trung hòa.
KHCO3 + KOH → K2CO3 + H2O
2KHCO3 + Ca(OH )2 → K2CO3 + CaCO3 + H2O
KHCO3 + Ca(OH)2 → KOH + CaCO3 + H2O
- Phản ứng của 2 muối axit với nhau: (muối axit mạnh sẽ đóng vai trò là axit; muối axit yếu sẽ đóng vài trò là bazơ)
KHSO4 + KHCO3 → K2SO4 + CO2 + H2O
- Tác dụng với axit: (muối của axit yếu phản ứng với axit mạnh tạo ra muối mới + axit yếu hơn)
HCl + KHCO3 → KCl + CO2 + H2O
H2SO4 + 2KHCO3 → K2SO4 + 2CO2 + 2H2O
- Tác dụng với muối:
KHCO3 + AlCl3 + H2O → KCl + CO2 + Al(OH)3
KHCO3 + FeCl3 + H2O → Fe(OH)3 + KCl + CO2
KHCO3 + BaCl2 -to→ BaCO3 + KCl + H2O
- Tác dụng với oxit axit:
KHCO3 + SO2 → KHSO3 + CO2
5. Cách thực hiện phản ứng
- Nhiệt phân KHCO3.
6. Bạn có biết
- Các muối hidrocacbonat đều bị nhiệt phân.
7. Bài tập liên quan
Ví dụ 1: Nhiệt phân hỗn hợp KHCO3 và NaHCO3 sau phản ứng thu được hỗn hợp chất rắn là?
A. K2CO3 và Na2CO3.
B. NaHCO3 và K2CO3.
C. K2O và Na2O.
D. K2CO3 và Na2O.
Hướng dẫn giải
2KHCO3 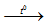
2NaHCO3 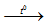
Đáp án A.
Ví dụ 2: Thể tích khí ở dktc thoát ra khi nhiệt phân hoàn toàn 10g KHCO3 là
A. 1,12 lít.
B. 2,24 lít.
C. 3,36 lít.
D. 4,48 lít.
Hướng dẫn giải
V = 0,05.22,4 = 1,12 lít.
Đáp án A.
Ví dụ 3: Nhiệt phân hoàn toàn 10 gam KHCO3 đến khi phản ứng xảy ra hoàn toàn, sau phản ứng thu được chất rắn có khối lượng giảm so với ban đầu là
A. 1,58 gam.
B. 3,10 gam.
C. 2,78 gam.
D. 1,00 gam.
Hướng dẫn giải
Khối lượng giảm = 0,05.(44+18) = 3,1 gam.
Đáp án B.
8. Một số phương trình phản ứng hóa học khác của Kali và hợp chất:
KHCO3 + HNO3 → KNO3 + CO2 + H2O
2KHCO3 + H2SO4 → K2SO4 + 2CO2 + 2H2O
KHCO3 + KHSO4 → K2SO4 + CO2 + H2O
2KHCO3 + 2NaHSO4 → K2SO4 + Na2SO4+ 2CO2 + 2H2O
2KHCO3 + Ba(HSO4)2 → K2SO4 + BaSO4 + 2CO2 + 2H2O