Với tóm tắt lý thuyết Vật Lí lớp 12 Bài 12: Áp suất khí theo mô hình động học phân tử. Quan hệ giữa động năng phân tử và nhiệt độ sách Kết nối tri thức hay, chi tiết cùng với 10 bài tập trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Vật Lí 12.
Lý thuyết Vật Lí 12 Bài 12: Áp suất khí theo mô hình động học phân tử. Quan hệ giữa động năng phân tử và nhiệt độ
A. Lý thuyết Áp suất khí theo mô hình động học phân tử. Quan hệ giữa động năng phân tử và nhiệt độ
I. Áp suất khí theo mô hình động học phân tử
1. Tác dụng của một phân tử khí lên thành bình
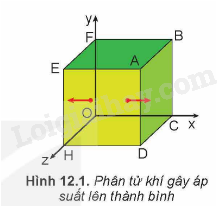
Xét một phân tử khí chuyển động trong một bình hình lập phương, mỗi cạnh có chiều dài L rất nhỏ. Phân tử này có khối lượng m và đang di chuyển với tốc độ v theo phương song song với một cạnh của bình tới va chạm đàn hồi và trực diện với thành bình ABCD. Sau khi va chạm, phân tử chuyển động theo chiều ngược lại với tốc độ có cùng độ lớn v tới thành bình đối diện.
Độ biến thiên độ lượng của phân tử do va chạm với thành bình ABCD có độ lớn là:
Thời gian giữa một lần va chạm của phân tử với thành bình ABCD và lần va chạm tiếp theo của nó với cùng thành bình đó là . Do giữa hai va chạm liên tiếp, phân tử khí lí tưởng chuyển động thẳng đều nên là thời gian ghi nhận được động lượng của phân tử khí biến thiên một lượng là 2mv.
Vậy độ lớn trung bình của lực gây ra thay đổi động lượng của phân tử khí đang xét là:
Lực do phân tử khí tác dụng lên thành bình ABCD có cùng độ lớn với F.
Thành bình ABCD là hình vuông nên diện tích của nó là:
Vậy áp suất do một phân tử khí gây ra là:
Trong bình không phải chỉ có một mà có một số lượng lớn các phân tử khí, mỗi phân tử khí có một giá trị khác nhau và mỗi phân tử đều góp phần gây ra áp suất lên thành bình. Vì thế, khi tính giá trị trung bình của , ta phải lấy giá trị trung bình của (kí hiệu là ).
2. Tác dụng của N phân tử khí lên thành bình
Nếu trong bình có N phân tử thì áp suất do chúng gây ra được tính bằng tích của N và giá trị trung bình của , tức là:
Thực tế, các phân tử trong bình chuyển động hỗn loạn không có phương nào ưu tiên, tức là chúng chuyển động và va chạm với ba cặp mặt đối diện của hình lập phương như nhau. Do đó, ta phải chia kết quả đã tính cho 3 để được áp suất do tất cả các phân tử gây ra lên mỗi mặt của bình lập phương. Với thể tích của bình là , ta thu được:
Vì N.m là khối lượng của tất cả các phân tử khí, tức là khối lượng của lượng khí trong bình nên ta có:
Với là khối lượng riêng của chất khí.
II. Mối quan hệ giữa động năng phân tử và nhiệt độ
Từ phương trình áp suất của khí lí tưởng và phương trình trạng thái của khí lí tưởng: pV = nRT
Ta rút ra được:
Với là số Avogadro, tức là số phân tử trong một mol khí.
Động năng trung bình của phân tử khí là , ta có:
Do R và đều là hằng số nên cũng là hằng số và được gọi là hằng số Boltzmann, .
Động năng tịnh tiến trung bình của phân tử khí lí tưởng:
* Khi thành lập công thức tính động năng của phân tử khí lí tưởng, ta chưa xét chuyển động quay của phân tử khí.
Sơ đồ tư duy Áp suất khí theo mô hình động học phân tử. Quan hệ giữa động năng phân tử và nhiệt độ
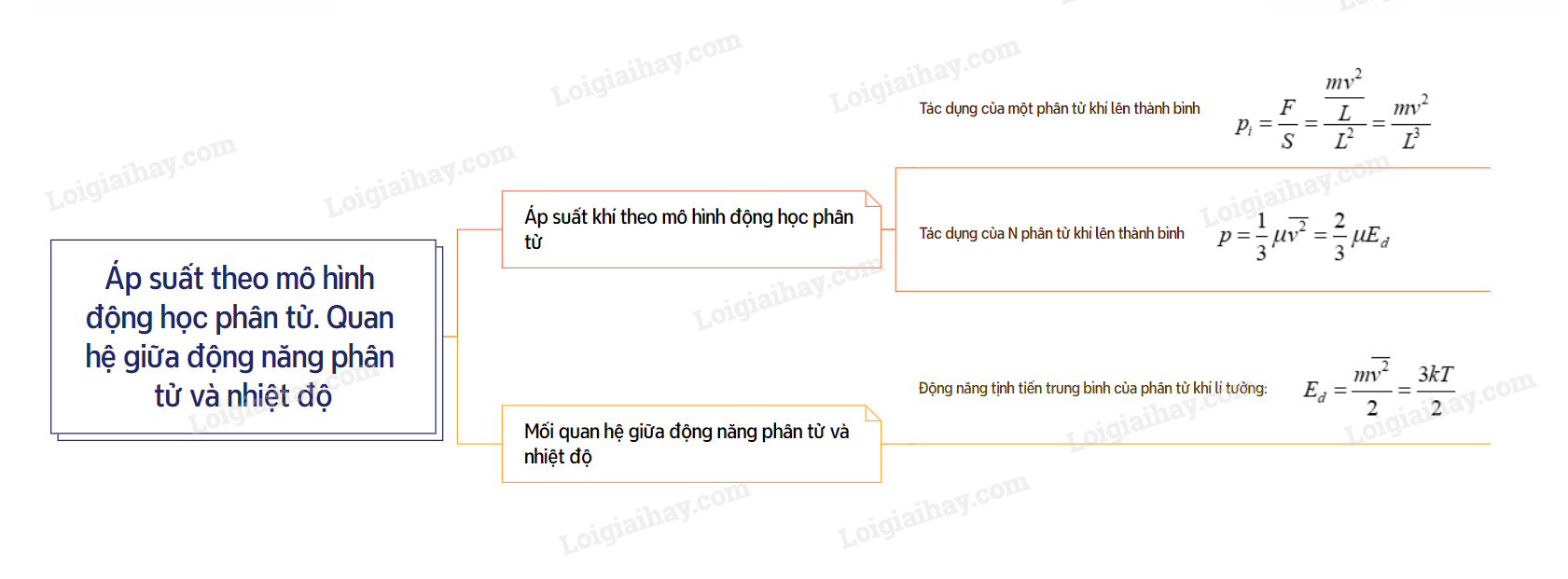
B. Trắc nghiệm Áp suất khí theo mô hình động học phân tử. Quan hệ giữa động năng phân tử và nhiệt độ
Đang cập nhật …
Xem thêm các bài tóm tắt lý thuyết Vật Lí lớp 12 Kết nối tri thức hay, chi tiết khác:
Lý thuyết Bài 15: Lực từ tác dụng lên dây dẫn mang dòng điện. Cảm ứng từ