Lời giải bài tập Hóa học lớp 12 Bài 1: Ester – Lipid sách Kết nối tri thức hay, chi tiết sẽ giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập môn Hóa học 12. Mời các bạn đón xem:
Giải bài tập Hóa học 12 Bài 1: Ester – Lipid
Lời giải:
1) Ester
- Khi thay thế nhóm OH ở nhóm carboxyl (-COOH) của carboxylic acid bằng nhóm –OR' thì được ester. Trong đó R' là gốc hydrocarbon.
-Tính chất vật lí:
+ Các phần tử ester có nhiệt độ sôi thấp hơn so với alcohol và carboxylic acid có phân tử khối tương đương.
+ Các ester có phân tử khối thấp và trung bình thường là chất lỏng ở nhiệt độ phòng. Những ester có phân tử khối lớn thường ở dạng rắn. Ester thường nhẹ hơn nước và ít tan trong nước. Một số ester có mùi thơm của hoa, quả chín.
- Tính chất hóa học: Ester bị thủy phân trong môi trường acid hoặc môi trường base.
2) Chất béo
- Chất béo là triester của glycerol với acid béo.
- Tính chất vật lí:
+ Ở nhiệt độ thường, chất béo ở trạng thái lỏng hoặc rắn.
+ Chất béo nhẹ hơn nước và không tan trong nước, dễ tan trong các dung môi hữu cơ.
- Tính chất hóa học:
+ Phản ứng thủy phân chất béo.
+ Phản ứng hydrogen hoá chất béo có gốc hydrocarbon không no (dạng lỏng) tạo thành chất béo có gốc hydrocarbon no (dạng rắn).
+ Chất béo bị oxi hoá bởi oxygen trong không khí tạo thành các hợp chất có mùi khó chịu.
Hoạt động trang 6 Hóa học 12: Tìm hiểu về đặc điểm chung của ester
Nhiều ester có trong tự nhiên là nguyên liệu để sản xuất hương liệu, mĩ phẩm. Hãy nhận xét đặc điểm chung về cấu tạo của các ester dưới đây:
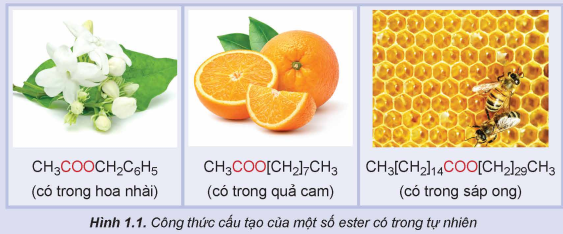
Lời giải:
Các ester trên đều có công thức chung là RCOOR’ (với R và R’ là gốc hydrocarbon).
Lời giải:
Tên của ester đơn chức RCOOR’ = Tên gốc R’ + Tên gốc carboxylic acid.
Các đồng phân ester có công thức phân tử C4H8O2:
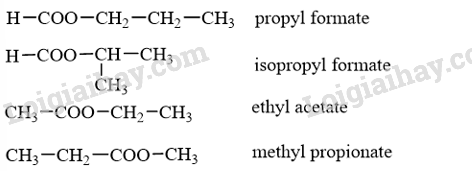
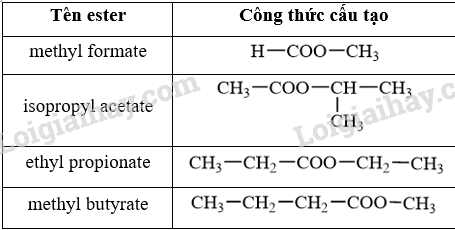
Câu hỏi 2 trang 7 Hóa học 12: Viết công thức cấu tạo của các ester có tên gọi sau đây:
a) methyl formate;
b) isopropyl acetate;
c) ethyl propionate;
d) methyl butyrate.
Lời giải:
|
|
CH3CH2CH2OH |
CH3COOH |
HCOOCH3 |
|
Loại hợp chất |
Alcohol |
Carboxylic acid |
Ester |
|
Phân tử khối |
60 |
60 |
60 |
|
Nhiệt độ sôi (oC) |
97 |
118 |
32 |
Lời giải:
Các phân tử ester không tạo được liên kết hydrogen với nhau, còn các phân tử alcohol và các phân tử carboxylic acid tạo được liên kết hydrogen liên phân tử nên nhiệt độ sôi của ester thấp hơn nhiều so với alcohol và carboxylic acid có phân tử khối tương đương.
Lời giải:
- Do không có liên kết hydrogen giữa các phân tử, ester có nhiệt độ sôi thấp hơn nhiệt độ sôi của carboxylic acid và alcohol có cùng số nguyên tử carbon hoặc có khối lượng phân tử tương đương. Do cấu tạo của nhóm carboxyl nên carboxylic acid có khả năng tạo thành liên kết hydrogen bền vững hơn liên kết hydrogen giữa các phân tử alcohol nên nhiệt độ sôi của carboxylic acid cao hơn nhiệt độ sôi của alcohol.
- Các chất trên có khối lượng phân tử tương đương, nhiệt độ sôi được sắp xếp theo thứ tự tăng dần như sau:
Methyl acetate (57oC); butan-1-ol (118oC); propanoic acid (141 °C).
Hoạt động trang 8 Hóa học 12: Nghiên cứu phản ứng thuỷ phân ester
Phản ứng thuỷ phân ester đã được tiến hành như sau:
- Cho vào hai ống nghiệm (1) và (2) mỗi ống khoảng 1,0 mL ethyl acetate.
- Thêm khoảng 2 mL dung dịch H2SO4 20% vào ống nghiệm (1) và khoảng 2 mL dung dịch NaOH 30% vào ống nghiệm (2). Quan sát thấy chất lỏng trong cả hai ống nghiệm tách thành hai lớp.
- Đun cách thuỷ ống nghiệm (1) và (2) trong cốc thuỷ tinh ở nhiệt độ 60 – 70 °C. Sau một thời gian, quan sát thấy:
Ống nghiệm (1): thể tích lớp chất lỏng phía trên giảm.
Ống nghiệm (2): tạo thành hỗn hợp đồng nhất.
Thực hiện các yêu cầu sau:
1. Tại sao ban đầu chất lỏng trong cả hai ống nghiệm lại tách thành hai lớp? Ester thuộc lớp nào?
2. Phản ứng thuỷ phân ester trong môi trường acid hay môi trường kiềm xảy ra tốt hơn?
Lời giải:
1. Vì ester ít tan trong nước và dung dịch của H2SO4 hoặc dung dịch NaOH, nên khi nhỏ ester vào hai ống nghiệm trên, tạo thành hỗn hợp không đồng nhất, chất lỏng trong cả hai ống nghiệm tách thành hai lớp.
Ester nhẹ hơn nước nên trong hỗn hợp trên, ester thuộc lớp chất lỏng phía trên.
2. Ở ống nghiệm (1): thể tích lớp chất lỏng phía trên giảm, chứng tỏ ester phản ứng chưa hết; ống nghiệm (2): tạo thành hỗn hợp đồng nhất, chứng tỏ ester phản ứng hết với dung dịch NaOH.
=> Phản ứng thủy phân ester diễn ra trong môi trường kiềm tốt hơn.
Câu hỏi 5 trang 9 Hóa học 12: Hoàn thành phương trình hóa học của các phản ứng sau
a) CH3COOC2H5 + H2O (trong dung dịch H2SO4, đun nóng).
b) HCOOCH3 + NaOH (dung dịch, đun nóng).
Lời giải:
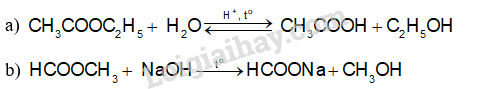
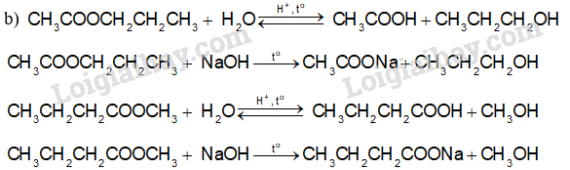
a) Viết công thức cấu tạo của propyl ethanoate và methyl butanoate.
b) Viết phương trình hoá học của phản ứng thuỷ phân propyl ethanoate và methyl butanoate trong môi trường acid và môi trường base.
Lời giải:
a)
|
Tên |
Công thức cấu tạo |
|
propyl ethanoate |
CH3COOCH2CH2CH3 |
|
methyl butanoate |
CH3CH2CH2COOCH3 |
Lời giải:
Phương trình hóa học:
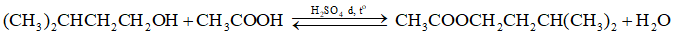
Mol: 0,173 0,27
Ta có: => isoamyl alcohol hết, ester tính theo isoamyl alcohol.
Hoạt động trang 10 Hóa học 12: Em hãy tìm hiểu và trình bày về ứng dụng của một ester mà em biết.
Lời giải:
Trong ngành chế biến thực phẩm, isoamyl acetate thường được gọi là dầu chuối. Dầu chuối là chất tạo mùi được sử dụng rất nhiều trong chế biến loại đồ ngọt.
Trong sản xuất, isoamyl acetate được sử dụng làm dung môi vecni và sơn mài nitrocellulose.
Isoamyl acetate còn được dùng làm chất dẫn dụ các đàn ong mật hoặc được dùng để kiểm tra độ hiệu quả của mặt nạ chống độc hoặc mặt nạ khí bởi đặc tính chứa mùi tạo hưng phấn, có cường độ mạnh và ít độc hại.
Lời giải:
|
CTCT của glycerol |
CTCT của palmitic acid |
CTCT của chất béo cần tìm |
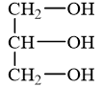 |
CH3(CH2)14COOH |
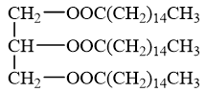 |
Lời giải:
- Nguồn omega-3 tốt nhất là cá có dầu (cá béo). Tuy nhiên, cũng có thể thu được các omega-3 này từ các nguồn hải sản khác, chẳng hạn như dầu tảo và các loại hạt như hạt chia, hạt óc chó, hạt lanh.
- Chất béo omega-6 được tìm thấy với số lượng lớn trong dầu thực vật tinh chế như dầu đậu nành, dầu ngô và các loại hạt như óc chó, hướng dương, hạnh nhân, hạt điều.
Lý thuyết Ester - Lipid
I. Ester
1. Khái niệm
- Khái niệm: Khi thay nhóm OH trong nhóm carboxylic của carboxylic acid bằng nhóm OR’ thì được ester. Trong đó, R’ là gốc hydrocarbon.
- Ester đơn chức có công thức chung là R – COO – R’, trong đó R là gốc hydrocarbon hoặc nguyên tử H, R’ là gốc hydrocarbon.
2. Danh pháp
Tên gọi của ester đơn chức: Tên ester RCOOR’ = Tên gốc R’ + Tên gốc acid RCOO
Ví dụ: HCOOCH2CH2CH3: proyl methanoate hay propyl formate
3. Tính chất vật lí
- Do không có liên kết hydrogen giữa các phân tử, ester có nhiệt độ sôi thấp hơn nhiệt độ sôi của carboxylic acid hoặc alcohol có cùng số nguyên tử carbon hoặc có khối lượng phân tử tương đương
- Ester là những chất lỏng hoặc rắn ở điều kiện thường, hầu hết nhẹ hơn nước, thường ít tan trong nước. Một số ester có mùi thơm của hoa, quả chín như: ethyl butyrate có mùi dứa chín, isomayl acetate có mùi chuối chín,…
4. Tính chất hóa học
Ester bị thủy phân trong môi trường acid hoặc môi trường base. Sản phẩm thu được khác nhau tùy thuộc vào điều kiện phản ứng
a) Phản ứng thủy phân ester trong môi trường acid như HCl, H2SO4,… thường là phản ứng thuận nghịch
Ví dụ: 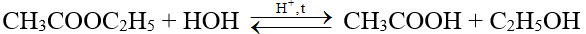
b) Phản ứng thủy phân trong môi trường base
Ester cũng bị thủy phân khi đun nóng với dung dịch kiềm như NaOH, KOH,… Phản ứng này được gọi là phản ứng xà phòng hóa.
Ví dụ: HCOOCH3 + NaOH HCOONa + CH3OH
5. Điều chế
- Các ester thường được điều chế bằng cách đun hỗn hợp gồm carboxylic acid và alcohol sử dụng H2SO4 đặc làm xúc tác.
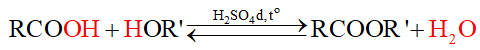
- Một số ester được điều chế bằng phương pháp khác. Chẳng hạn, trong công nghiệp, vinyl acetate được tổng hợp từ ethylene và acetic acid với sự có mặt của oxygen, sử dụng xúc tác palladium:
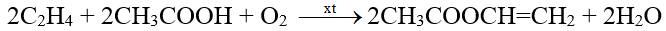
6. Ứng dụng
II. Lipid
1. Khái niệm về lipid, chất béo, acid béo
- Lipid là các hợp chất hữu cơ có trong tế bào sống, không tan trong nước nhưng tan trong dung môi hữu cơ không phân cực. Dựa trên cấu tạo, lipid được phân loại thành: chất béo, sáp, steroid, phospholipid,…
- Chất béo là triester (ester ba chức) của glycerol với acid béo, goi chung là triglyceride.
- Công thức cấu tạo chung của chất béo:
+ Acid béo là carboxylic acid đơn chức, hầu hết chúng có mạch carbon dài (thường từ 12 đến 24 nguyên tử carbon), không phân nhánh và có số nguyên tử carbon cchẳn.
+ Gốc hydrocarbon trong phân tử acid béo có thể là gốc no (acid béo bão hòa) hoặc không no chứa một hay nhiều liên kết đôi C=C
- Các chất béo hay gặp
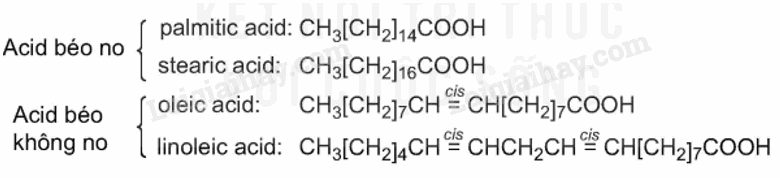
2. Tính chất vật lí của chất béo
- Ở nhiệt độ thường, chất béo ở trạng thái lỏng hoặc rắn. Khi trong phân tử chất béo chứa nhiều gốc aicd béo no thì chất béo thường ở trạng thái rắn như mỡ lợn, mỡ bò, mỡ cừu,… Khi trong phân tử chất béo chứa nhiều gốc acid béo không no thì chúng thường ở trạng thái lỏng như dầu lạc, dầu vừng, dầu cá,…
- Chất béo nhẹ hơn nước và không tan trong nước, dễ tan trong các dung môi hữu cơ ít phân cực hoặc không phân cực
3. Tính chất hóa học của chất béo
a) Phản ứng hydrogen hóa
các chất béo có gốc acid không no có thể phản ứng với hydrogen (khi có mặt xúc tác ở điều kiện thích hợp), tạo thành chất béo chứa gốc acid no

b) Phản ứng oxi hóa chất béo bởi oxygen không khí
Khi để lâu trong không khí, các gốc acid béo không no trong chất béo có thể bị oxi hóa chậm bởi oxygen, tạo thành các chất có mùi khó chịu. Đây là nguyên nhân của hiện tượng dầu mỡ bị ôi.
4. Ứng dụng của chất béo và acid béo
Chất béo là thức ăn quan trọng của con người. Trong cơ thể, chất béo bị oxi hóa thành CO2 và H2O, giải phóng năng lượng cho cơ thể. Chất béo dư thừa được tích lũy vào các mô mỡ.
- Acid béo omega – 3 và omega – 6 đều có lợi cho sức khỏe tim mạch, ngăn ngừa các bệnh về tim, động mạch vành, trong đó - linolenic acid và linoleic acid là hai acid béo thiết yếu vì cơ thể không tự tổng hợp được mà phải lấy từ nguồn thực phẩm bên ngoài.
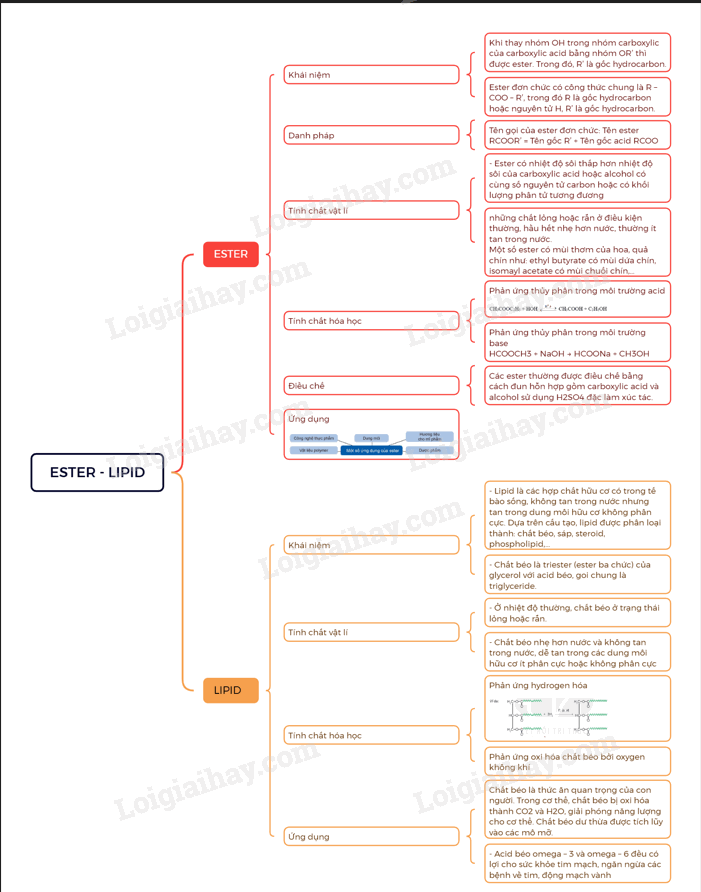
Sơ đò tư duy Ester - Lipid
Xem thêm các bài giải bài tập Hóa Học lớp 12 Kết nối tri thức hay, chi tiết khác:
Bài 2. Xà phòng và chất giặt rửa
Bài 4. Giới thiệu về carbohydrate. Glucose và fructose