Tailieumoi.vn biên soạn và giới thiệu các kiến thức lý thuyết trọng tâm bao gồm định nghĩa, tính chất, ứng dụng và cách điều chế của ankan trong bài viết dưới đây, giúp học sinh ôn tập và bổ sung kiến thức cũng như hoàn thành tốt các bài kiểm tra môn Hóa học. Mời các bạn đón xem:
I. Định nghĩa của Amin quan trọng là gì?
- Định nghĩa: Amin là sản phẩm thu được khi thay thế một hay nhiều nguyên tử hiđro trong phân tử NH3 bằng một hay nhiều gốc hiđrocacbon.
- Công thức tổng quát: CxHyNz hoặc CnH2n+2-2k+tNt
Tên gọi:
+ Tên thay thế: Tên hiđrocacbon + vị trí + amin
Ví dụ: CH3NH2 (Metanamin)
+ Tên gốc chức: Tên gốc hiđrocacbon + amin
Ví dụ: CH3NH2 (Metylamin)
+ Tên thường
II. Tính chất vật lí và nhận biết của Amin quan trọng
- Metyl–, đimetyl–, trimetyl– và etylamin là những chất khí có mùi khai khó chịu, độc, dễ tan trong nước, các amin đồng đẳng cao hơn là chất lỏng hoặc rắn.
- Anilin là chất lỏng, nhiệt độ sôi là 184°C, không màu, rất độc, ít tan trong nước, tan trong ancol và benzen.
III. Tính chất hóa học của Amin quan trọng
1. Tính Bazơ :
Do nguyên tử N trong phân tử amin còn cặp e chưa sử dụng có khả năng nhận proton.
* So sánh tính bazơ của các amin:
+ Nếu nguyên tử N trong phân tử amin được gắn với gốc đẩy e (gốc no: ankyl) thì tính bazơ của amin mạnh hơn so với tính bazơ của NH3. Những amin này làm cho quỳ tím chuyển thành màu xanh.
+ Nếu nguyên tử N trong phân tử amin gắn với các gốc hút e (gốc không no, gốc thơm) thì tính bazơ của amin yếu hơn so với tính bazơ của NH3. Những amin này không làm xanh quỳ tím.
+ Amin có càng nhiều gốc đẩy e thì tính bazơ càng mạnh, amin có càng nhiều gốc hút e thì tính bazơ càng yếu.
⇒ Lực bazơ: CnH2n + 1NH2 > HNH2 > C6H5NH2
2. Phản ứng với axit nitrơ HNO2 :
- Amin bậc một tác dụng với axit nitrơ ở nhiệt độ thường cho ancol hoặc phenol và giải phóng nitơ.
C2H5NH2 + HONO → C2H5OH + N2↑ + H2O
- Anilin và các amin thơm bậc một tác dụng với axit nitrơ ở nhiệt độ thấp (0 - 5°C) cho muối điazoni:
C6H5NH2 + HONO + HCl → C6H5N2+Cl- + 2H2O
3. Phản ứng ankyl hóa :
- Amin bậc một hoặc bậc hai tác dụng với ankyl halogenua (CH3I, …) , nguyên tử H của nhóm amin có thể bị thay thế bởi gốc ankyl:
Ví dụ: C2H5NH2 + CH3I → C2H5NHCH3 + HI
- Phản ứng này dùng để điều chế amin bậc cao từ amin bậc thấp hơn.
4. Phản ứng thế ở nhân thơm của anilin :
IV. Điều chế Amin quan trọng
- Thay thế nguyên tử H của phân tử amoniac:
NH3 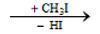
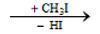
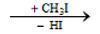
- Khử hợp chất nitro:
V. Ứng dụng Amin quan trọng
- Các ankylamin được dùng trong tổng hợp hữu cơ, đặc biệt là các điamin được dùng để tổng hợp polime.
- Anilin là nguyên liệu quan trọng trong công nghiệp phẩm nhuộm (phẩm azo, đen anilin,...), polime (nhựa anilin - fomanđehit,...), dược phẩm (streptoxit, suafaguaniđin,...)
VI. Bài tập liên quan về Amin quan trọng
Bài 1: Đốt cháy hoàn toàn m gam hỗn hợp X gồm các amin đồng đẳng của vinylamin thu được 41,8 gam CO2 và 18,9 gam H2O. Giá trị của m là:
A. 16,7 gam
B. 17,1 gam
C. 16,3 gam
D. 15,9 gam
Lời giải:
Đáp án: C
X có dạng CnH2n+1N
nN = nX = 2 × (nH2O - nCO2) = 2 × (1,05 - 0,95) = 0,2 mol.
mX = m C+ m H+ mN = 0,95 × 12 + 2,1 × 1 + 0,2 × 14 = 16,3 gam.
Bài 2: Đốt cháy hoàn toàn m gam metylamin (CH3NH2), sinh ra 2,24 lít khí N2 (ở đktc). Giá trị của m là
A. 3,1 gam.
B. 6,2 gam.
C. 4,65 gam.
D. 1,55 gam.
Lời giải:
Đáp án: B
mCH3NH2 = 0,2 × 31 = 6,2 gam
Bài 3: Cho hỗn hợp X gồm 0,15 mol H2NC3H5(COOH)2 (axit glutamic) và 0,1 mol H2N(CH2)4CH(NH2)COOH (lysin) vào 250 ml dung dịch NaOH 2M, thu được dung dịch Y. Cho HCl dư vào dung dịch Y. Sau khi các phản ứng xảy ra hoàn toàn, số mol HCl đã phản ứng là :
A. 0,75. B. 0,65. C. 0,70. D. 0,85.
Lời giải:
Đáp án: D
Tổng số mol nhóm –NH2 trong hỗn hợp X là 0,15 + 0,1.2 = 0,35 mol.
Số mol OH- = số mol của NaOH = 0,25.2 = 0,5 mol.
Bản chất của phản ứng là :
Theo (1), (2) và giả thiết ta thấy :
Số mol của HCl phản ứng = số mol của H+ phản ứng = 0,35 + 0,5 = 0,85 mol.