Tailieumoi.vn giới thiệu Giải bài tập hóa học 8 Bài 23: Bài luyện tập 4, chi tiết nhất giúp học sinh dễ dàng làm bài tập
Số mol của nguyên tử lưu huỳnh là: nS = m : M = (mol)
Số mol của nguyên tử oxi là: = m : M = (mol)
Ta có: = : =
Vậy công thức hóa học đơn giản nhất của oxit lưu huỳnh là SO3.
Khối lượng nguyên tử của mỗi nguyên tố trong 1 mol hợp chất là:
mFe = = 56 g
mS = = 32 g
mO = = 64 g
Số mol nguyên tử mỗi nguyên tố trong 1 mol hợp chất là:
nFe = = 1 mol
nS = = 1 mol
nO = = 4 mol
Suy ra 1 mol hợp chất có chứa 1 mol Fe, 1 mol S và 4 mol O.
Vậy hợp chất có công thức hóa học là FeSO4.
a) Khối lượng mol của chất đã cho.
b) Thành phần phần trăm (theo khối lượng) của các nguyên tố có trong hợp chất.
Lời giải:a) Khối lượng mol của chất đã cho: = 39 . 2 + 12 + 16 . 3 = 138 g/mol
b) Thành phần phần trăm (theo khối lượng) của các nguyên tố có trong hợp chất
%K = = 56,5 %
%C = = 8,7%
%O = = 34,8%
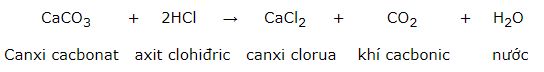
a) Tính khối lượng canxi clorua thu được khi cho 10 g canxi cacbonat tác dụng với axit clohiđric dư.
b) Tính thể tích khí cacbonic thu được trong phòng khi làm thí nghiệm, nếu có 5 g canxi cacbonat tác dụng hết với axit. Biết 1 mol khí ở điều kiện phòng có thể tích là 24 lít.
Lời giải:Phương trình hóa học:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
1 mol 1 mol 1 mol
a) Số mol canxi cacbonat tham gia phản ứng là:
= = 0,1 mol
Theo phương trình hóa học, ta có:
= = 0,1 mol
Khối lượng của canxi clorua tham gia phản ứng là:
= 0,1 . (40 + 71) = 11,1 g
b) Số mol canxi cacbonat tham gia phản ứng là:
Theo phương trình hóa học, ta có:
== 0,05 mol
Thể tích khí CO2 thu được ở điều kiện phòng là:
= 24 . 0,05 = 1,2 lít
CH4 + 2O2 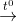 CO2 + 2H2O
CO2 + 2H2O
a) Tính thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2lít khí metan. Các thể tích khí đo cùng điều kiện t0 và p
b) Tính thể tích khí CO2 (đktc) thu được sau khi đốt cháy hoàn toàn 0,15 mol khí metan.
c) Khí metan nặng hay nhẹ hơn không khí bằng bao nhiêu lần ?
Lời giải:a) Theo phương trình hóa học:
Mà tỉ lệ về thể tích cũng là tỉ lệ về số mol, ta suy ra:
= 2.2 = 4 (lít)
b) Theo phương trình hóa học:
= 0,15 (mol)
Thể tích khí CO2 thu được ở đktc là:
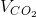 = 0,15 . 22,4 = 3,36 (lít)
= 0,15 . 22,4 = 3,36 (lít)
c) Tỉ khối của khí metan và không khí là:
Vậy khí metan nhẹ hơn không khí, bằng 0,55 lần.
1. Mol là lượng chất chứa 6. 1023 nguyên tử hoặc phân tử của chất đó.
2. Khối lượng mol (kí hiệu M) của một chất là khối lượng tính bằng gam của N nguyên tử hoặc phân tử chất đó.
3. Thể tích mol chất khí: thể tích mol của chất khí là thể tích chiếm bởi N phân tử của chất khí đó.
4. Công thức về mối liên hệ giữa số mol – khối lượng; số mol – thể tích;
n = trong đó: m: khối lượng chất
M: Khối lượng mol
n = trong đó: V: thể tích chất khí ở đktc