Cho phản ứng:
CH4(g) + H2O(l) → CO(g) + 3H2(g)
∆r = 249,9 kJ
Ở điều kiện chuẩn, để thu được 1 gam H2, phản ứng này cần hấp thu nhiệt lượng bằng bao nhiêu?
 Giải bởi Vietjack
Giải bởi Vietjack
Để đốt cháy 1 mol CH4(g) cần hấp thu 249,9 kJ nhiệt lượng
Vậy đốt cháy mol CH4(g) cần hấp thu 249,9. = 41,65 kJ nhiệt lượng.
Lý thuyết và phương pháp giải
Giả sử có phản ứng tổng quát:
aA + bB → mM + nN
Biến thiên enthalpy chuẩn của phản ứng này được tính theo công thức:
Giá trị enthalpy tạo thành chuẩn của một số chất được cho ở bảng sau:
(Trích phụ lục 3 – SGK Hóa học 10 – Cánh diều)
Chú ý:
- Với các phản ứng có kèm theo sự trao đổi năng lượng dưới dạng nhiệt, có hai khả năng sau đây:
+ Phản ứng tỏa nhiệt: biến thiên enthalpy của phản ứng có giá trị âm. Biến thiên enthalpy càng âm, phản ứng tỏa ra càng nhiều nhiệt.
+ Phản ứng thu nhiệt: biến thiên enthalpy của phản ứng có giá trị dương. Biến thiên enthalpy càng dương, phản ứng thu vào càng nhiều nhiệt.
- Các phản ứng tỏa nhiệt () thường diễn ra thuận lợi hơn các phản ứng thu nhiệt ().
CaSO4 là thành phần chính của thạch cao. Biết rằng:
2CaSO4(s) → 2CaO(s) + 2SO2(g) + O2(g) có ∆r = 1000,6 kJ.
a) Phản ứng này diễn ra thuận lợi hay không thuận lợi?
b) Giải thích vì sao trong xây dựng, người ta sử dụng thạch cao để chế tạo các tấm vật liệu chịu nhiệt, chống cháy.
Joseph Priestly (Dô-sép Prits-li) đã điều chế oxygen vào năm 1774 bằng cách nung nóng HgO(s) thành Hg(l) và O2(g). Tính lượng nhiệt cần thiết (kJ, ở điều kiện chuẩn) để điều chế được 1 mol O2 theo phương pháp này.
Biết ∆f (HgO(s)) = -90,5 kJ mol-1
Giải thích vì sao để giữ ấm cơ thể, trước khi lặn, người ta thường uống nước mắm cốt (là loại nước mắm chứa nhiều chất đạm).
Cho phản ứng sau ở điều kiện chuẩn:
H-H(g) + F-F(g) → 2H-F(g)
Tính năng lượng cần để phá vỡ các liên kết trong H2, F2 và năng lượng tỏa ra (theo kJ) khi hình thành liên kết trong HF cho phản ứng trên.
Phản ứng quang hợp là phản ứng thu năng lượng dưới dạng ánh sáng:
6nCO2(g) + 6nH2O(l) → (C6H12O6)n(s) + 6nO2(g)
Hãy tính xem cần phải cung cấp bao nhiêu năng lượng dưới dạng ánh sáng cho những phản ứng quang hợp để tạo thành 1 mol glucose C6H12O6(s), biết enthalpy tạo thành chuẩn của chất này là -1271,1 kJ mol-1. Biến thiên enthalpy tạo thành chuẩn của các chất khác tra ở phụ lục 3, trang 120.
Cho biết:
2NaHCO3(s) → Na2CO3(s) + CO2(g) + H2O(l) ∆r = 91,6 kJ
NaHCO3 có trong thành phần bột nở dùng để làm bánh. Vì sao khi bảo quản, cần tránh để bột nở ở nơi có nhiệt độ cao?
Dựa vào năng lượng liên kết, tính ∆r các phản ứng sau:
a) Các phản ứng đốt cháy hoàn toàn 1 mol mỗi chất C2H4, C2H6, H2 ở thể khí.
b) F2(g) + H2O(g) → 2HF(g) + O2(g)
Dự đoán các phản ứng trên là thuận lợi hay không thuận lợi.
Cho hai phản ứng đốt cháy:
(1) C(s) + O2(g) → CO2(g) ∆r = -393,5 kJ
(2) 2Al(s) + O2(g) → Al2O3(s) ∆ r = -1675,7 kJ
Với cùng một khối lượng C và Al, chất nào khi đốt cháy tỏa ra nhiều nhiệt hơn?
Tính ∆r cho phản ứng sau dựa theo năng lượng liên kết.
CH4(g) + X2(g) → CH3X(g) + HX(g) Với X = F, Cl, Br, I.
Liên hệ giữa mức độ phản ứng (dựa theo ∆f) với tính phi kim (F > Cl > Br > I). Tra các giá trị năng lượng liên kết ở Phụ lục 2, trang 119.
Xác định số lượng mỗi loại liên kết trong các phân tử trước và sau phản ứng của CH4 và Cl2
Vì sao khi nung vôi người ta phải xếp đá vôi lẫn với than trong lò?
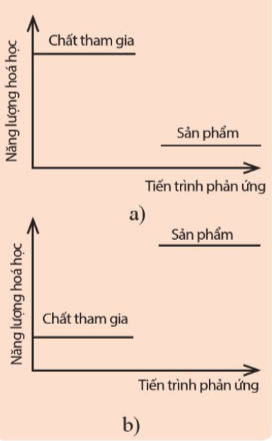
Xác định dấu của ∆r trong các phản ứng được thể hiện trong hai hình dưới đây: