Với giải Câu hỏi 6 trang 38 Hóa học lớp 10 Chân trời sáng tạo chi tiết trong Bài 5: Cấu tạo bảng tuần hoàn các nguyên tố hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 10 Bài 5: Cấu tạo bảng tuần hoàn các nguyên tố hóa học
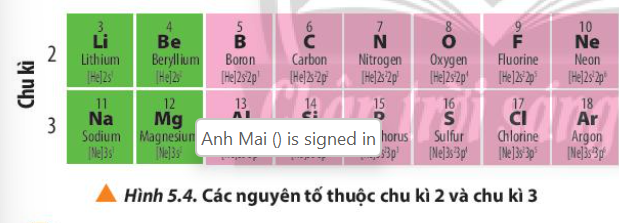
Câu hỏi 6 trang 38 Hóa học 10: Quan sát Hình 5.4, hãy nhận xét về số lớp electron trong nguyên tử của các nguyên tố cùng chu kì.
Phương pháp giải:
So sánh số lớp eletron của các nguyên tố trong 1 chu kì
Lời giải:
- Các nguyên tố thuộc chu kì 2 đều có 2 lớp electron
- Các nguyên tố thuộc chu kì 3 đều có 3 lớp electron
Lý thuyết Bảng tuần hoàn các nguyên tố hóa học
1. Ô nguyên tố
- Mỗi nguyên tố hóa học được xếp vào một ô trong bảng tuần hoàn các nguyên tố hóa học, gọi là ô nguyên tố.
- Số thứ tự của một ô nguyên tố bằng số hiệu nguyên tử của nguyên tố hóa học trong ô đó.
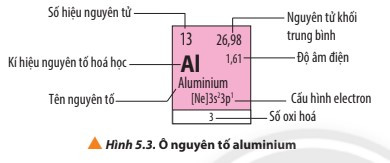
- Ví dụ: Ô nguyên tố aluminium
2. Chu kì
- Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành một hàng, gọi là chu kì.
- Số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố trong chu kì.
- Bảng tuần hoàn gồm 7 chu kì:
+ Các chu kì 1, 2 và 3 là các chu kì nhỏ.
+ Các chu kì 4, 5, 6 và 7 là các chu kì lớn.

3. Nhóm
- Nhóm là tập hợp các nguyên tố mà nguyên tử có cấu hình electron tương tự nhau (trừ nhóm VIIIB), do đó có tính chất hóa học gần giống nhau và được xếp theo cột.
- Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong nhóm.
- Bảng tuần hoàn hiện nay có 18 cột, chia thành 8 nhóm A (IA đến VIIIA) và 8 nhóm B (IB đến VIIIB). Mỗi cột tương ứng với một nhóm, riêng nhóm VIIIB có 3 cột.
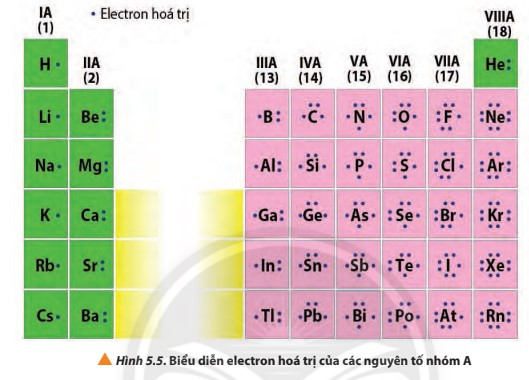
- Electron hóa trị là những electron có khả năng tham gia hình thành liên kết hóa học. Chúng thường nằm ở lớp ngoài cùng hoặc cả ở phân lớp sát lớp ngoài cùng nếu phân lớp đó chưa bão hòa. Những nguyên tố có cùng số electron hóa trị thường có tính chất hóa học tương tự nhau.
4. Phân loại nguyên tố dựa theo cấu hình electron và tính chất hóa học
- Các nguyên tố hóa học cũng có thể được chia thành các khối như sau:
+ Khối các nguyên tố s gồm các nguyên tố thuộc nhóm IA và nhóm IIA, có cấu hình electron: [Khí hiếm] ns1-2.
+ Khối các nguyên tố p gồm các nguyên tố thuộc nhóm IIIA đến VIIIA (trừ nguyên tố He), có cấu hình electron: [Khí hiếm] ns2np1-6.
+ Khối các nguyên tố d gồm các nguyên tố nhóm B, có cấu hình electron: [khí hiếm] (n – 1)d1-10ns1-2.
+ Khối các nguyên tố f gồm các nguyên tố xếp thành 2 hàng ở cuối bảng tuần hoàn, có cấu hình electron: [Khí hiếm] (n – 2)f0-14(n – 1)d0-2ns2 (trong đó n = 6 và n = 7)
- Dựa vào tính chất hóa học, người ta phân loại các nguyên tố hóa học thành:
+ Nguyên tố kim loại;
+ Nguyên tố phi kim;
+ Khí hiếm.
5. Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn
Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn:
+ Các nguyên tố được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử.
+ Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp vào cùng một chu kì.
+ Các nguyên tố có cùng số electron hóa trị trong nguyên tử được xếp vào cùng một nhóm, trừ nhóm VIIIB.
Xem thêm các bài giải Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Mở đầu trang 35 Hóa học 10: Cách đây hàng nghìn năm, người ta chỉ biết đến một số nguyên tố như đồng (copper), bạc (silver) và vàng (gold). Mãi đến năm 1700, cũng chỉ mới có 13 nguyên tố được xác định. Khi đó, các nhà hóa học nghi ngờ rằng vẫn còn nhiều nguyên tố bí ẩn khác chưa được khám phá. Bằng việc sử dụng các phương pháp khoa học hiện đại, chi trong một thập kỉ (1765 – 1775) đã có thêm 5 nguyên tố hóa học được xác định. Trong đó, có 3 khí không màu là hydrogen, nitrogen và oxygen. Tính đến năm 2016, tổng cộng đã có 118 nguyên tố hóa học được xác định trên bảng tuần hoàn các nguyên tố hóa học. Trong bảng tuần hoàn, các nguyên tố được sắp xếp theo nguyên tắc nào và có mối liên hệ như thế nào với cấu hình electron nguyên tử của nguyên tố đó?...
Câu hỏi 1 trang 36 Hóa học 10: Quan sát Hình 5.1, hãy mô tả bảng tuần hoàn các nguyên tố hóa học của Mendeleev. Nhận xét về cách sắp xếp các nguyên tố hóa học theo chiều từ trên xuống dưới trong cùng một cột...
Câu hỏi 2 trang 36 Hóa học 10: Quan sát hai nguyên tố Te và I trong Hình 5.1, em nhận thấy điều gì khác thường?...
Câu hỏi 3 trang 36 Hóa học 10: Hãy cho biết các dấu chấm hỏi trong bảng tuần hoàn ở Hình 5.1 có hàm ý gì?...
Câu hỏi 4 trang 36 Hóa học 10: Quan sát Hình 5.2, hãy cho biết 3 nguyên tố Sc, Ga và Ge nằm ở vị trí nào trong bảng tuần hoàn của Mendeleev (Hình 5.1)...
Câu hỏi 5 trang 38 Hóa học 10: Quan sát Hình 5.3, em hãy nêu các thông tin có trong ô nguyên tố aluminium...
Luyện tập 1 trang 38 Hóa học 10: Quan sát Hình 5.3, cho biết số electron lớp ngoài cùng, số proton của nguyên tử aluminium...
Luyện tập 2 trang 38 Hóa học 10: Dựa vào cấu hình electron, em hãy cho biết nguyên tố có số hiệu nguyên tử là 20 thuộc chu kì nào trong bảng tuần hoàn...
Câu hỏi 7 trang 38 Hóa học 10: Quan sát Hình 5.2, nhận xét đặc điểm cấu hình electron nguyên tử của các nguyên tố trong cùng một nhóm A...
Câu hỏi 8 trang 38 Hóa học 10: Quan sát nhóm VIIIB trong bảng tuần hoàn, cho biết nhóm này có đặc điểm gì khác biệt so với các nhóm còn lại...
Câu hỏi 9 trang 39 Hóa học 10: Quan sát Hình 5.5, nhận xét mối quan hệ giữa số electron hóa trị của nguyên tử với số thứ tự nhóm của nguyên tố nhóm A...
Câu hỏi 10 trang 39 Hóa học 10: Quan sát Hình 5.2, dựa vào cấu hình electron nguyên tử, hãy nhận xét mối quan hệ giữa số electron hóa trị của nguyên tử các nguyên tố với số thứ tự nhóm của nguyên tố nhóm B. Nêu rõ các trường hợp đặc biệt...
Câu hỏi 11 trang 39 Hóa học 10: Dựa vào cấu hình electron, cho biết nguyên tố có số hiệu nguyên tử là 6, 8, 18, 20 thuộc khối nguyên tố nào trong bảng tuần hoàn. Chúng là kim loại, phi kim hay khí hiếm?...
Luyện tập trang 40 Hóa học 10: Nitrogen là thành phần dinh dưỡng cần thiết cho sự sinh trưởng, phát triển và sinh sản của thực vật. Biết nitrogen có số hiệu nguyên tử là 7...
Câu hỏi 12 trang 40 Hóa học 10: Quan sát Hình 5.2, nhận xét chiều tăng điện tích hạt nhân nguyên tử các nguyên tố trong chu kì và nhóm...
Vận dụng trang 40 Hóa học 10: Silicon là một nguyên tố phổ biến và có nhiều ứng dụng trong cuộc sống. Silicon siêu tinh khiết là chất bán dẫn, được dùng trong kĩ thuật vô tuyến và điện tử. Ngoài ra, nguyên tố này còn được sử dụng để chế tạo pin mặt trời nhằm mục đích chuyển đổi năng lượng ánh sáng thành năng lượng điện để cung cấp cho các thiết bị trên tàu vũ trụ. Xác định vị trí của nguyên tố silicon (Z = 14) trong bảng tuần hoàn...
Bài 1 trang 42 Hóa học 10: Viết cấu hình electron nguyên tử và xác định vị trí của các nguyên tố sau trong bảng tuần hoàn. Cho biết chúng thuộc khối nguyên tố nào (s, p, d, f) và chúng là kim loại, phi kim hay khí hiếm:...
Bài 2 trang 42 Hóa học 10: Dãy nào gồm các nguyên tố có tính chất hóa học tương tự nhau? Vì sao?...
Bài 3 trang 42 Hóa học 10: Viết cấu hình electron nguyên tử của các nguyên tố sau:...
Xem thêm các bài giải SGK Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 4: Cấu trúc lớp vỏ electron của nguyên tử
Bài 5: Cấu tạo bảng tuần hoàn các nguyên tố hóa học
Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố, thành phần và một số tính chất của hợp chất trong một chu kì và nhóm
Bài 7: Định luật tuần hoàn - Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
Bài 8: Quy tắc octet



