Tailieumoi.vn xin giới thiệu phương trình CH3COOCH2CH=CH2 + HOH ⇋ CH3COOH + CH2=CHCH2OH gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học. Mời các bạn đón xem:
Phương trình CH3COOCH2CH=CH2 + HOH ⇋ CH3COOH + CH2=CHCH2OH
1. Phản ứng hóa học:
CH3COOCH2CH=CH2 + HOH 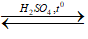
2. Điều kiện phản ứng
- Đun sôi nhẹ trong môi trường axit.
3. Cách thực hiện phản ứng
- Cho 2ml anlyl axetat vào ống nghiệm, sau đó cho tiếp dung dịch 1 ml H2SO4 20%. Lắc đều ống nghiệm rồi đun cách thủy trong 5 phút.
4. Hiện tượng nhận biết phản ứng
- Ban đầu chất lỏng trong ống nghiệm tách thành hai lớp. Sau phản ứng lượng chất lỏng trong ống nghiệm vẫn tách thành hai lớp nhưng tỉ lệ hai lớp chênh lệch so với ban đầu.
5. Tính chất hóa học
5.1. Tính chất hóa học của CH3COOC3H5
a. Phản ứng thủy phân trong mỗi trường axit
CH3COOCH2CH=CH2 + H-OH 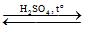
b. Phản ứng thủy phân trong mỗi trường kiềm
CH3COOCH2CH=CH2 + NaOH 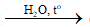
c. Phản ứng cộng H2 vào gốc không no
CH3COOCH2CH=CH2 + H2 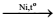
d. Phản ứng trùng hợp
Vì có liên kết C=C nên anlyl axetat tham gia phản ứng trùng hợp giống như anken
e. Phản ứng đốt cháy:
Phản ứng oxi hóa hoàn toàn tạo CO2 và H2O
CH3COOCH2CH=CH2+ 6O2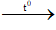
5.2. Tính chất hóa học của H2O
a. Nước tác dụng với kim loại
Nước tác dụng được với một số kim loại ở nhiệt độ thường như: Li, Na, K, Ca.. tạo thành bazo và khí H2.
2Na + 2H2O → 2NaOH + H2 ↑
2K + 2H2O → 2KOH + H2 ↑
Ca + 2H2O → Ca(OH)2 + H2 ↑
Nước tác dụng với oxit bazo tạo thành bazo tương ứng. Dung dịc bazo làm quỳ tím hóa xanh.
Na2O + H2O → 2NaOH
CaO + H2O → Ca(OH)2
Nước tác dụng với oxit axit tạo thành axit tương ứng. Dung dịch axit làm quỳ tím hóa đỏ.
SO2 + H2O → H2SO3
P2O5 + 3H2O → 2H3PO4
6. Bạn có biết
- Phản ứng trên gọi là phản ứng thủy phân este trong môi trường axit.
- Sau phản ứng còn tạo thành hai lớp chất lỏng nên phản ứng là phản ứng thuận nghịch.
7. Bài tập liên quan
Ví dụ 1: Khi thủy phân anlyl axetat trong môi trường axit thu được một sản phẩm là
A. Axit không no.
C. Ancol no.
B. Ancol thơm.
D. Ancol không no.
Hướng dẫn:
CH3COOCH2CH=CH2 + HOH 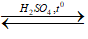
Đáp án D.
Ví dụ 2: Diều kiện xảy ra phản ứng thủy phân anlyl axetat trong môi trường axit là?
A. Dun sôi mạnh.
B. Dun sôi nhẹ.
C. Nung nóng.
D. Xảy ra ngay điều kiện thường.
Hướng dẫn:
Điều kiện phản ứng; Đun sôi nhẹ trong môi trường axit.
Đáp án B.
Ví dụ 3: Khi thủy phân anlyl axetat trong môi trường axit, chất sau phản ứng không có
A. Ancol không no.
B. Axit no.
C. Este.
D. Andehit.
Hướng dẫn: Sau phản ứng không thu được andehit.
Đáp án D.
8. Một số phương trình phản ứng hoá học khác của Este và hợp chất: