Tailieumoi.vn xin giới thiệu phương trình FeO + C → CO↑ + Fe gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học của Sắt. Mời các bạn đón xem:
Phương trình FeO + C → CO↑ + Fe
1. Phương trình phản ứng hóa học:
FeO + C → CO↑ + Fe
2. Hiện tượng nhận biết phản ứng
- Phản ứng thoát ra khí CO rất độc
3. Điều kiện phản ứng
- Nhiệt độ
4. Tính chất hoá học
4.1. Tính chất hoá học của FeO
- Mang đầy đủ tính chất hóa học của oxit bazo.
- Là chất vừa có tính oxi hóa, vừa có tính khử
Tính oxit bazơ
FeO tác dụng với dung dịch axit: HCl, H2SO2 loãng
FeO + 2HCl → FeCl2 + H2
FeO + H2SO4 loãng → FeSO4 + H2O
Tính oxi hóa
- Tác dụng với chất khử như H2, CO, Al, C…
FeO + H2 → Fe + H2O
FeO + CO → Fe + CO2
3FeO + 2Al → Al2O3 + 3Fe
Tính khử
- FeO là chất khử khi tác dụng với các chất có tính oxi hóa mạnh:
3FeO + 10HNO3 loãng → 3Fe(NO3)3 + NO + 5H2O
2FeO + 4H2SO4 (đặc) → Fe2(SO4)3 + SO2 + 4H2O
4.2. Tính chất hoá học của Cacbon
Nhận xét:
- Độ hoạt động hóa học: kim cương < than chì < cacbon vô định hình
- C là chất vừa có tính khử, vừa có tính oxi hóa
Tính khử
a. Khử oxi
Cacbon khử oxi khi đun nóng:
Ở nhiệt độ cao:
b. Khử oxit kim loại
- C khử oxit kim loại yếu, trung bình (ZnO → CuO)
2ZnO + C 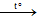
2CuO + C 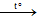
- C khử được một số oxit kim loại mạnh
CaO + 3C 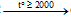
c. Khử nước
C + H2O 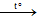
CO2 + C 
d. Khử một số hợp chất có tính oxi hóa mạnh
5. Cách thực hiện phản ứng
- Cho FeO tác dụng với cacbon
6. Bạn có biết
Ở nhiệt độ cao, Cacbon có thể khử được một số oxit kim loại như CuO, PbO, ZnO,... thành kim loại tương ứng
7. Bài tập liên quan
Ví dụ 1: Phản ứng nào sau đây tạo ra sản phẩm là muối sắt (II) sunfua
A. Sắt (II)clorua tác dụng với dung dịch hidrosunfua.
B. Sắt tác dụng với dung dịch natrisunfua.
C. Sắt tác dụng với đồng sunfua nung nóng.
D. Sắt tác dụng với bột lưu huỳnh nung nóng.
Hướng dẫn giải
Fe không phản ứng với Na2S; CuS. FeCl2 không phản ứng với H2S
Đáp án : D
Ví dụ 2: Dung dịch FeCl2 có màu gì?
A. Dung dịch không màu.
B. Dung dịch có màu nâu đỏ.
C. Dung dịch có màu xanh nhạt.
D. Dung dịch màu trắng sữa.
Hướng dẫn giải
Đáp án : C
Ví dụ 3: Cho kim loại X tác dụng với dung dịch HCl loãng dư thu được dung dịch Y. Cho dung dịch Y tác dụng với dung dịch NaOH dư thu được kết tủa Z màu trắng xanh sau một thời gian kết tủa chuyển sang màu nâu đỏ. Kim loại X là kim loại:
A. Al
B. Cu
C. Zn
D. Fe
Hướng dẫn giải
Fe + 2HCl → FeCl2 + H2
FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
8Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
Đáp án : D
8. Một số phương trình phản ứng hoá học khác của Sắt (Fe) và hợp chất:
3FeO + 2NH3 → 3Fe + 3H2O + N2↑
FeO + 2AgNO3 → Ag2O↓ + Fe(NO3)2