Tailieumoi.vn xin giới thiệu phương trình Cu + HNO3 → Cu(NO3)2 + NO+ H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học. Mời các bạn đón xem:
Phương trình Cu + HNO3 → Cu(NO3)2 + NO+ H2O
1. Phương trình phản ứng hóa học
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO+ 4H2O
2. Hiện tượng nhận biết phản ứng.
- Kim loại Cu rắn đỏ dần tạo thành dung dịch màu xanh lam và khí không màu hóa nâu trong không khí thoát ra.
3. Điều kiện phản ứng
- Dung dịch HNO3 loãng dư
4. Cân bằng phương trình phản ứng
Xác định sự thay đổi số oxi hóa
Cuo + HN+5O3→ Cu+2(NO3)2+ N+2O + H2O
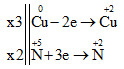
Vậy 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Nhắc lại kiến thức: Các bước cân bằng phản ứng bằng phương pháp thăng bằng electron
Bước 1. Viết sơ đồ phản ứng với các chất tham gia xác định nguyên tố có số oxi hóa thay đổi
Bước 2. Viết phương trình:
Khử (Cho electron)
Oxi hóa (nhận electron)
Bước 3. Cân bằng electron: Nhân hệ số để
Tổng số electron cho = tổng số electron nhận
Bước 4. Cân bằng nguyên tố: nói chung theo thứ tự
Kim loại (ion dương)
Gốc axit (ion âm)
Môi trường (axit, bazo)
Nước (cân bằng H2O là để cân bằng hidro)
Bước 5. Kiểm tra số nguyên tử oxi ở hai vế (phải bằng nhau)
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của Cu (Đồng)
- Trong phản ứng trên Cu là chất khử.
- Cu là kim loại phản ứng được với các axit oxi hoá mạnh như axit HNO3 và H2SO4 đặc, nóng.
5.2. Bản chất của HNO3 (Axit nitric)
- Trong phản ứng trên HNO3 là chất oxi hoá.
- Đây là một monoaxit mạnh, có tính oxi hóa mạnh có thể nitrat hóa nhiều hợp chất vô cơ.
6. Tính chất hóa học
Axit nitric có tính chất của một axit bình thường nên nó làm quỳ tím chuyển sang màu đỏ.
Tác dụng với bazo, oxit bazo, muối cacbonat tạo thành các muối nitrat
2HNO3 + CuO → Cu(NO3)2 + H2O
2HNO3 + Mg(OH)2 → Mg(NO3)2 + 2H2O
2HNO3 + BaCO3→ Ba(NO3)2 + H2O + CO2
Tác dụng với hầu hết các kim loại trừ Au và Pt tạo thành muối nitrat và nước .
Kim loại + HNO3 đặc → muối nitrat + NO + H2O ( to)
Mg + HNO3 đặc
Kim loại + HNO3 loãng → muối nitrat + NO + H2O
Kim loại + HNO3loãng lạnh → muối nitrat + H2
Mg(rắn) + 2HNO3 loãng lạnh → Mg(NO3)2 + H2 (khí)
Nhôm, sắt, crom thụ động với axit nitric đặc nguội do lớp oxit kim loại được tạo ra bảo vệ chúng không bị oxy hóa tiếp.
(Các nguyên tố á kim, ngoại trừ silic và halogen) tạo thành nito dioxit nếu là axit nitric đặc và oxit nito với axit loãng và nước, oxit của phi kim.
C + 4HNO3 đặc → 4NO2 + 2H2O + CO2
FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O
FeCO3 + 4HNO3 → Fe(NO3)3+ NO2 + 2H2O + CO2
3Fe(OH)2 + 10HNO3 → 3Fe(NO3)3 + NO + 8H2O
3H2S + 2HNO3 (>5%) → 3S ↓+ 2NO + 4H2O
Ag3PO4 tan trong HNO3, HgS không tác dụng với HNO3.
6.2. Tính chất hóa học của Cu (Đồng)
Đồng là loại kim loại có tính khử yếu hơn so với các kim loại khác. Đồng có thể tác dụng được với phi kim, tác dụng với các axit và tác dụng với các dung dịch muối
a. Tác dụng với phi kim
Khi (Cu) phản ứng với Oxi đun nóng sẽ tạo thành CuO bảo vệ do đó (Cu) sẽ không bị oxi hoá.
2Cu + O2→ CuO
Khi ta đun nóng đến nhiệt độ từ (800-1000oC)
CuO + Cu → Cu2O (đỏ)
Khi tác dụng trực tiếp với khí Cl2, Br2, S…
Cu + Cl2 → CuCl2
Cu + S → CuS
b. Tác dụng với các axit
(Cu) không thể tác dụng với dung dịch HCl và H2SO4 loãng.
Khi có oxi, (Cu) có thể tác dụng với dung dịch HCl, có tiếp xúc giữa axit và không khí.
2Cu + 4HCl + O2 → 2CuCl2 + 2H2O
Đối với HNO3, H2SO4 đặc thì:
Cu + 2H2SO4 đặc → CuSO4 + SO2 + H2O
Cu + 4HNO3 (đặc) → Cu(NO3)2 + 2NO2+ 2H2O
c. Tác dụng với các dung dịch muối
Đồng có thể khử được các ion kim loại đứng sau nó trong dung dịch muối.
Cu + 2AgNO3→ Cu(NO3)2 + 2Ag
7. Cách thực hiện phản ứng
- Cho đồng Cu tác dụng với dung dịch axit nitric HNO3
8. Bạn có biết
- Hiện tại chúng tôi không có thêm bất kỳ thông tin nào thêm về phương trình này.
9. Bài tập liên quan
Câu 1. Ứng dụng nàosau đây không phải của HNO3?
A. Để điều chế phân đạm NH4NO3, Ca(NO3)2
B. Sản xuất dược phẩm
C. Sản xuất khí NO2 và N2H4
D. Để sản xuất thuốc nổ, thuốc nhuộm
Lời giải:
Một số ứng dụng của axit HNO3 như chế tạo thuốc nổ (TNT, …), điều chế các hợp chất hữu cơ, sản xuất bột màu, sơn, thuốc nhuộm, …
⇒ Sản xuất khí NO2 và N2H4 không phải ứng dụng của HNO3.
Câu 2. Phát biểu nào sau đây đúng:
A. Dung dịch HNO3 làm xanh quỳ tím và làm phenolphtalein hóa đỏ.
B. Axit nitric được dùng để sản xuất phân đạm (NH4NO3, Ca(NO3)2), thuốc nổ (TNT), thuốc nhuộm, dược phẩm.
C. Trong công nghiệp, để sản xuất HNO3 người ta đun hỗn hợp (KNO3) với H2SO4 đặc
D. điều chế HNO3 trong phòng thí nghiệm người ta dùng khí amoniac (NH3)
Lời giải:
Axit nitric được dùng để sản xuất phân đạm (NH4NO3, Ca(NO3)2), thuốc nổ (TNT), thuốc nhuộm, dược phẩm.
A Sai: dung dịch HNO3 chỉ làm xanh quỳ tím hóa đỏ.
C. Trong công nghiệp để sản xuất axit nitric, người ta thường đun nóng hỗn hợp natri nitrat rắn với dung dịch H2SO4 đặc
D. Để điều chế HNO3 trong phòng thí nghiệm người ta dùng NaNO3 và H2SO4 đặc
Câu 3. Trong các thí nghiệm với dung dịch HNO3 thường sinh ra khí độc NO2. Để hạn chế khí NO2 thoát ra từ ống nghiệm, người ta sử dụng biện pháp nhét bông có tẩm hóa chất và nút ống nghiệm. Hóa chất đó chính là
A. H2O
B. Dung dịch nước vôi trong
C. dung dịch giấm ăn
D. dung dịch muối ăn
Lời giải:
Phương trình phản ứng minh họa
4NO2 + 2Ca(OH)2 → Ca(NO3)2 + 2H2O + Ca(NO2)2
Khí màu nâu đỏ NO2 bị hòa tan trong dung dịch, tạo thành chất rắn Ca(NO2)2 và Ca(NO3)2
Câu 4. Chất nào sau đây không tạo kết tủa khi cho vào dung dịch AgNO3:
A. HCl
B. HNO3
C. KBr
D. K3PO4
Lời giải:
Phương trình phản ứng
AgNO3 + HCl → AgCl + HNO3
AgNO3 + KBr → AgBr + KNO3
3AgNO3 + K3PO4 → Ag3PO4 + 3KNO3
Câu 5. Cho 19,2 gam Cu tan hoàn toàn trong dung dịch HNO3 loãng dư, sau phản ứng thu được V lít NO (đktc, sản phẩm khử duy nhất). Giá trị của V là:
A. 6,72 lít
B. 2,24 lít
C. 3,36 lít
D. 4,48 lít
Lời giải:
Phương trình phản ứng hóa học
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO↑ + 4H2O
2nCu = 3nNO
=> nNO = 0,2 mol
=> V = 4,48 lit
Câu 6. Cho phương trình hóa học sau: Fe + HNO3 → Fe(NO3)3 + NO + H2O
Tổng hệ số tối giản của phương trình sau:
A. 8
B. 9
C. 12
D. 16
Lời giải:
Cân bằng phương trình hóa học sau: Fe + HNO3 → Fe(NO3)3 + NO + H2O
Tổng hệ số tối giản của phương trình sau 9
Câu 7. Cho Cu (z = 29), vị trí của Cu trong bảng tuần hoàn là
A. ô 29, chu kỳ 4, nhóm IB.
B. ô 29, chu kỳ 4, nhóm IA.
C. ô 29, chu kỳ 4, nhóm VIIIB.
D. ô 29, chu kỳ 4, nhóm IIB.
Lời giải:
Nguyên tố X có Z = 29 => Cấu hình X là 1s22s22p63s23p63d104s1
=> X thuộc ô thứ 29, chu kì 4, phân nhóm IB
Câu 8. Chỉ dùng 1 chất để phân biệt 3 kim loại sau: Al, Ba, Mg?
A. Dung dịch HCl
B. Nước
C. Dung dịch NaOH
D. Dung dịch H2SO4
Lời giải:
Để phân biệt 3 kim loại Al, Ba, Mg ta dùng nước. Cho nước vào 3 mẫu kim loại, kim loại tốt trong nước và sủi bọt khí là Ba, 2 kim loại không tan trong nước là Al và Mg.
Ba + 2H2O → Ba(OH)2 + H2 ↑
- Lấy dung dịch Ba(OH)2 vừa thu được đổ vào mẫu 2 kim loại còn lại, kim loại nào tan, sủi bọt khí là Al, kim loại không có hiện tượng gì là Mg
2Al + Ba(OH)2 + 2H2O → Ba(AlO2)2 + 3H2 ↑
Câu 9. Cho các dung dịch: HCl, NaOH đặc, NH3, KCl. Số dung dịch phản ứng được với Cu(OH)2 là
A. 1.
B. 3.
C. 2.
D. 4.
Lời giải:
Các dung dịch phản ứng được với Cu(OH)2 là HCl, NH3
Phương trình phản ứng minh họa
Cu(OH)2 + HCl → CuCl2 + H2O
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2
Câu 10. Hiện tượng nào xảy ra khi cho mảnh đồng kim loại vào dung dịch HNO3 loãng
A. không có hiện tượng gì
B. dung dịch có màu xanh, H2 bay ra
C. dung dịch có màu xanh, có khí màu nâu bay ra
D. dung dịch có màu xanh lam, có khí không màu bay ra, bị hoá nâu trong không khí.
Lời giải:
Phương trình hóa học
Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O
→ Hiện tượng: Dung dịch có màu xanh của Cu(NO3)2 và khí màu nâu đỏ NO2.
Câu 11. Chỉ dùng 1 hóa chất nào sau đây để nhận biết các dung dịch: NH4Cl, NaOH, NaCl, H2SO4, Na2SO4, Ba(OH)2?
A. Dung dịch phenolphtalein.
B. Dung dịch AgNO3.
C. Dung dịch quỳ tím.
D. Dung dịch BaCl2.
Đáp án C
Để nhận biết các dụng dịch trên ta dùng dung dịch quỳ tím ta chia thành 3 nhóm
Nhóm (I): quỳ tím hóa đỏ : NH4Cl, H2SO4
Nhóm (II) quỳ tím hóa xanh: NaOH, Ba(OH)2
Nhóm (III): quỳ tím không đổi màu: NaCl, Na2SO4
Cho lần lượt từng chất ở nhóm (II) vào từng chất ở nhóm (I)
|
|
NH4Cl |
H2SO4 |
|
NaOH |
Khí mùi khai |
Không hiện tượng |
|
Ba(OH)2 |
Khí mùi khai |
Kết tủa trắng |
Phương trình phản ứng minh họa
NH4Cl + NaOH → NH3 + H2O + NaCl
2NH4Cl + Ba(OH)2 BaCl2 + 2NH3 ↑ + 2H2O
Ba(OH)2 + H2SO4 → BaSO4+ 2H2O
Cho Ba(OH)2 nhận biết được vào từng chất ở nhóm (III), chất tạo kết tủa trắng là Na2SO4, chất không hiện tượng là NaCl
Phương trình phản ứng minh họa
Ba(OH)2 + Na2SO4 → BaSO4 + 2 NaOH
10. Một số phương trình phản ứng hoá học khác của Đồng (Cu) và hợp chất:
Cu + HNO3 → Cu(NO3)2 + NO+ H2O
Cu + S → CuS
Cu + Br2 → CuBr2
Cu + HCl + 1/2O2 → CuCl2 + H2O
Cu + H2S + 1/2O2 → CuS + H2O
Cu + H2SO4 + 1/2O2 → CuSO4 + H2O
Cu + 4HNO3 (đặc, nóng) → Cu(NO3)2 + NO2 + 2H2O
Cu + 2H2SO4 (đặc, nóng) → CuSO4 + SO2 + 2H2O
3Cu + 8HCl + 8NaNO3 → 3Cu(NO3)2 + 2NO + 8NaCl + 4H2O
3Cu + 8HCl + 2NaNO3 → 3CuCl2 + 2NO + 2NaCl + 4H2O
3Cu + 8HCl + 8KNO3 → 3Cu(NO3)2 + 2NO + 8KCl + 4H2O
3Cu + 8HCl + 2KNO3 → 3CuCl2 + 2NO + 2KCl + 4H2O
Cu + H2O + O2 + CO2 → Cu2CO3(OH)2
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Cu + 2Fe(NO3)3 → Cu(NO3)2 + 2Fe(NO3)2