Tailieumoi.vn xin giới thiệu phương trình K2Cr2O7 + HCl → CrCl3 + KCl + Cl2 + H2O gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học. Mời các bạn đón xem:
Phương trình K2Cr2O7 + HCl → CrCl3 + KCl + Cl2 + H2O
1. Phương trình phản ứng hóa học
K2Cr2O7(da cam) + 14HCl → 2CrCl3(vàng) + 2KCl + 3Cl2(vàng lục) + 7H2O
2. Cân bằng phản ứng K2Cr2O7 + HCl → CrCl3 + KCl + Cl2 + H2O
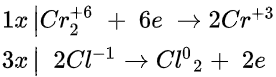
Phương trình phản ứng: K2Cr2O7 + 14HCl → 2CrCl3 + 2KCl + 3Cl2 + 7H2O
3. Hiện tượng nhận biết phản ứng
- Xuất hiện khí màu vàng lục Clo (Cl2) làm sủi bọt khí.
4. Điều kiện phản ứng
- Nhiệt độ thường
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của K2Cr2O7 (Kali dicromat)
- Trong phản ứng trên K2Cr2O7 là chất oxi hoá.
- K2Cr2O7 là một chất oxi hoá mạnh tác dụng được với các axit.
5.2. Bản chất của HCl (Axit clohidric)
Trong phản ứng trên HCl là chất khử.
6. Tính chất hóa học
6.1. Tính chất hóa học của K2Cr2O7
4K2Cr2O7 4K2CrO4 + 2Cr2O3 + 3O2
K2Cr2O7 + 2KOH → 2K2CrO4 + H2O
(da cam) (vàng)
K2Cr2O7 + 14HCl → 2CrCl3 + 2KCl + 3Cl2 + 7H2O
K2Cr2O7 + 3SO2 + H2SO4 → Cr2(SO4)3 + K2SO4 + H2O
K2Cr2O7 + 6FeSO4 + 7H2SO4 → Cr2(SO4)3 + 3Fe2(SO4)3 + K2SO4 + 7H2O
Ở trạng thái rắn, K2Cr2O7 có thể oxi hóa được S.
6.2. Tính chất hóa học của HCl
Dung dịch axit HCl có đầy đủ tính chất hoá học của một axit mạnh.
a/ Tác dụng chất chỉ thị:
Dung dịch HCl làm quì tím hoá đỏ (nhận biết axit)
HCl → H+ + Cl-
b/ Tác dụng với kim loại
Tác dụng với KL (đứng trước H trong dãy Bêkêtôp) tạo muối (với hóa trị thấp của kim loại) và giải phóng khí hidrô (thể hiện tính oxi hóa)
Fe + 2HCl 
2Al + 6HCl 
Cu + HCl → không có phản ứng
c/ Tác dụng với oxit bazo và bazo:
Sản phẩm tạo muối và nước
NaOH + HCl → NaCl + H2 O
CuO + 2HCl 
Fe2 O3 + 6HCl
d/ Tác dụng với muối (theo điều kiện phản ứng trao đổi)
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
AgNO3 + HCl → AgCl↓ + HNO3
(dùng để nhận biết gốc clorua )
Ngoài tính chất đặc trưng là axit , dung dịch axit HCl đặc còn thể hiện vai trò chất khử khi tác dụng chất oxi hoá mạnh như KMnO4, MnO2, K2 Cr2O7, MnO2, KClO3 ……
4HCl + MnO2 
K2 Cr2 O7 + 14HCl → 3Cl2 + 2KCl + 2CrCl3 + 7H2 O
Hỗn hợp 3 thể tích HCl và 1 thể tích HNO3 đặc được gọi là hỗn hợp nước cường toan ( cường thuỷ) có khả năng hoà tan được Au ( vàng)
3HCl + HNO3 → 2Cl + NOCl + 2H2O
NOCl → NO + Cl
Au + 3Cl → AuCl3
7. Mở rộng kiến thức về muối Crom(VI)
- Muối cromat như natri cromat (Na2CrO4) và kali cromat (K2CrO4) là muối của axit
cromic,có màu vàng của ion cromat (CrO42-).
- Muối đicromat như natri đicromat Na2Cr2O7 và kali đicromat K2Cr2O7 là muối của axit
đicromat, có màu da cam của ion đicrom Cr2O72-
- Các muối cromat và đicromat có tính oxi hóa mạnh, đặc biệt trong môi trường axit muối
crom(VI) bị khử thành muối crom(III).
K2Cr2O7 + 6KI + 7H2SO4 → Cr2(SO4)3 + 4K2SO4 + 3I2 + 7H2O.
K2Cr2O7 + 14HCl → 2KCl + 3CrCl3 + 3Cl2 + 7H2O
8. Mở rộng kiến thức về HCl
8.1. Tính chất vật lí
- Hiđro clorua tan vào nước tạo thành dung dịch axit clohiđric.
- Axit clohiđric là chất lỏng, không màu, mùi xốc.
- Dung dịch HCl đặc nhất (ở 20oC) đạt tới nồng độ 37% và có khối lượng riêng D = 1,19 g/cm3.
- Dung dịch HCl đặc “bốc khói” trong không khí ẩm. Đó là do hiđro clorua thoát ra tạo với hơi nước trong không khí thành những hạt dung dịch nhỏ như sương mù.
8.2. Tính chất hóa học
Axit clohiđric là một axit mạnh, mang đầy đủ tính chất hóa học của một axit như:
- Làm quỳ tím chuyển sang màu đỏ.
- Tác dụng với kim loại đứng trước (H) trong dãy hoạt động hóa học của kim loại.
Ví dụ:
Mg + 2HCl → MgCl2 + H2
2Al + 6HCl → 2AlCl3 + 3H2
Chú ý: Kim loại có nhiều hóa trị tác dụng với dung dịch HCl thu được muối trong đó kim loại ở mức hóa trị thấp. Ví dụ:
Fe + 2HCl → FeCl2 + H2
- Tác dụng với oxit bazơ và bazơ tạo thành muối và nước. Ví dụ:
CuO + 2HCl CuCl2 + H2O
Fe2O3 + 6HCl 2FeCl3 + 3H2O
NaOH + HCl → NaCl + H2O
Cu(OH)2 + 2HCl → CuCl2 + 2H2O
- Tác dụng với muối của axit yếu hơn tạo thành muối mới và axit mới. Ví dụ:
CaCO3 + 2HCl → CaCl2 + H2O + CO2 ↑
AgNO3 + HCl → AgCl↓ + HNO3
Ngoài tính chất đặc trưng là tính axit, dung dịch axit HCl đặc còn thể hiện tính khử khi tác dụng chất oxi hoá mạnh như KMnO4, MnO2, K2Cr2O7, MnO2, KClO3…
8.3. Điều chế
a) Trong phòng thí nghiệm
- Điều chế hiđro clorua bằng cách cho tinh thể NaCl vào dung dịch H2SO4 đậm đặc và đun nóng (phương pháp sunfat) rồi hấp thụ vào nước để được axit clohiđric.
- Phương trình hóa học minh họa:
2NaCltt + H2SO4 đặc Na2SO4 + 2HCl ↑
NaCltt + H2SO4 đặc NaHSO4 + HCl ↑
b) Trong công nghiệp
- Phương pháp tổng hợp: Đốt H2 trong khí quyển Cl2
H2 + Cl2 2HCl
9. Cách thực hiện phản ứng
- Cho dung dịch axit HCl tác dụng với K2Cr2O7
10. Bạn có biết
- Hiện tại chúng tôi không có thêm bất kỳ thông tin nào thêm về phương trình này.
11. Bài tập liên quan
Câu 1. Cho phản ứng K2Cr2O7 + HCl → KCl + CrCl3 + Cl2 + H2O. Số phân tử HCl đóng vai trò môi trường là
A. 3
B. 6
C. 8
D.14
Lời giải:
Câu 2. Trong phản ứng
K2Cr2O7 + HCl → CrCl3 + KCl + Cl2 + H2O
Tổng hệ số cân bằng tối giản của phản ứng là
A. 28
B. 29
C. 30
D. 31
Lời giải:
Phương trình hóa học
K2Cr2O7 + 14HCl → 2CrCl3 + 2KCl + 3Cl2 + 7H2O
Tổng hệ số cân bằng trong phương trình là: 1 + 14 + 2 + 2 + 3 + 7 = 29
Câu 3. Khi cho dung dịch kiềm vào dung dịch K2Cr2O7 thì có hiện tượng
A. Màu da cam của dung dịch chuyển thành không màu
B. Dung dịch không màu chuyển thành màu vàng
C. Màu vàng của dung dịch chuyển thành màu da cam
D. Màu da cam của dung dịch chuyển thành màu vàng
Lời giải:
Khi cho dung dịch kiềm vào dung dịch K2Cr2O7 thì có hiện tượng màu da cam của dung dịch chuyển thành màu vàng
Cr2O72- (màu da cam ) + 2OH- → 2CrO42- (màu vàng)+ H2O
Câu 4. Cho các phát biểu sau:
(1). K2Cr2O7 có màu da cam, là chất oxi hóa mạnh.
(2). Kim loại Al và Cr đều phản ứng với dung dịch HCl theo cùng tỷ lệ.
(3). CrO3 là một oxit axit, là chất oxi mạnh, bốc cháy khi tiếp xúc với lưu huỳnh, photpho,...
(4). Cr2O3 được dùng để tạo màu lục cho đồ sứ, đồ thủy tinh.
(5). Hợp chất crom (VI) vừa có tính oxi hóa, vừa có tính khử.
(6). Crom (III) oxit và crom (III) hiđroxit đều là chất có tính lưỡng tính.
Tổng số phát biểu đúng là
A. 2
B. 3
C. 4.
D. 5
Lời giải:
(1) đúng
(2) Sai , Cr tác dụng HCl tỉ lệ 1 :2
(3) Đúng
(4) Đúng
(5) Sai, Crom (VI) chỉ có tính oxh
(6) Đúng
Câu 5. Khi cho Kalidicromat vào dung dịch HCl dư đun nóng xảy ra phản ứng:
K2Cr2O7 + HCl → KCl + CrCl3 + Cl2 + H2O
Nếu dùng 5,88 gam K2Cr2O7 thì số mol HCl bị Oxi hóa là:
A. 0,14 mol.
B. 0,28 mol.
C. 0,12 mol.
D. 0,06 mol.
Lời giải:
Số mol HCl bị oxi hóa chính là số mol HCl chuyển thành Cl2
Phương trình phản ứng hóa học
K2Cr2O7 + 14HCl → 2KCl + 2CrCl3 + 3Cl2 + 7H2O
⇒ nHCl bị OXH = 2nCl2 = 6nK2Cr2O7 = 6 × 0,02 = 0,12 mol
Câu 6. Nung hỗn hợp bột gồm 15,2 gam Cr2O3 và m gam Al ở nhiệt độ cao. Sau khi phản ứng hoàn toàn thu được 23,3 gam hỗn hợp rắn X. Cho toàn bộ hỗn hợp X phản ứng với axit HCl dư thấy thoát ra V lit khí H2 (dktc). Giá trị của V là :
A. 10,08 lit
B. 4,48 lit
C. 7,84 lit
D. 3,36 lit
Lời giải:
Áp dụng Bảo toàn khối lượng:
mAl + mCr2O3 = mX
=> nAl = 0,3 mol; nCr2O3 = 0,1 mol
Phương trình phản ứng hóa học
2Al + Cr2O3 → Al2O3 + 2Cr
Sau phản ứng có: nCr= 0,2 mol ;
nAl= 0,1 mol là phản ứng với axit tạo H2
Phương trình phản ứng hóa học
Cr + 2HCl → CrCl2 + H2
Al + 3HCl → AlCl3 + 1,5H2
=> nH2 = nCr+ nAl.1,5 = 0,35 mol
=> VH2 = n.22,4 = 0,35.22,4 = 7,84 lit
Câu 7. Crom không phản ứng với chất nào sau đây ?
A. dung dịch H2SO4 loãng, đun nóng
B. dung dịch HNO3 đặc nguội
C. dung dịch HNO3 đặc, đun nóng
D. dung dịch H2SO4 đặc, đun nóng
Lời giải:
Câu 8. Khối lượng K2Cr2O7 cần dùng để oxi hoá hết 0,3 moi FeSO4 trong môi trường dung dịch H2SO4 loãng là:
A. 29,4 gam
B. 59,2 gam.
C. 24,9 gam.
D. 14,7 gam
Lời giải:
K2Cr2O7 + 6FeSO4 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4+ 7H2O
0,05 ← 0,3 (mol)
mK2Cr2O7 = 0,05.294 = 14,7 gam
Câu 9. Muốn điều chế 6,72 lít khí Clo (đktc) thì khối lượng K2Cr2O7 tối thiều cần dùng đế tác dụng với dung dịch HCl đặc, dư là
A. 29,4 gam.
B. 27,4 gam.
C. 24,9 gam.
D. 26,4 gam
Lời giải:
Ta có: nCl2= = 0,3 (mol)
Phương trình hóa học
K2Cr2O7 + 14HCl → 2CrCl3 + 2KCl + 3Cl2 + 7H2O
Theo phương trình hóa học: nK2Cr2O7= nCl2= .0,3 = 0,1 (mol)
Khối lượng K2Cr2O7 tối thiểu cần lấy là: nK2Cr2O7= 0,1.294 = 29,4(g)
Câu 10. Dung dịch FeSO4 không làm mất màu dung dịch nào sau đây?
A. Dung dịch K2Cr2O7 trong môi trường H2SO4
B. Dung dịch KMnO4 trong môi trường H2SO4
C. Dung dịch Br2 trong môi trường H2SO4
D. Dung dịch NaOH
Lời giải:
Các dung dịch KMnO4/ H2SO4; K2Cr2O7/ H2SO4;
Br2 đều là các chất oxi hóa → Fe2+ sẽ có phản ứng oxi hóa khử làm mất màu các dung dịch trên
6FeSO4 + K2Cr2O7 + 7H2SO4→ 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
2FeSO4+ Br2 + H2SO4→ Fe2(SO4)3+ 2HBr
Câu 11. Dãy các chất chỉ thể hiện tính oxi hóa là:
A. HNO3; KMnO4; Fe(NO3)3
B. O2; H2SO4 đặc
C. HNO3; KMnO4; Fe(NO3)2
D. KMnO4, Zn, HCl
Lời giải:
Chất chỉ thể hiện mình tính oxh tức là số oxh cao nhất O2; H2SO4 đặc
A sai vì Fe(NO3)3 thể hiện cả tính khử và tính oxi hóa
B đúng
C sai do Fe(NO3)2 thể hiện cả tính khử và tính oxi hóa
D sai do HCl thể hiện cả 2 tính còn Zn là chất khử
Câu 12. Khi cho dung dịch kiềm vào dung dịch K2Cr2O7 thì có hiện tượng
A. Màu da cam của dung dịch chuyển thành không màu
B. Dung dịch không màu chuyển thành màu vàng
C. Màu vàng của dung dịch chuyển thành màu da cam
D. Màu da cam của dung dịch chuyển thành màu vàng
Lời giải:
Khi cho dung dịch kiềm vào dung dịch K2Cr2O7 thì có hiện tượng màu da cam của dung dịch chuyển thành màu vàng
Cr2O72- (màu da cam ) + 2OH- → 2CrO42- (màu vàng)+ H2O
Câu 13. Chọn phát biểu đúng về phản ứng của crom với phi kim:
A. Ở nhiệt độ thường crom chỉ phản ứng với flo.
B. Ở nhiệt độ cao, oxi sẽ oxi hóa crom thành Cr(VI).
C. Lưu huỳnh không phản ứng được với crom.
D. Ở nhiệt độ cao, clo sẽ oxi hóa crom thành Cr(II).
Lời giải:
B sai vì oxi phản ứng với crom tạo Cr2O3
C sai vì lưu huỳnh có phản ứng với crom ở nhiệt độ cao
D sai vì clo sẽ oxi hóa crom thành CrCl3
Câu 14. Các kim loại nào sau đây luôn được bảo vệ trong môi trường không khí, nước nhờ lớp màng oxit?
A. Al và Ca.
B. Fe và Cr.
C. Cr và Al
D. Fe và Mg.
Lời giải:
Câu 15. Nhận xét nào sau đây là không đúng?
A. Crom là kim loại cứng nhất trong tất cả các kim loại
B. Nhôm và crom đều bị thụ động hóa bởi HNO3 đặc nguội.
C. Nhôm và crom đều bị phản ứng với HCl theo cùng tỉ lệ số mol.
D. Vật dụng làm bằng nhôm và crom đều bền trong không khí và nước vì có màng oxit bảo vệ.
Lời giải:
Phương trình phản ứng minh họa
Al + 3HCl → AlCl3 + 3/2H2
Cr + 2HCl → CrCl2 + H2
Câu 16. Cho vào ống nghiệm một vài tinh thể K2Cr2O7, sau đó thêm tiếp khoảng 1 ml nước và lắc đều để K2Cr2O7tan hết, thu được dung dịch X. Thêm vài giọt dung dịch KOH vào dung dịch X, thu được dung dịch Y. Màu sắc của dung dịch X và Y lần lượt là
A. màu da cam và màu vàng chanh.
B. màu vàng chanh và màu da cam.
C. màu nâu đỏ và màu vàng chanh.
D. màu vàng chanh và màu nâu đỏ.
Lời giải:
Cr2O72- + 2OH- ⇆ 2CrO42- + H2O
màu da cam màu vàng
Khi nhỏ từ từ dung dịch KOH vào dung dịch K2Cr2O7thì cân bằng trên chuyển dịch sang phải
=> dung dịch chuyển từ màu da cam sang màu vàng
Câu 17. Dung dịch trong nước của chất nào dưới đây có màu da cam?
A. K2Cr2O7.
B. KCl.
C. K2CrO4.
D. KMnO4
Lời giải:
A. dung dịch K2Cr2O7 có màu da cam
B. dung dich KCl không có màu
C. dung dich K2CrO4 có màu vàng.
D. dung dich KMnO4 có màu tím
Câu 18. Cho Br2 vào dung dịch CrCl3 trong môi trường NaOH thì sản phẩm thu được có chứa:
A. CrBr3.
B. Na[Cr(OH)4].
C. Na2CrO4.
D. Na2Cr2O7.
Lời giải:
Phương trình phản ứng
2CrCl3 + 3Br2 + 16NaOH → 2Na2CrO4 + 6NaBr + 6NaCl + 8H2O
12. Một số phương trình phản ứng hoá học khác của Kali (K) và hợp chất:
Cr2O3 + 6HCl(đặc) → 2CrCl3 + 3H2O
Cr2O3 + 2NaOH(đặc) → 2NaCrO2 + H2O
Cr2O3 + 2KOH(đặc) → 2KCrO2 + H2O
Cr2O3 + 2Al → 2Cr + Al2O3
6FeSO4 + K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + 7H2O