Với giải Bài 3 trang 32 Chuyên đề Hóa học 10 Chân trời sáng tạo chi tiết trong Bài 4: Entropy và biến thiên năng lượng tự do Gibbs giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Chuyên đề Hóa 10. Mời các bạn đón xem:
Giải bài tập Chuyên đề Hóa học 10 Bài 4: Entropy và biến thiên năng lượng tự do Gibbs
Bài 3 trang 32 Chuyên đề Hóa học 10: Cho phản ứng hóa học:
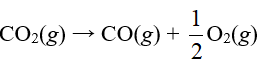
a) Ở điều kiện chuẩn và 25oC phản ứng trên có tự xảy ra được không?
b) Nếu coi và không phụ thuộc vào nhiệt độ, hãy cho biết ở nhiệt độ nào phản ứng trên có thể tự xảy ra ở điều kiện chuẩn?
Lời giải:
⇒ Phản ứng trên không tự xảy ra.
b) Để phản ứng trên tự xảy ra, cần có:
Xem thêm lời giải bài tập Chuyên đề Hóa học 10 Chân trời sáng tạo hay, chi tiết khác:
Câu hỏi 1 trang 27 Chuyên đề Hóa học 10: Tại sao khi tăng nhiệt độ lại làm tăng entropy của hệ?...