Tailieumoi.vn giới thiệu Giải bài tập Hóa học 9 Bài 24: Ôn tập học kì 1 chính xác, chi tiết nhất giúp học sinh dễ dàng làm bài tập Bài 24: Ôn tập học kì 1 lớp 9.
Giải bài tập Hóa học 9 Bài 24: Ôn tập học kì 1
Bài 1 trang 71 SGK Hóa 9: Viết các phương trình hoa học biểu diễn các chuyển hóa sau đây :
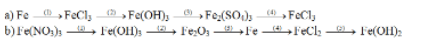
Lời giải:

Phương pháp giải:
Các dãy chuyển hóa có thể có:
Dãy biến hóa 1:
Dãy biến hóa 2:
Lời giải:
Các dãy chuyển hóa có thể có:
Dãy biến hóa 1:
Dãy biến hóa 2:

Dựa vào tính chất hóa học khác nhau của các kim loại để chọn hóa chất nhận biết chúng
Gợi ý: Dùng dung dịch NaOH để nhận biết ra Al
Dùng dung dịch HCl để nhận biết ra Fe
Lời giải:
Phân biệt Al, Ag, Fe: Cho dung dịch NaOH vào ba kim loại trên, kim loại nào tác dụng và có bọt khí bay lên là Al, hai kim loại còn lại (Fe, Ag) không tác dụng.
- Cho dung dịch HCl vào hai kim loại Fe và Ag, kim loại nào tác dụng và có khí bay lên là Fe, kim loại nào không tác dụng là Ag.
A. .
B. NaOH, CuO, Ag, Zn.
C. .
D. .
Phương pháp giải:
Ghi nhớ tính chất hóa học của axit H2SO4
+ Làm quỳ tím chuyển sang màu đỏ
+ Tác dụng với oxit bazo, bazo
+ Tác dụng với muối ( điều kiện tạo ra chất kết tủa hoặc bay hơi)
+ Tác dụng với kim loại ( đứng trước H trong dãy điện hóa)
Lời giải:
A. Loại Cu và không tác dụng ( vì Cu đứng sau H trong dãy điện hóa)
B. Loại Ag không tác dụng ( vì Ag đứng sau H trong dãy điện hóa)
C. Loại NaCl không tác dụng ( vì sản phẩm không sinh ra chất kết tủa hoặc bay hơi)
D. Chọn
3H2SO4 + 2Al → Al2(SO4)3 + 3H2↑
3H2SO4 + Al2O3 → Al2(SO4)3 + 3H2O↑
H2SO4 + Fe(OH)2 → FeSO4 + 2H2O
H2SO4 + BaCl2 → BaSO4 ↓ + 2HCl
Đáp án D
A. .
B. .
C. .
D. .
Phương pháp giải:
Ghi nhớ tính chất hóa học của dd NaOH
+ Làm quỳ tím chuyển sang màu xanh
+ Tác dụng với oxit axit, tác dụng với axit
+ Tác dụng với dd muối ( điều kiện tạo ra chất kết tủa hoặc bay hơi)
Đặc biệt: dd NaOH tác dụng với kim loại Al, Zn, Al(OH)3 và Zn(OH)2
Lời giải:
A. Loại CuO
B. Chọn
C. Loại KNO3 không tác dụng ( vì sản phẩm không tạo chất kết tủa hoặc bay hơi)
D. Loại HgO và BaCl2
2NaOH + H2SO4 → Na2SO4 + H2O
2NaOH + SO2 → Na2SO3 + H2O
Hoặc NaOH + SO2 → NaHSO3
2NaOH + CO2 → Na2CO3 + H2O
Hoặc NaOH + CO2 → NaHCO3
2NaOH + FeCl2 → Fe(OH)2↓ + 2NaCl
Đáp án B
A. Nước vôi trong.
B. Dung dịch HCl.
C. Dung dịch NaCl.
D. Nước.
Giải thích và viết phương trình phản ứng hóa học nếu có.
Phương pháp giải:
Lời giải:
Giải thích: Chọn nước vôi trong là tốt nhất, vì nước vôi trong có phản ứng với tất cả các chất khí thải tạo thành chất kết tủa hay dung dịch.
Phương trình hóa học:
.
.
.
.
Đáp án A
Phương pháp giải:
Lời giải:
Bạc dạng bột có lẫn tạp chất đồng, nhôm. Làm sạch tạp chất để thu được bạc tinh khiết bằng cách: Cho hỗn hợp vào dung dịch dư, đồng và nhôm sẽ phản ứng, kim loại thu được là Ag.
Phương pháp giải:
H2SO4 đặc dùng để làm khô các khí mà không có phản ứng với nó
CaO khan dùng để làm khô các khí mà không có phản ứng với nó
Lời giải:
Lập bảng để thấy chất nào có phản ứng với chất làm khô
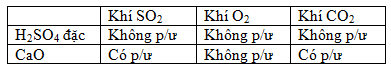
Kết luận: Có thể dùng đặc để làm khô các khí ẩm: vì đặc không phản ứng với các khí này. Có thể dùng CaO khan để làm khô khí ẩm . CaO khan tác dụng với khí ẩm khi đó các khí này sẽ sinh ra các chất khác không còn là chất ban đầu nữa nên không thể làm khô chúng được.
Phương trình hóa học:
Hoặc
Bài 9 trang 72 SGK Hóa 9: Cho 10g dung dịch muối sắt clorua 32,5% tác dụng với dung dịch bạc nitrat dư thì tạo thành 8,61g kết tủa. Hãy tìm công thức hóa học của muối sắt đã dùng.
Phương pháp giải:
Vì Fe là kim loại có nhiều hóa trị nên gọi hóa trị của Fe là x
Viết PTHH
tính toán theo PTHH số mol của FeClx theo số mol của AgCl => suy ra được x
Lời giải:
Đặt công thức muối sắt clorua là: FeClx với khối lượng =
Phương trình hóa học: FeClx + xAgNO3 → Fe(NO3)x + xAgCl↓
Theo phương trình ta có tỉ lệ:
=> x = 3
Vậy công thức của muối sắt là FeCl3
a) Viết phương trình hóa học.
b) Xác định nồng độ mol của chất trong dung dịch khi phản ứng kết thúc. Giả thiết rằng thể tích của dung dịch sau phản ứng thay đổi không đáng kể.
Phương pháp giải:
a) PTHH:
b) Từ PTHH xác định đươc chất nào phản ứng hết, chất nào còn dư, mọi tính toán theo chất phản ứng hết
Công thức nồng độ mol CM = n : V
Lời giải:
Số mol =
Số mol Fe =
a) Phương trình hóa học.
Ta có tỉ lệ: dư
Theo phương trình :
b) Nồng độ mol của các chất trong dung dịch:
dư = 0,07 – 0,035 = 0,035 mol
.