Với giải Hoạt động thí nghiệm 1 trang 22 Hóa học 12 Kết nối tri thức chi tiết trong Bài 4: Giới thiệu về carbohydrate. Glucose và fructose giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 12. Mời các bạn đón xem:
Giải bài tập Hóa học 12 Bài 4: Giới thiệu về carbohydrate. Glucose và fructose
Hoạt động thí nghiệm 1 trang 22 Hóa học 12: Thí nghiệm: Phản ứng của glucose với Cu(OH)2
Chuẩn bị:
Hoá chất dung dịch CuSO4 5%, dung dịch NaOH 10%, dung dịch glucose 2%.
Dụng cụ: ống nghiệm.
Tiến hành:
Cho khoảng 2 mL dung dịch NaOH 10% vào ống nghiệm. Sau đó, thêm khoảng 0,5 mL dung dịch CuSO4 5% vào, lắc nhẹ.
Cho tiếp khoảng 3 mL dung dịch glucose 2% vào ống nghiệm và lắc đều.
Quan sát hiện tượng xảy ra, giải thích và viết phương trình hoá học.
Lời giải:
- Hiện tượng:
+ Khi nhỏ dung dịch CuSO4 vào dung dịch NaOH, xuất hiện kết tủa màu xanh lam.
+ Nhỏ dung dịch glucose vào ống nghiệm chứa kết tủa, lắc đều, kết tủa tan.
- Giải thích:
+ Kết tủa màu xanh lam thu được khi nhỏ dung dịch CuSO4 vào dung dịch NaOH là Cu(OH)2.
+ Nhỏ dung dịch glucose vào ống nghiệm chứa kết tủa, lắc đều, kết tủa tan vì glucose hoà tan copper(II) hydroxide tạo thành dung dịch có màu xanh lam.
Lý thuyết Glucose – Fructose
1. Cấu tạo phân tử
- Glucose có công thức phân tử C6H12O6. Phân tử glucose ở dạng mạch hở có năm nhóm – OH và 1 nhóm – CHO với công thức cấu tạo là CH2O[CHOH]4CH=O.
- Glucose tồn tại ở dạng mạch hở và mạch vòng.
- Fructose có công thức phân tử C6H12O6, phân tử dạng mạch hở chứa 5 nhóm – OH và 1 nhóm – CO. Fructose tồn tại ở dạng mạch hở và mạch vòng.
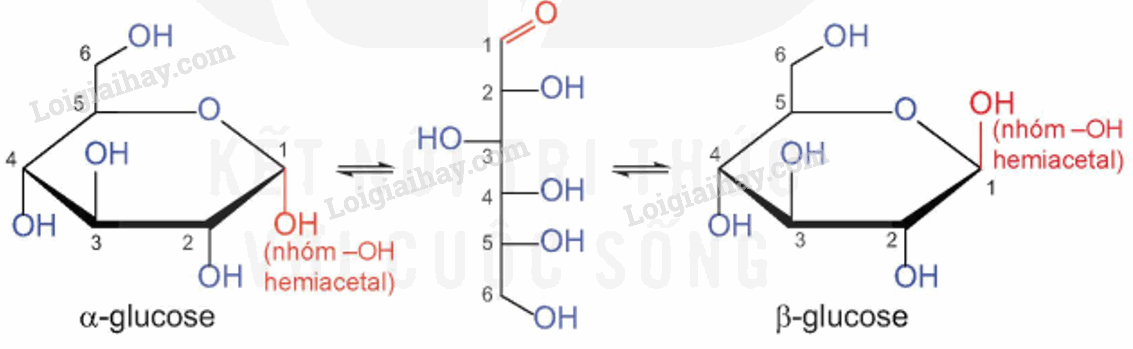
Trong môi trường kiềm, glucose và fructose có thể chuyển hóa qua lại.
2. Tính chất hóa học
a) Tính chất polyalcohol.
Phân tử glucose và fructose có nhiều nhóm – OH liền kề nên dung dịch glucose và dung dịch fructose có thể hòa tan copper(II) hydroxide trong môi trường kiềm, tạo thành dung dịch có màu xanh lam.
2C6H12O6 + Cu(OH)2 (C6H12O6)2Cu + 2H2O
b) Tính chất aldehyde
- Nhóm – CHO của glucose có thể bị oxi hóa bởi Cu(OH)2 trong môi trường kiềm khi đun nóng, tác dụng với thuốc thử Tollens và phản ứng với bromine
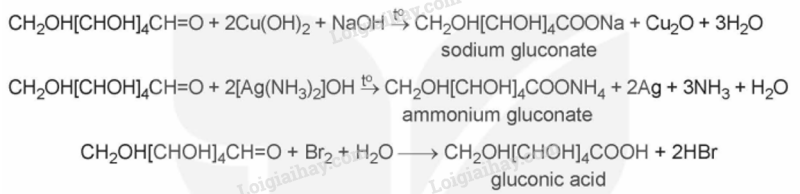
- Tương tự glucose, fructose cũng bị oxi hóa bởi thuốc thử Tollens và bởi Cu(OH)2 trong môi trường kiềm.
c) Tính chất của nhóm – OH hemiacetal
Ở dạng cấu tạo mạch vòng, nhóm – OH hemiacetal của glucose tác dụng với methanol khi có mặt của HCl khan, tạo thành methyl glucoside
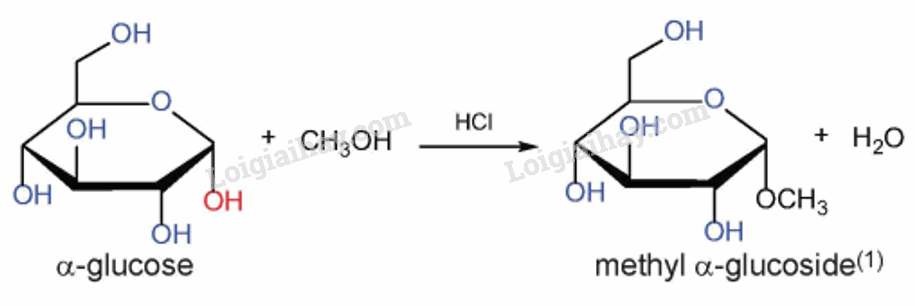
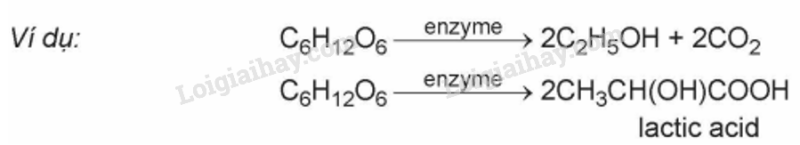
d) Phản ứng lên men của glucose
Dưới tác dụng của các enzyme từ các vi sinh vật khác nhau, glucose được lên men tạo thành các hợp chất có nhiều ứng dụng trong đời sống như ethanol, lactic acid,….
3. Trạng thái tự nhiên và ứng dụng
a) Glucose
- Glucose là chất rắn, dễ tan trong nước, có vị ngọt
- Glucose có nhiều trong hoa quả chín, có trong cơ thể người và động vật. Trong máu người trưởng thành, khỏe mạnh hàm lượng glucose nằm trong khoảng 4,4 – 7,2 mmol/L
- Ứng dụng của glucose:
b) Fructose
- Fructose là chất rắn, dễ tan trong nước, có vị ngọt
- Fructose có nhiều trong loại trái cây và mật ong. Fructose có nhiều ứng dụng trong ngành công nghiệp thực phẩm, y tế,…
Xem thêm lời giải bài tập Hóa học lớp 12 Kết nối tri thức hay, chi tiết khác:
Hoạt động 1 trang 20 Hóa học 12: Xét công thức cấu tạo mạch hở của hai carbohydrate sau:...
Hoạt động thí nghiệm 1 trang 22 Hóa học 12: Thí nghiệm: Phản ứng của glucose với Cu(OH)2...
Hoạt động thí nghiệm 2 trang 23 Hóa học 12: Thí nghiệm: Tính chất aldehyde của glucose...
Xem thêm các bài giải bài tập Hóa Học lớp 12 Kết nối tri thức hay, chi tiết khác: