Với tóm tắt lý thuyết Khoa học tự nhiên lớp 8 Bài 11: Muối sách Kết nối tri thức hay, chi tiết cùng với bài tập trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn KHTN 8.
Khoa học tự nhiên 8 Bài 11: Muối
A. Lý thuyết KHTN 8 Bài 11: Muối
I. Khái niệm
- Phản ứng tạo muối là quá trình tạo ra muối từ sự kết hợp giữa cation kim loại và anion gốc acid thông qua phản ứng giữa acid và kim loại hoặc oxide base.
- Các phản ứng tạo muối trong bảng 11.1 đều có thành phần phân tử gồm cation kim loại và anion gốc acid.
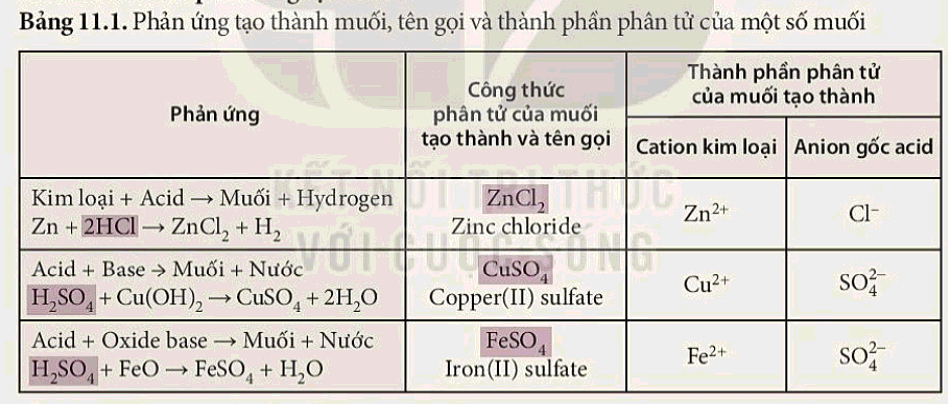
- Nhận xét về cách gọi tên muối
+ Muối được đặt tên theo quy tắc : Tên kim loại (hoá trị, đối với kim loại nhiều hoá trị) + tên gốc acid.
- Thành phần phân tử của muối gồm cation kim loại và anion gốc acid.
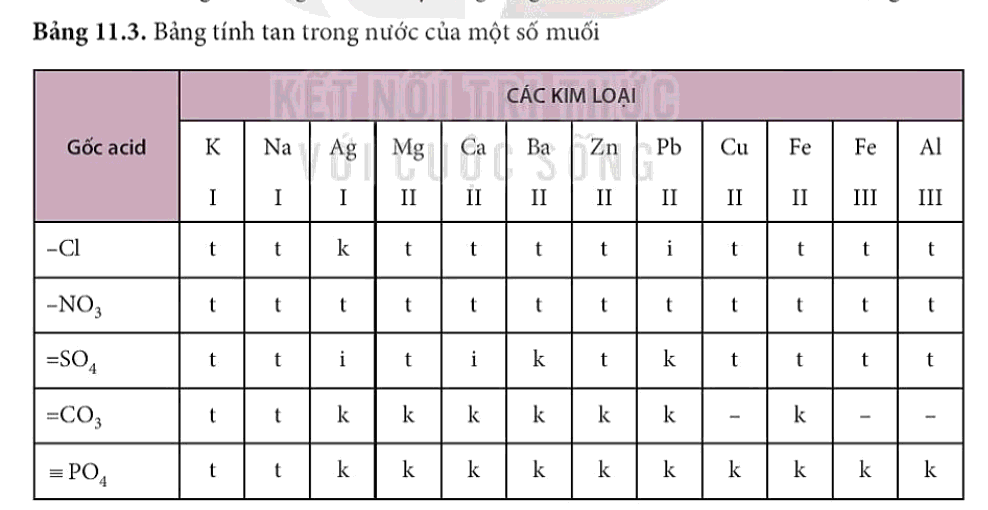
- Đa số các muối là chất rắn, có muối không tan hoặc tan ít trong nước. Các bảng tính tan được xây dựng để tiện sử dụng.
- Dung dịch muối có thể tác dụng với một số kim loại tạo thành muối mới và kim loại mới.
- Muối có thể tác dụng với một số dung dịch acid tạo thành muối mới và acid mới, sản phẩm của phản ứng có thể là chất ít tan hoặc không tan.
- Dung dịch muối tác dụng với dung dịch base
- Dung dịch muối tác dụng với dung dịch base tạo thành muối mới và base mới, trong đó có ít nhất một sản phẩm là chất khi/chất ít tan/không tan..
Vi du: FeSO4+2NaOH→→ Fe(OH)2+ Na2SO4
- Dung dịch muối tác dụng với dung dịch muối
- Hai dung dịch muối tác dụng với nhau tạo thành hai muối mới, trong đó ít nhất có một muối không tan hoặc ít tan.
- Muối có thể điều chế bằng một số phương pháp như sau:
+ Dung dịch acid tác dụng với base.
+ Dung dịch acid tác dụng với muối.
+ Oxide acid tác dụng với dung dịch base.
Sơ đồ tư duy KHTN 8 Bài 11: Muối
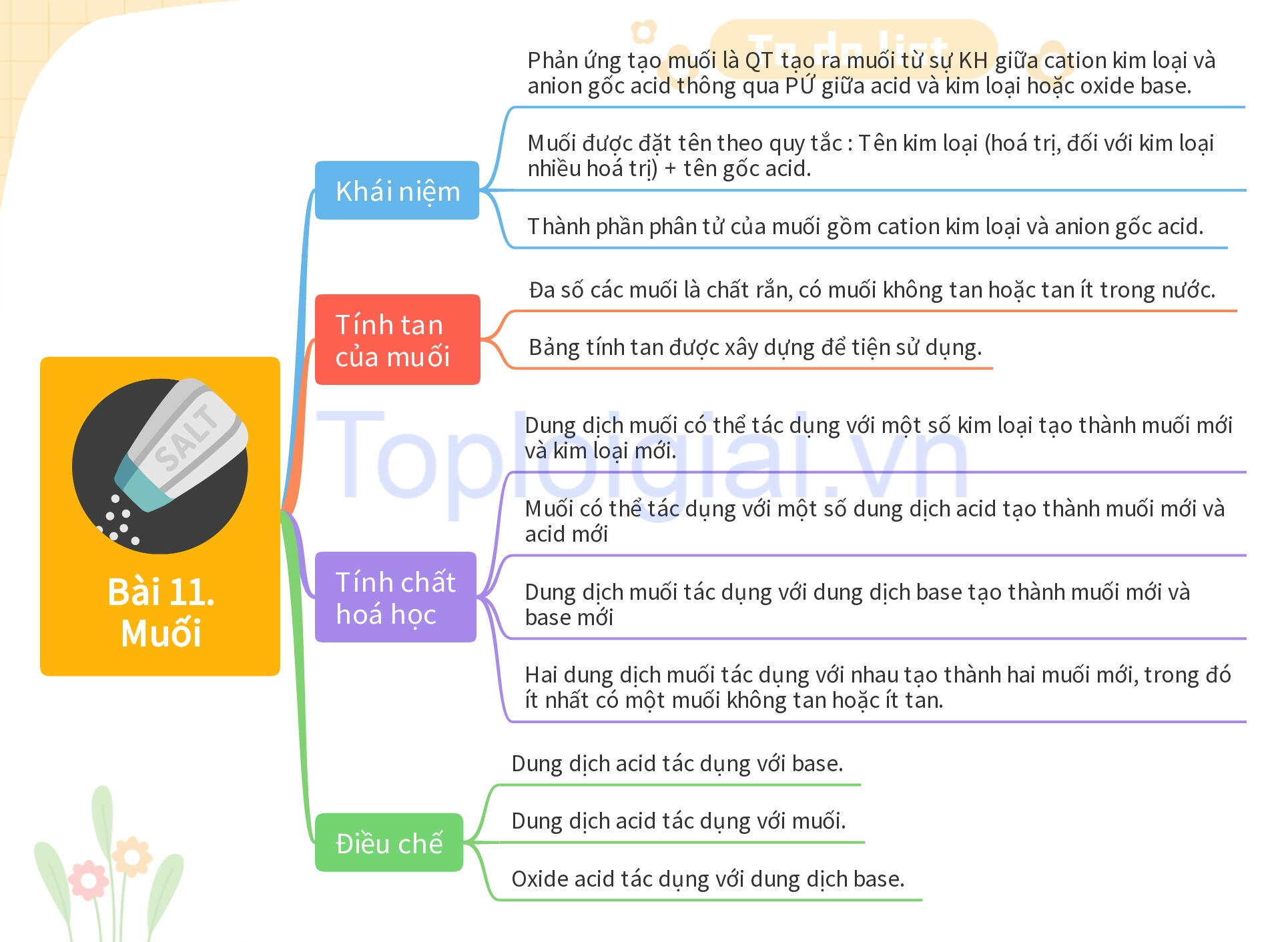
B. Bài tập trắc nghiệm KHTN 8 Bài 11: Muối
Câu 1. Phản ứng nào sau đây không tạo ra muối?
A. Acid tác dụng với base.
B. Kim loại tác dụng với oxygen.
C. Acid tác dụng với oxide base.
D. Base tác dụng với oxide acid.
Đáp án đúng là: B
Kim loại tác dụng với oxygen sinh ra oxide.
Câu 2. Hợp chất nào sau đây không phải là muối?
A. Calcium hydroxide.
B. Sodium sulfite.
C. Calcium sulfite.
D. Sodium sulfate.
Đáp án đúng là: A
Calcium hydroxide là base.
Câu 3. Trong số những chất có công thức hoá học dưới đây, dung dịch chất nào không làm đổi màu quỳ tím?
A. HNO3.
B. NaCl.
C. NaOH.
D. KOH.
Đáp án đúng là: B
Dung dịch NaCl không làm đổi màu quỳ tím.
Câu 4. Cho sơ đồ phản ứng sau:
? + 2HCl → ZnCl2 + H2
Chất thích hợp để điền vào vị trí dấu hỏi là
A. Zn(OH)2.
B. ZnO.
C. Zn.
D. ZnCO3.
Đáp án đúng là: C
Zn + 2HCl → ZnCl2 + H2
Câu 5. Công thức của copper(II) sulfate là
A. CuS.
B. CuSO4.
C. CaSO4.
D. CoSO4.
Đáp án đúng là: B
Công thức của copper(II) sulfate là CuSO4.
Câu 6. Chất nào sau đây thuộc loại muối?
A. Ca(OH)2.
B. Fe2O3.
C. H2SO4.
D. CaCl2.
Đáp án đúng là: D
Chất thuộc loại muối là: CaCl2.
Câu 7. Cho dãy các chất: KCl, Cu(OH)2, BaO, MgCO3, ZnCl2, KOH, CuSO4, NH4NO3. Số lượng muối có trong dãy là
A. 3. B. 4.
C. 5. D. 6.
Đáp án đúng là: C
Các chất là muối có trong dãy: KCl; MgCO3; ZnCl2; CuSO4; NH4NO3.
Câu 8. Hợp chất Na2SO4 có tên gọi là
A. sodium sulfate.
B. sodium sulfite.
C. potassium sulfate.
D. sodium sulfuric.
Đáp án đúng là: A
Na2SO4: sodium sulfate.
Câu 9. Muối nào sau đây tan tốt trong nước?
A. KCl.
B. BaCO3.
C. CaCO3.
D. AgCl.
Đáp án đúng là: A
Muối KCl tan tốt trong nước.
Câu 10. Trong các muối NaCl, CaCO3, KNO3, BaSO4, CuSO4, AgCl, MgCO3, số lượng muối tan trong nước là
A. 3. B. 4.
C. 5. D. 6.
Đáp án đúng là: A
Số lượng muối tan trong nước là 3, gồm: NaCl; KNO3; CuSO4.
Câu 11. Cho dãy các muối sau: Al2(SO4)3; Na2SO4; K2SO4; BaCl2; CuSO4. Muối nào trong dãy có gốc kim loại mang hóa trị II?
A. K2SO4; BaCl2.
B. BaCl2; CuSO4.
C. Al2(SO4)3.
D. Na2SO4.
Đáp án đúng là: B
Các muối thoả mãn: BaCl2; CuSO4.
Câu 12. Dãy chất nào sau đây chỉ gồm các muối?
A. MgCl2; Na2SO4; KNO3.
B. Na2CO3; H2SO4; Ba(OH)2.
C. CaSO4; HCl; MgCO3.
D. H2O; Na3PO4; KOH.
Đáp án đúng là: A
Dãy chỉ gồm các muối: MgCl2; Na2SO4; KNO3.
Câu 13. Cho 0,1 mol NaOH tác dụng với 0,2 mol HCl, sản phẩm sinh ra sau phản ứng là muối NaCl và nước. Khối lượng muối NaCl thu được là
A. 11,7. B. 5,85.
C. 4,68. D. 9,87.
Đáp án đúng là: B
NaOH + HCl → NaCl + H2O
0,1 0,2 mol
Sau phản ứng HCl còn dư, nên số mol muối sinh ra tính theo NaOH.
Theo phương trình hoá học:
nNaCl = nNaOH = 0,1 (mol).
Vậy mNaCl = 0,1.58,5 = 5,85 (gam).
Câu 14. Cho sơ đồ phản ứng sau:
Na2CO3 + ? BaCO3 + NaCl
Chất phù hợp để điền vào dấu ? là
A. BaCl.
B. BaCl2.
C. BaClO.
D. Ba(ClO)2.
Đáp án đúng là: B
Na2CO3 + BaCl2 → BaCO3 + 2NaCl
Câu 15. Cho 0,1 mol CuSO4 tác dụng với dung dịch Ba(OH)2 dư, thu được kết tủa có khối lượng là
A. 9,8 gam.
B. 33,1 gam.
C. 23,3 gam.
D. 31,3 gam.
Đáp án đúng là: B
CuSO4 + Ba(OH)2 → Cu(OH)2↓ + BaSO4↓
0,1 → 0,1 0,1 mol
Kết tủa sau phản ứng gồm: Cu(OH)2 0,1 mol và BaSO4 0,1 mol
Khối lượng kết tủa thu được sau phản ứng là: 0,1.98 + 0,1.233 = 33,1 gam.