Tailieumoi.vn sưu tầm và biên soạn chuyên đề Anken gồm đầy đủ lý thuyết, các dạng bài tập chọn lọc và ví dụ minh họa từ cơ bản đến nâng cao giúp học sinh ôn luyện kiến thức, biết cách làm bài tập môn Hóa học 11.
Chuyên đề Anken
I. LÍ THUYẾT TRỌNG TÂM
1. Đồng đẳng, đồng phân, danh pháp
a. Dãy đồng đẳng anken là những hiđrocacbon mạch hở, trong phân tử có 1 liên kết đôi C=C, có công thức phân tử chung là .
Ví dụ: C2H4, C3H6, C4H8,…
b. Đồng phân
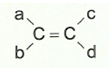
Đồng phân cis-: có mạch chính nằm ở cùng phía liên kết đôi.
Đồng phân trans-: có mạch chính nằm ở hai phía khác nhau của liên kết đôi.
Điều kiện để có đồng phân hình học: .
c. Danh pháp
Tên thông thường: Từ tên ankan cùng số cacbon, đổi đuôi “an” thành đuôi “ilen”.
Tên thay thế của anken = Số chỉ vị trí nhánh
+ Tên nhánh
+ Tên mạch chính
+ số chỉ vị trí liên kết đôi + en
Mạch chính: Mạch dài nhất có chứa liên kết đôi.
Đánh số thứ tự trên mạch chính từ phía gần liên kết đôi hơn.
Gọi tên nhánh theo thứ tự vần chữ cái cùng với số chỉ của nhánh.
Ví dụ: C2H4 : etilen; C3H6 : propilen; C4H8 : butilen
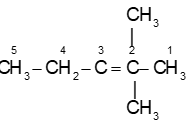
Đọc tên: 2,3-đimetylpent-2-en.
2. Tính chất vật lí
Điều kiện thường, các anken từ C2H4 đến C4H8 là chất khí, từ C5H10 trở đi là chất lỏng hoặc rắn.
Nhiệt độ sôi, nhiệt độ nóng chảy và khối lượng riêng của anken tăng theo chiều tăng của phân tử khối.
Các anken nhẹ hơn trước, hầu như không tan trong nước.
3. Tính chất hóa học
Liên kết đôi C=C gồm 1 liên kết bền và 1 liên kết kém bền, dễ bị phân cắt trong các phản ứng hóa học.
a. Phản ứng cộng
Ví dụ:
Ví dụ:
(màu nâu đỏ) (không màu)
Dùng dung dịch brom làm thuốc thử để nhận biết anken.
Ví dụ:
Các anken có cấu tạo phân tử không đối xứng khi cộng HX có thể cho hỗn hợp hai sản phẩm.
Quy tắc cộng Mac-côp-nhi-côp định hướng sản phẩm chính: nguyên tử H được cộng vào nguyên tử C có nhiều H hơn.
Ví dụ:
b. Phản ứng trùng hợp
Phản ứng trùng hợp là quá trình kết hợp liên tiếp nhiều phân tử nhỏ giống nhau hoặc tương tự nhau (monome) tạo thành những phân tử rất lớn gọi là polime.
Điều kiện để monome tham gia phản ứng trùng hợp là phân tử phải có liên kết
Ví dụ:
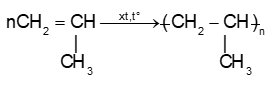
c. Phản ứng oxi hóa
Ví dụ:
Nhận xét: Khi đốt anken luôn có
Ví dụ:
(etylen glicol)
Nhận xét: Các đồng đẳng của anken đều làm mất màu dung dịch thuốc tím (KMnO4).
4. Điều chế
a. Trong phòng thí nghiệm
Etilen được điều chế từ ancol etylic
b. Trong công nghiệp
Các anken được điều chế từ ankan bằng phản ứng tách hiđro:
Ví dụ:
5. Ứng dụng
Các anken và dẫn xuất của anken là nguyên liệu cho nhiều quá trình sản xuất hóa học.
Dùng làm chất đầu tổng hợp các polime có nhiều ứng dụng như chất dẻo PE, PVC…

Nguyên liệu cho công nghiệp hóa học
Dung môi, axit hữu cơ.
II. CÁC DẠNG BÀI TẬP
Dạng 1: Lí thuyết liên quan đến đồng phân, danh pháp, tính chất của anken, điều chế ứng dụng của anken
Kiểu hỏi 1: Đặc điểm phân tử, danh pháp
Ví dụ mẫu
Ví dụ 1: Anken X có công thức cấu tạo: Tên của X là
A. isohexan. B. 3-metylpent-3-en.
C. 3-metylpent-2-en. D. 2-etylbut-2-en.
Hướng dẫn giải
Mạch chính có chứa liên kết đôi C=C, có 5C.
Đánh số thứ tự để số chỉ vị trí liên kết đôi nhỏ nhất.
Gọi tên: 3-metylpent-2-en.
Chọn C.
Ví dụ 2: Cho các phát biểu sau:
(1) Anken là các hiđrocacbon mà phân tử có một liên kết đôi C=C.
(2) Những hiđrocacbon có công thức phân tử là anken.
(3) Anken là hiđrocacbon không no, mạch hở có công thức phân tử .
(4) Anken là hiđrocacbon mạch hở có chứa liên kết đôi C=C trong phân tử.
Số nhận xét đúng là
A. 1. B. 2.
C. 3. D. 4.
Hướng dẫn giải
Có 2 phát biểu đúng là (1) và (3).
(2) sai vì ngoài anken thì xicloankan cũng là hiđrocacbon có công thức phân tử
(4) sai vì trong phân tử anken chỉ có 1 liên kết đôi C=C
Chọn B.
Kiểu hỏi 2: Đồng phân anken
Phương pháp giải
Khi viết đồng phân của anken, các bước làm tương tự ankan.
Chú ý:
Anken có 2 loại đồng phân cấu tạo: đồng phân mạch C và đồng phân về vị trí liên kết đôi.
Anken có đồng phân hình học: cis- và trans-
Điều kiện để có đồng phân hình học:
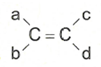
Viết đồng phân của anken:
Viết mạch dài nhất, di chuyển vị trí liên kết đôi.
Giảm mạch C, di chuyển vị trí liên kết đôi, vị trí nhánh.
Lưu ý loại đồng phân đề bài yêu cầu.
+ Nếu đề bài yêu cầu đồng phân cấu tạo: chỉ có đồng phân mạch C và đồng phân vị trí liên kết đôi.
+ Nếu đề bài yêu cầu đồng phân anken nói chung: phải tính thêm cả đồng phân hình học (cis-, trans-).
Ví dụ: Số đồng phân anken có công thức phân tử C5H10 là
A. 4. B. 5.
C. 6. D. 7.
Hướng dẫn giải
Có 6 đồng phân thỏa mãn là:
(cis-, trans-)
Chọn C.
Ví dụ mẫu
Ví dụ 1: Hợp chất C5H10 mạch hở có số đồng phân cấu tạo là
A. 4. B. 5.
C. 6. D. 10.
Hướng dẫn giải
Đồng phân cấu tạo gồm đồng phân mạch cacbon và đồng phân vị trí liên kết đôi.
C5H10 có 5 đồng phân cấu tạo mạch hở là:
Chọn B.
Ví dụ 2: Cho các anken có công thức: (I); (II); (III); (IV); (V). Những anken có đồng phân hình học là:
A. (I), (IV), (V). B. (II), (IV), (V).
C. (III), (IV). D. (II), (III), (IV), (V).
Hướng dẫn giải
Cho anken có công thức:
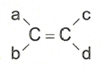
Điều kiện để có đồng phân hình học:
Có 3 anken thỏa mãn điều kiện có đồng phân hình học là (II), (IV), (V).
Chọn B.
Kiểu hỏi 3: Tính chất hóa học của anken.
Ví dụ mẫu
Ví dụ 1: Khi cho but-1-en tác dụng với dung dịch HBr, theo quy tắc Mac-côp-nhi-côp thì sản phẩm chính thu được là
A.
B.
C.
D.
Hướng dẫn giải
Quy tắc cộng Mac-côp-nhi-côp định hướng sản phẩm chính: Nguyên tử H gắn vào C có nhiều H hơn.
Phương trình hóa học:
Chọn B.
Ví dụ 2: Số đồng phân cấu tạo anken ở thể khí (đktc) mà khi cho mỗi anken đó tác dụng với dung dịch HCl chỉ cho một sản phẩm hữu cơ duy nhất là
A. 2. B. 1.
C. 3. D. 4.
Hướng dẫn giải
Các anken ở thể khí có số cacbon không vượt quá 4. Có 5 anken thỏa mãn là:
(*)
(**)
Anken cộng HCl cho một sản phẩm hữu cơ duy nhất: anken có cấu tạo đối xứng.
Có 2 công thức thỏa mãn là: (*) và (**).
Chọn A.
Kiểu hỏi 4: Nhận biết anken
Ví dụ mẫu
Ví dụ 1: Nêu phương pháp hóa học phân biệt hai khí metan và etilen.
Hướng dẫn giải
Dẫn lần lượt hai khí vào hai ống nghiệm chứa dung dịch brom:
Khí nào làm mất màu dung dịch brom, đó là khí etilen:
nâu đỏ không màu
Khí không làm mất màu dung dịch brom là metan.
Kiểu hỏi 5: Điều chế, ứng dụng của anken
Ví dụ mẫu
Ví dụ 1: Cho hình vẽ mô tả thí nghiệm điều chế khí Y từ dung dịch X:
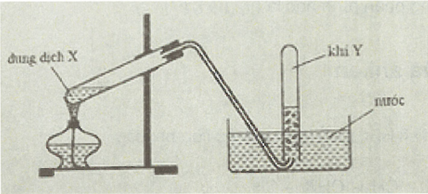
Hình vẽ trên minh họa cho phản ứng:
A.
B.
C.
D.
Hướng dẫn giải
Khí Y được thu bằng phương pháp dời chỗ của nước, nên khí Y không tan trong nước Loại đáp án A, B (NH3 và HCl tan tốt trong nước).
Khí Y được điều chế từ dung dịch X Loại đáp án D.
Chọn C.
Ví dụ 2: Kể tên 3 ứng dụng thường gặp của etilen trong đời sống sản xuất.
Hướng dẫn giải
Ứng dụng trong đời sống hay gặp của etilen là:
Là nguyên liệu để tổng hợp nhựa polietilen.
Là nguyên liệu để sản xuất ancol etylic.
Dùng etilen để kích thích quả mau chín.
III. Bài tập tự luyện dạng 1
Bài tập cơ bản
Câu 1: Anken là
A. những hiđrocacbon có 1 liên kết đôi trong phân tử là anken.
B. những hiđrocacbon mạch hở có 1 liên kết đôi trong phân tử anken.
C. những hiđrocacbon có liên kết ba trong phân tử.
D. những hiđrocacbon mạch hở có liên kết ba trong phân tử.
Câu 2: Anken X có đặc điểm: Trong phân tử có 11 liên kết xích ma . Công thức phân tử của X là
A. C3H6. B. C4H8
C. C6H12. D. C5H10.
Câu 3: Hợp chất có đồng phân hình học là
A. 2-metylbut-2-en. B. 2-clobut-1-en.
C. 2,3-điclobut-2-en. D. 2,3-đimetylpent-2-en.
Câu 4: Cho các chất sau:
(1) 2-metylbut-1-en; (2) 3,3-đimetylbut-1-en;
(3) 3-metylpent-1-en; (4) 3-metylpent-2-en.
Những chất là đồng phân của nhau là
A. (3) và (4). B. (1), (2) và (3).
C. (1) và (2). D. (2), (3) và (4).
Câu 5: Hợp chất 2,4-đimetylhex-1-en ứng với công thức cấu tạo là
A. B.
C. D.
Câu 6: Cho 3,3-đimetylbut-1-en tác dụng với HBr. Sản phẩm chính của phản ứng là
A. 2-brom-3,3-đimetylbutan.
B. 2-brom-2,3-đimetylbutan.
C. 2,2-đimetylbutan.
D. 3-brom-2,2-đimetylbutan.
Câu 7: Hyđrat hóa hai anken chỉ tạo thành hai ancol. Hai anken đó là
A. 2-metylpropen và but-1-en.
B. propen và but-2-en.
C. eten và but-2-en.
D. eten và but-1-en.
Câu 8: Cho etilen tác dụng với dung dịch H2SO4 loãng, nóng, sản phẩm chính thu được là
A. CH3CH2OH. B. CH3CH2SO4H.
C. CH3CH2SO3H. D.
Câu 9: Trùng hợp eten, sản phẩm thu được có cấu tạo là
A. . B.
C. D.
Câu 10: Oxi hóa etilen bằng dung dịch KMnO4 thu được sản phẩm là:
A. MnO2, C2H4(OH)2, KOH. B. K2CO3, H2O, MnO2.
C. C2H5OH, MnO2, KOH. D. C2H4(OH)2, K2CO3, MnO2.
Câu 11: Chất nào sau đây được dùng làm nguyên liệu tổng hợp nên nhựa PP?
A. etilen. B. Propan.
C. Propen. D. butan.
Bài tập nâng cao
Câu 12: Khi điều chế etilen trong phòng thí nghiệm từ C2H5OH, (H2SO4 đặc, ) thường lẫn một số tạp chất. Để làm sạch etilen, cần sục hỗn hợp sản phẩm qua bình đựng dung dịch nào dưới đây?
A. dung dịch brom dư. B. dung dịch NaOH dư.
C. dung dịch Na2CO3 dư. D. dung dịch KMnO4 loãng dư.
Câu 13: Để phân biệt etan và eten, người ta dùng phản ứng nào là thuận tiện nhất?
A. Phản ứng đốt cháy. B. Phản ứng cộng với hiđro.
C. Phản ứng cộng với nước brom. D. Phản ứng trùng hợp.
Câu 14: Có bao nhiêu đồng phân anken là chất khí ở điều kiện thường?
A. 2. B. 3.
C. 5. D. 6.
Dạng 2: Phản ứng cộng của anken
Bài toán 1: Anken tác dụng với HX, X2 (X là Cl, Br, I)
![]() Phương pháp giải
Phương pháp giải
Phương trình hóa học:
Theo phương trình:
Nếu Hiđrocacbon mạch hở là anken
Nhận xét:
Ví dụ: 0,05 mol hiđrocacbon mạch hở X làm mất màu vừa đủ dung dịch chứa 8 gam brom cho ra sản phẩm có hàm lượng brom đạt 69,56%. Công thức phân tử của X là
A. C3H6. B. C4H8.
C. C5H10. D. C5H8.
Hướng dẫn giải
Xét tỉ lệ:
là anken:
Phương trình hóa học:
Ta có:
n = 5
Vậy công thức của X là
Chọn C.
Ví dụ mẫu
Ví dụ 1: Cho hiđrocacbon mạch hở X phản ứng với brom (dung dịch) theo tỉ lệ mol 1 : 1, thu được chất hữu cơ Y (chứa 74,08% Br về khối lượng). Khi X phản ứng với HBr thì thu được hai sản phẩm hữu cơ khác nhau. Tên gọi của X là
A. but-1-en. B. but-2-en.
C. propilen. D. butan.
Hướng dẫn giải
X phản ứng với Br2 theo tỉ lệ mol 1 : 1 nên X là anken, có công thức .
Phương trình hóa học:
Ta có:
Công thức của X là C4H8
Khi X phản ứng với HBr thì thu được hai sản phẩm hữu cơ khác nhau nên X là but-1-en.
Chọn A.
Ví dụ 2. Dẫn 3,36 lít (đktc) hỗn hợp X gồm hai anken là đồng đẳng kế tiếp vào bình nước brom dư, thấy khối lượng bình tăng thêm 7,7 gam.
a) Xác định công thức phân tử của hai anken.
b) Tính thành phần phần trăm về thể tích của hai anken.
Hướng dẫn giải
a) Ta có:
Khối lượng bình brom tăng chính là khối lượng của anken nên
Gọi công thức phân tử chung của hai anken trong X là
Ta có:
Vì hai anken là đồng đẳng kế tiếp Công thức phân tử của hai anken là C3H6 và C4H8.
b) Áp dụng sơ đồ đường chéo cho số nguyên tử C trung bình của hỗn hợp C3H6 và C4H8 ta có:
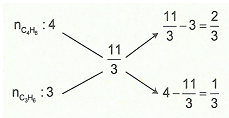
Các khí đo ở cùng điều kiện nên tỉ lệ về thể tích chính là tỉ lệ về số mol.
Thành phần phần trăm về thể tích của hai anken là:
Bài toán 2: Anken tác dụng với H2
Phương pháp giải
Phương trình hóa học:
Theo phương trình:
Nhận xét:
Bảo toàn khối lượng:
Chú ý: Sau phản ứng cộng hiđro vào anken mà thì trong hỗn hợp sau phản ứng có H2 dư.
Ví dụ: Cho H2 và một anken có thể tích bằng nhau qua niken đun nóng ta được hỗn hợp A. Biết tỉ khối hơi của A đối với H2 là 23,2. Hiệu suất phản ứng hiđro hóa là 75%. Công thức phân tử của anken là
A. C2H4. B. C3H6.
C. C4H8. D. C5H10.
Hướng dẫn giải
Ta chọn
Phương trình hóa học:
Ta có:
Vì nên
Bảo toàn khối lượng:
Vậy công thức của anken là C4H8.
Chọn C.
Ví dụ mẫu
Ví dụ 1: Cho hỗn hợp X gồm anken và hiđro có tỉ khối so với heli bằng 3,33. Cho X đi qua bột niken nung nóng đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp Y có tỉ khối so với heli là 4. Công thức phân tử của X là
A. C2H4. B. C3H8.
C. C4H8. D. C5H10.
Hướng dẫn giải
Gọi công thức của anken là .
Nhận thấy:
Sau phản ứng H2 còn dư, C2H2n đã phản ứng hết.
Bảo toàn khối lượng:
Chọn .
Ta có:
Lại có:
Công thức của anken là .
Chọn D.
Ví dụ 2. Hỗn hợp khí X gồm H2 và C2H4 có tỉ khối so với He là 3,75. Dẫn X qua Ni nung nóng, thu được hỗn hợp khí Y có tỉ khối so với He là 5. Hiệu suất của phản ứng hiđro hóa là
A. 20%. B. 40%.
C. 50%. D. 25%.
Hướng dẫn giải
Ta có: Sơ đồ đường chéo:
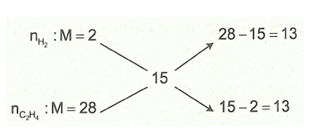
Có thể tính hiệu suất phản ứng theo H2 hoặc theo C2H4.
Bảo toàn khối lượng:
Chọn
Trong X ban đầu có
Lại có:
Chọn C.
IV. Bài tập tự luyện dạng 2
Bài tập cơ bản
Câu 1: Cho 2,24 lít anken lội qua bình đựng dung dịch brom thì thấy khối lượng bình tăng 4,2 gam. Anken có công thức phân tử là
A. C2H4. B. C3H6.
C. C4H8. D. C4H10.
Câu 2: Một anken X cộng hợp với dung dịch Br2 tạo sản phẩm có thành phần khối lượng brom là 85,11%. Công thức phân tử của X là
A. C3H6. B. C2H4.
C. C5H10. D. C4H8.
Câu 3: Cho 3,36 lít hỗn hợp etan và etilen (đktc) đi chậm qua dung dịch brom dư. Sau phản ứng khối lượng bình brom tăng thêm 2,8 gam. Số mol etan và etilen trong hỗn hợp lần lượt là
A. 0,05 và 0,10. B. 0,10 và 0,05.
C. 0,12 và 0,03. D. 0,03 và 0,12.
Câu 4: Cho 2,8 gam anken A làm mất màu vừa đủ dung dịch chứa 8 gam Br2. Hiđrat hóa A chỉ thu được một ancol duy nhất. A có tên là
A. but-1-en. B. but-2-en.
C. hex-2-en. D. 2,3-đimetylbut-2-en.
Câu 5: Hỗn hợp X gồm H2 và C2H4 có tỉ khối so với H2 là 7,5. Dẫn X qua Ni nung nóng thu được hỗn hợp khí Y có tỉ khối so với H2 là 12,5. Hiệu suất của phản ứng hiđro hóa là
A. 70%. B. 60%.
C. 50%. D. 80%.
Câu 6: Hỗn hợp X gồm etilen và hiđro có tỉ khối so với H2 là 4,25. Dẫn X qua bột Ni nung nóng thu được hỗn hợp Y (thể tích các khí đo ở cùng điều kiện). Tỉ khối hơi của Y so với H2 là
A. 5,23. B. 10,4.
C. 4,25. D. 5,75.
Câu 7: Hỗn hợp X gồm H2, C2H4 và C3H6 có tỉ khối so với H2 là 9,25. Cho 22,4 lít X (đktc) vào bình kín có sẵn một ít bộ Ni. Đun nóng bình một thời gian, thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 10. Tổng số mol H2 đã phản ứng là
A. 0,070 mol. B. 0,015 mol.
C. 0,075 mol. D. 0,050 mol.
Bài tập nâng cao
Câu 8: Dẫn hỗn hợp X gồm CnH2n và H2 (số mol bằng nhau) qua Ni, thu được hỗn hợp Y. Tỉ khối hơi của Y so với X là 1,6. Hiệu suất của phản ứng là
A. 40%. B. 60%.
C. 65%. D. 75%.
Câu 9: Hỗn hợp X gồm anken Y và H2. Tỉ khối hơi của X so với H2 là 7,67. Dẫn X qua Ni nung nóng đến phản ứng hoàn toàn thu được hỗn hợp Z có tỉ khối so với H2 là 11,50. Anken Y là
A. C2H4. B. C3H6.
C. C4H8. D. C5H10.
Câu 10: Một hỗn hợp X gồm ankan A và anken B, A có nhiều hơn B một nguyên tử cacbon, A và B đều ở thể khí (ở đktc). Khi cho 6,72 lít khí X (đktc) đi qua nước brom dư, khối lượng bình brom tăng lên 2,8 gam; thể tích khí còn lại chỉ bằng 2/3 thể tích hỗn hợp X ban đầu. Công thức phân tử của A, B và khối lượng của hỗn hợp X là
A. C4H10, C3H6 và 5,8 gam.
B. C3H8, C2H4 và 5,8 gam.
C. C4H10, C3H8 và 12,8 gam.
D. C3H8, C2H4 và 11,6 gam.
Dạng 3: Phản ứng oxi hóa anken
Bài toán 1: Phản ứng oxi hóa hoàn toàn
Phương pháp giải
Phương trình hóa học:
Theo phương trình:
Đốt hiđrocacbon mạch hở có thì hiđrocacbon đó là anken.
Chú ý: Bài toán hỗn hợp có thể sử dụng phương pháp trung bình để tìm ra số nguyên tử cacbon trung bình. Bảo toàn khối lượng:
Bảo toàn nguyên tố O:
Ví dụ: Đốt cháy hoàn toàn 8,96 lít (đktc) hỗn hợp hai anken là đồng đẳng liên tiếp thu được m gam H2O và (m + 39) gam CO2. Công thức phân tử của hai anken là
A. C2H4 và C3H6. B. C4H8 và C5H10.
C. C3H6 và C4H8. D. C6H12 và C5H10.
Hướng dẫn giải
Ta có:
Gọi công thức phân tử của hai anken là .
Phương trình hóa học:
mol
Ta có:
Hai anken là C3H6 và C4H8.
Chọn C.
![]() Ví dụ mẫu
Ví dụ mẫu
Ví dụ 1: Đốt cháy hoàn toàn a gam hỗn hợp eten, propen, but-2-en cần dùng vừa đủ b lít oxi (ở đktc) thu được 2,4 mol CO2 và 2,4 mol nước. Giá trị của b là
A. 92,40. B. 94,20. C. 80,64. D. 24,90.
Hướng dẫn giải
Gọi công thức phân tử của ba anken là
Phương trình hóa học:
Bảo toàn nguyên tố O:
lít
Chọn C.
Ví dụ 2: Đốt cháy hoàn toàn 0,1 mol hỗn hợp gồm CH4, C4H10 và C2H4 thu được 0,14 mol CO2 và 0,23 mol H2O. Số mol của ankan và anken trong hỗn hợp lần lượt là
A. 0,09 mol và 0,01 mol. B. 0,01 mol và 0,09 mol.
C. 0,08 mol và 0,02 mol. D. 0,02 mol và 0,08 mol.
Hướng dẫn giải
Khi đốt ankan: và
Khi đốt anken:
Chọn A.
Bài toán 2: Phản ứng oxi hóa không hoàn toàn
![]() Ví dụ mẫu
Ví dụ mẫu
Ví dụ 1: Để khử hoàn toàn 200 ml dung dịch KMnO4 0,2M tạo thành chất rắn màu nâu đen cần V lít khí C2H4 (ở đktc). Giá trị tối thiểu của V là
A. 2,240. B. 2,688. C. 4,480. D. 1,344.
Hướng dẫn giải
Ta có:
Số mol C2H4 tối thiểu là số mol C2H4 phản ứng vừa đủ với KMnO4.
Phương trình hóa học:
mol
lít
Chọn D.
![]() Bài tập tự luyện dạng 3
Bài tập tự luyện dạng 3
Bài tập cơ bản
Câu 1: Thổi 0,25 mol khí etilen qua 125 ml dung dịch KMnO4 1M trong môi trường trung tính (hiệu suất 100%), khối lượng etilen glicol thu được là
A. 11,625 gam. B. 23,250 gam. C. 15,500 gam. D. 31,000 gam.
Câu 2: Dẫn 3,36 lít hỗn hợp khí etilen và khí propilen (đktc) đi qua dung dịch KMnO4 dư. Sau phản ứng xảy ra hoàn toàn thấy xuất hiện m gam chất rắn màu nâu đen. Giá trị của m là
A. 6,525. B. 13,050. C. 8,700. D. 17,400.
Câu 3: Đốt cháy hoàn toàn 0,05 mol một anken A thu được 4,48 lít CO2 (đktc). Cho A tác dụng với dung dịch HBr chỉ cho một sản phẩm duy nhất. Công thức cấu tạo của A là
A. B. C. D.
Câu 4: Đốt cháy hoàn toàn V lít (đktc) hỗn hợp X gồm CH4, C2H4 thu được 0,15 mol CO2 và 0,2 mol H2O. Giá trị của V là
A. 2,24. B. 3,36. C. 4.48. D. 1.68.
Câu 5: Đem đốt cháy hoàn toàn 0,1 mol hỗn hợp X gồm hai anken là đồng đẳng kế tiếp nhau thu được CO2 và nước có khối lượng hơn kém nhau 6,76 gam. Công thức phân tử của hai anken là
A. C2H4 và C3H6. B. C3H6 và C4H8. C. C4H8 và C5H10. D. C5H10 và C6H12.
Câu 6: X là hỗn hợp C4H8 và O2 (tỉ lệ mol tương ứng 1 : 10). Đốt cháy hoàn toàn X được hỗn hợp Y. Dẫn Y qua bình H2SO4 đặc, dư được hỗn hợp Z. Tỉ khối của Z so với hiđro là
A. 18. B. 19. C. 20. D. 21.
Câu 7: Hỗn hợp X gồm C3H8 và C3H6 có tỉ khối so với hiđro là 21,8. Đốt cháy hết 5,6 lít X (đktc) thì thu được khối lượng CO2 và H2O lần lượt là
A. 33,0 gam và 17,1 gam. B. 22 gam và 9,9 gam.
C. 13,2 gam và 7,2 gam. D. 33 gam và 21,6 gam.
Bài tập nâng cao
Câu 8: Cho 0,2 mol hỗn hợp X gồm etan, propan và propen qua dung dịch brom dư, thấy khối lượng bình brom tăng 4,2 gam. Lượng khí còn lại đem đốt cháy hoàn toàn thu được 6,48 gam nước. Phần trăm thể tích etan, propan và propen lần lượt là:
A. 30%, 20%, 50%. B. 20%, 50%, 30%.
C. 50%, 20%, 30%. D. 20%, 30%, 50%.
Câu 9: Đốt cháy hoàn toàn 0,1 mol anken X thu được CO2 và hơi nước. Hấp thụ hoàn toàn sản phẩm bằng 100 gam dung dịch NaOH 21,62% thu được dung dịch mới trong đó nồng độ của NaOH chỉ còn 5%. Công thức phân tử của X là
A. C2H4. B. C3H6. C. C4H8. D. C5H10.
Đáp án và lời giải
Dạng 1: Lí thuyết liên quan đến đồng phân, danh pháp, tính chất của anken, điều chế ứng dụng của anken
|
1 – B |
2 – B |
3 – C |
4 – D |
5 – B |
6 – A |
7 – C |
8 – A |
9 – B |
10 – A |
|
11 – C |
12 – B |
13 – C |
14 – D |
|
|
|
|
|
|
Câu 12:
Do H2SO4 đặc có tính háo nước và tính oxi hóa mạnh, nên có thể tạo ra các sản phẩm phụ như CO2, SO2 lẫn với etilen.
Để làm sạch etilen cần dẫn sản phẩm qua dung dịch kiềm để hấp thụ hết CO2, SO2
Câu 13:
Eten có tham gia phản ứng cộng và trùng hợp khác với metan.
Điều kiện để thực hiện phản ứng cộng H2 và trùng hợp phức tạp và hiện tượng không rõ.
Eten có khả năng làm mất màu dung dịch brom ngay ở điều kiện thường.
Câu 14: Từ C2 đến C4: anken là chất khí ở điều kiện thường.
C2H4: 1 đồng phân.
C3H6: 1 đồng phân.
C4H8: 4 đồng phân ( (cis,trans); ).
Vậy có tất cả 6 đồng phân.
Dạng 2: Phản ứng cộng của anken
|
1 – B |
2 – B |
3 – A |
4 – B |
5 – D |
6 – A |
7 – C |
8 – D |
9 – B |
10 – D |
Câu 7:
Bảo toàn khối lượng:
Câu 8: Giả sử
Hiệu suất tính theo anken hay H2 đều được.
Bảo toàn khối lượng:
Câu 9. Gọi công thức của anken là
Nhận thấy:
Sau phản ứng H2 còn dư, CnH2n đã phản ứng hết.
Bảo toàn khối lượng:
Chọn
Ta có:
Vậy ban đầu, trong X có 0,5 mol CnH2n và 1 mol H2.
Công thức của anken là C3H6.
Câu 10: Ta có:
là C2H4 (0,1 mol); A là C3H8 (0,2 mol).
Dạng 3. Phản ứng oxi hóa anken
|
1 – A |
2 – C |
3 – D |
4 – A |
5 – A |
6 – B |
7 – A |
8 – D |
9 – A |
Câu 8. Gọi số mol C2H6, C3H8, C3
H6 trong hỗn hợp lần lượt là x, y, z mol.
Ta có hệ phương trình:
Phần trăm theo thể tích của mỗi chất là:
Câu 9:
Gọi công thức của anken là
mol
Dẫn sản phẩm cháy qua bình đựng dung dịch NaOH, vì NaOH dư nên ta có chỉ tạo muối trung hòa:
mol
Ta có:
Công thức phân tử của X là C2H4.