Tailieumoi.vn xin giới thiệu phương trình HOOC–CH(NH2)–CH2–CH2–COOH + HCl → HOOC–CH(NH3Cl)–CH2–CH2–COOH gồm điều kiện phản ứng, cách thực hiện, hiện tượng phản ứng và một số bài tập liên quan giúp các em củng cố toàn bộ kiến thức và rèn luyện kĩ năng làm bài tập về phương trình phản ứng hóa học. Mời các bạn đón xem:
Phương trình HOOC–CH(NH2)–CH2–CH2–COOH + HCl → HOOC–CH(NH3Cl)–CH2–CH2–COOH
1. Phản ứng hóa học:
HOOC–CH(NH2)–CH2–CH2–COOH + HCl → HOOC–CH(NH3Cl)–CH2–CH2–COOH
2. Điều kiện phản ứng
- Phản ứng xảy ra ở điều kiện thường.
3. Cách thực hiện phản ứng
- Nhỏ từ từ axit glutamic 10% vào ống nghiệm chứa 1 ml HCl 10%
4. Hiện tượng nhận biết phản ứng
- Quan sát sự chuyển màu của chỉ thị phù hợp trước và sau phản ứng.
5. Tính chất hóa học
5.1. Tính chất hóa học của Axit Glutamic
a. Tác dụng với dung dịch bazơ (do có nhóm COOH):
Axit glutamic có tính axit nên nó làm đổi màu qùy tím
b. Tác dụng với dung dịch axit (do có nhóm NH2):
- Tác dụng với dung dịch bazơ (do có nhóm COOH)
HOOC–CH(NH2)–CH2–CH2–COOH + 2NaOH → NaOOC–CH(NH2)–CH2–CH2–COONa + 2H2O
- Tác dụng với dung dịch axit (do có nhóm NH2)
HOOC–CH(NH2)–CH2–CH2–COOH + HCl → HOOC–CH(NH3Cl)–CH2–CH2–COOH
c. Phản ứng este hóa nhóm COOH :
Tương tự axit cacboxylic, axit gultamic phản ứng được với ancol cho ra este
H2N–C3H5–(COOH)2 + 2C2H5OH 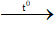
5.2. Tính chất hóa học của HCl
- Axit HCl làm đổi màu quỳ tím: Khi nhúng quỳ tím vào dung dịch axit sẽ có hiện tượng quỳ tím chuyển đỏ.
- Axit clohidric tác dụng với kim loại đứng trước H, tạo thành muối và hidro
Fe + 2HCl → FeCl2 + H2↑
- Axit clohidric tác dụng với oxit kim loại, tạo thành muối Clorua và nước
6HCl + Al2O3 →2AlCl3 + 3H2O
- Axit clohidric tác dụng với Bazơ, tạo thành muối Clorua và nước
3HCl + Al(OH)3 → AlCl3 + 3H2O
- Axit clohidric tác dụng với muối, tạo thành muối mới và axit mới
AgNO3 + 2HCl → AgCl↓ + HNO3
- Axit clohidric tác dụng với hợp chất có tính oxi hoá, thể hiện tính khử
6HCl + KClO3 → KCl + 3Cl2↑ + 3H2O
Lưu ý: Axit HCl sẽ không tác dụng với những kim loại đứng sau H trong dãy điện hoá, không tác dụng với các phi kim, axit, oxit kim loại, oxit phi kim.
6. Bạn có biết
- Phản ứng trên cho thấy axit glutamic có chứa nhóm chức thể hiện tính bazo.
- Các amino axit khác cũng có phản ứng với NaOH tương tự axit glutamic.
7. Bài tập liên quan
Ví dụ 1: Dãy gồm các chất đều phản ứng với HCl là
A. axit glutamic, glyxin, natri clorua.
B. valin, amoni clorua, glyxin.
C. alanin, kali clorua,axit glutamic .
D. valin, glyxin, axit glutamic.
Hướng dẫn:
Valin, glyxin, axit glutamic đều phản ứng với HCl.
Đáp án: D
Ví dụ 2: Khối lượng axit glutamic cần dung để phản ứng vừa đủ với 0,1 mol HCl là
A. 11,7g. B. 14,7g.
C. 8,5g. D. 9,0g.
Hướng dẫn:
HOOC – CH(NH2) – CH2 – CH2 – COOH (0,1) + HCl → HOOC – CH(NH3Cl) – CH2 – CH2 – COOH (0,1 mol)
m = 0,1.147 = 14,7 gam.
Đáp án: B
Ví dụ 3: Cho 0,15 mol axit glutamic vào 175 ml dung dịch HCl 2M thu dung dịch X. Cho NaOH dư vào dung dịch X. Sau khi phản ứng xảy ra hoàn toàn, số mol NaOH cần dung là
A. 0,70 B. 0,50
C. 0,65 D. 0,55
Hướng dẫn:
Coi hỗn hợp phản ứng với NaOH gồm H2N-C3H5-(COOH)2 và HCl
HCl (0,35) + NaOH → NaCl (0,35 mol) + H2O
H2N- C3H5-(COOH)2 (0,15) + 2NaOH (0,3 mol) → H2N-C3H5-(COONa)2 + 2H2O
Số mol NaOH = 0,35 + 0,3 = 0,65 mol
Đáp án: C
8. Một số phương trình phản ứng hoá học khác của Amino Axit và hợp chất: