Tailieumoi.vn giới thiệu giải Chuyên đề học tập Hóa học lớp 12 Bài 2: Một số cơ chế phản ứng trong hoá học hữu cơ sách Cánh diều hay, chi tiết giúp học sinh xem và so sánh lời giải từ đó biết cách làm Chuyên đề Hóa 12. Mời các bạn đón xem:
Giải Chuyên đề Hóa 12 Bài 2: Một số cơ chế phản ứng trong hoá học hữu cơ
Lời giải:
- Phản ứng ứng cộng của HBr vào alkene không đối xứng tuân theo quy tắc Markovnikov vì phản ứng cộng HBr vào alkene không đối xứng xảy ra theo hướng tạo carbocation bền hơn.
- Phản ứng thế bromine vào hexane xảy ra theo cơ chế thế gốc (SR);
- Phản ứng nitro hoá benzene xảy ra theo cơ chế thế electrophile vào nhân thơm (SEAr);
- Phản ứng thuỷ phân dẫn xuất halogen xảy ra theo cơ chế thế nucleophile (SN1 hoặc SN2);
- Phản ứng cộng HCN vào hợp chất carbonyl xảy ra theo cơ chế cộng nucleophile vào C = O (AN).
II. Phản ứng thế gốc của alkane (SR)
Câu hỏi 1 trang 11 Chuyên đề Hóa học 12: Cho các tiểu phân sau:
.
Trong các tiểu phân trên, tiểu phân nào là tác nhân electrophile, tiểu phân nào là tác nhân nucleophile?
Lời giải:
- Tác nhân electrophile là các tiểu phân thiếu electron, có khả năng nhận electron, có ái lực với electron.
Vậy các tác nhân electrophile là: H+, Br+.
- Tác nhân nucleophile là các tiểu phân giàu electron, có khả năng nhường electron, có ái lực với hạt nhân.
Vậy các tác nhân nucleophile là: −OH, H2O, NH3, C2H5O−, C2H5OH, Br−.
Lời giải:
- Các gốc tự do có thể sinh ra từ propane khi phân cắt một liên kết C – H:
Trong đó gốc (2) bền hơn gốc (1).
- Lại có khi cho propane phản ứng với chlorine khi có ánh sáng sinh ra sản phẩm monohalogenoalkane ưu tiên theo hướng tạo ra gốc tự do trung gian bền hơn.
Khi cho propane phản ứng với chlorine khi có ánh sáng thì thu được sản phẩm chính là 2 – chloropropane.
III. Phản ứng cộng electrophile vào alkene (AE)
Lời giải:
Phản ứng giữa propene và bromine diễn ra theo cơ chế cộng electrophile.
CH2=CH-CH3 + Br2 → CH2Br – CHBr– CH3.
Cơ chế của phản ứng xảy ra như sau:
Lời giải:
Phản ứng cộng HBr vào propene xảy ra theo cơ chế cộng electrophile (AE).
Phương trình hoá học:
Giải thích sự tạo thành sản phẩm chính bằng cơ chế phản ứng như sau:
+ Giai đoạn đầu tiên là quá trình phản ứng của H+ (tác nhân electrophile) với C = C, tạo carbocation trung gian:
+ Giai đoạn thứ hai là quá trình kết hợp giữa carbocation với Br−.
Phản ứng cộng HBr vào propene (hay phản ứng cộng HX vào alkene bất đối xứng) ưu tiên xảy ra theo hướng tạo carbocation bền hơn. Do đó, sản phẩm chính của phản ứng là 2 – bromopropane.
Lời giải:
Phương trình hoá học của phản ứng cộng nước của propene (xúc tác H+):
Cơ chế phản ứng:
+ Bước 1: Quá trình proton hoá liên kết đôi C = C của propene tạo thành carbocation:
+ Bước 2: Quá trình nước cộng hợp vào carbocation:
+ Bước 3: Quá trình tách proton để tạo alcohol:
Phản ứng cộng nước vào propene (hay phản ứng cộng HX vào alkene bất đối xứng) ưu tiên xảy ra theo hướng tạo carbocation bền hơn. Do đó, sản phẩm chính của phản ứng là propan – 2 – ol (CH3-CH(OH)-CH3).
V. Phản ứng thế nucleophile (SN1 và SN2)
Lời giải:
Phản ứng thuỷ phân bromoethane trong dung dịch kiềm:
C2H5-Br + NaOH C2H5-OH + NaBr
Cơ chế của phản ứng như sau:
NaOH → Na+ + −OH
Lời giải:
- Phương trình hoá học của phản ứng thuỷ phân 2 – bromo – 2 – methylbutane trong dung dịch sodium hydroxide:
- Cơ chế của phản ứng: 2 – bromo – 2 – methylbutane là dẫn xuất halogen bậc ba, phản ứng xảy ra theo cơ chế SN1 là chủ yếu.
NaOH → Na+ + −OH
VI. Phản ứng cộng nucleophile vào C = O (AN)
Lời giải:
Phản ứng giữa acetone và HCN:
Cơ chế phản ứng:
Lời giải:
HCHO là hợp chất carbonyl nên có phản ứng với HCN.
Phương trình hoá học của phản ứng:
Phản ứng xảy ra theo cơ chế cộng nucleophile (AN) như sau:
Bài tập (trang 17)
Lời giải:
- Tác nhân electrophile là các tiểu phân thiếu electron, có khả năng nhận electron, có ái lực với electron.
Vậy tác nhân electrophile là: b)
- Tác nhân nucleophile là các tiểu phân giàu electron, có khả năng nhường electron, có ái lực với hạt nhân.
Vậy các tác nhân nucleophile là: a) CH3O− và c) (CH3)3N.
Lời giải:
Phương trình hoá học của phản ứng:
Cơ chế phản ứng giải thích quá trình tạo thành sản phẩm monobromohexane:
Phản ứng xảy ra theo cơ chế thế gốc SR, gồm các giai đoạn sau đây:
- Giai đoạn khơi mào:
- Giai đoạn phát triển mạch:
- Giai đoạn tắt mạch:
Bài tập 3 trang 17 Chuyên đề Hóa học 12: Cho các phản ứng sau:
(1) Propene phản ứng với H2O (có xúc tác acid).
(2) But – 2 – ene phản ứng với HBr.
a) Dùng công thức cấu tạo, viết phương trình hoá học của phản ứng xảy ra.
b) Hãy cho biết sản phẩm chính của phản ứng (1). Viết cơ chế để giải thích quá trình hình thành sản phẩm chính.
Lời giải:
a) Phương trình hoá học:
(1) Propene phản ứng với H2O (có xúc tác acid).
(2) But – 2 – ene phản ứng với HBr.
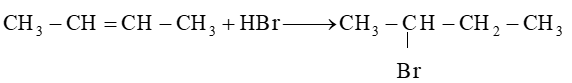
Cơ chế phản ứng:
+ Bước 1: Quá trình proton hoá liên kết đôi C = C của propene tạo thành carbocation:
+ Bước 2: Quá trình nước cộng hợp vào carbocation:
+ Bước 3: Quá trình tách proton để tạo alcohol:
Phản ứng cộng nước vào propene (hay phản ứng cộng HX vào alkene bất đối xứng) ưu tiên xảy ra theo hướng tạo carbocation bền hơn. Do đó, sản phẩm chính của phản ứng là propan – 2 – ol (CH3-CH(OH)-CH3).
Lời giải:
Phương trình hoá học của phản ứng:
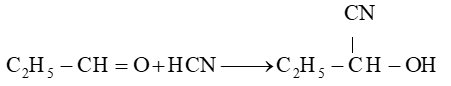
Xem thêm các bài giải Chuyên đề học tập Hóa học 12 Cánh diều hay, chi tiết khác: