Tailieumoi.vn giới thiệu Giải bài tập Vật Lí lớp 12 Bài 1: Sự chuyển thể của các chất chi tiết sách Cánh diều giúp học sinh xem và so sánh lời giải từ đó biết cách làm bài tập môn Vật lí 12. Mời các bạn đón xem:
Giải bài tập Vật Lí 12 Bài 1: Sự chuyển thể của các chất

Hình 1.1. Ba thể của nước: a) nước đá (thể rắn), b) nước (thể lỏng) và c) hơi nước (thể khí)
Lời giải:
Các chất rắn, chất lỏng và chất khí là các trạng thái của vật chất, được xác định bởi cấu trúc và sắp xếp của các phân tử, nguyên tử hoặc ion trong chất đó. Sự chuyển đổi giữa các trạng thái này thường liên quan đến việc thay đổi nhiệt độ và áp suất.
- Chất rắn:
+ Các phân tử, nguyên tử hoặc ion trong chất rắn được sắp xếp đều đặn và chặt chẽ, tạo thành một cấu trúc lưới cứng.
+ Đối với kim loại, cấu trúc này có thể là một lưới tinh thể.
- Chất lỏng:
+ Trong chất lỏng, cấu trúc của các phân tử, nguyên tử hoặc ion không còn đều đặn như trong chất rắn. Chúng có thể di chuyển nhẹ nhàng và tự tổ chức thành cấu trúc không gian không cố định.
- Chất khí:
+ Cấu trúc của chất khí không giữ các đặc điểm cụ thể về sự xếp đặt của các phân tử, nguyên tử hoặc ion. Chúng có thể tự do di chuyển và không giữ hình dạng hoặc kích thước cố định.
Câu hỏi 1 trang 7 Vật lí 12: Thanh sắt được tạo thành từ các phân tử chuyển động không ngừng nhưng tại sao lại không bị tan rã thành các hạt riêng biệt?
Lời giải:
Thanh sắt không được tạo thành từ các phân tử mà là từ các nguyên tử sắt. Trong kim loại, như thành sắt, nguyên tử không tồn tại dưới dạng phân tử như trong một số chất khác.
Cấu trúc của kim loại được mô tả bởi mô hình lưới kim loại, trong đó các nguyên tử sắt tạo thành một lưới không gian mà mỗi nguyên tử đều kết nối với những nguyên tử xung quanh thông qua liên kết kim loại. Liên kết này là kết quả của sự chia sẻ tự do của các electron dẫn năng (electron tự do) trong lưới kim loại.
Do cấu trúc này, thành sắt không tồn tại ở dạng phân tử riêng biệt và không bị tan rã thành các hạt riêng lẻ như trong các chất phân tử. Sự liên kết mạnh mẽ giữa các nguyên tử sắt trong lưới kim loại làm cho chúng giữ vững cấu trúc của mình. Nguyên tử sắt không tự do di chuyển và tự tạo thành các đơn vị riêng lẻ mà không cần đến sự liên kết phân tử như trong chất phân tử.
Lời giải:
Độ lớn của lực tương tác tăng từ chất khí đến chất lỏng và cao nhất trong chất rắn, do mức độ tự tổ chức và liên kết giữa các phân tử tăng lên.
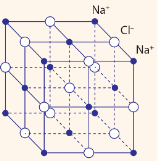
Lời giải:
Trong một tinh thể muối ăn như NaCl (muối bàn), các ion Na⁺ và Cl⁻ được sắp xếp theo một mô hình lưới tinh thể. Mỗi ion Na⁺ được bao quanh bởi các ion Cl⁻ và ngược lại. Cấu trúc này tạo ra một lưới tinh thể với các ion ở các vị trí cân bằng.
Trong môi trường tĩnh lặng, các ion trong tinh thể muối ăn không thể di chuyển tự do và dao động như các phân tử trong chất lỏng. Tuy nhiên, chúng thực sự có các dao động nhỏ do năng lượng nhiệt độ của môi trường xung quanh.
Cụ thể, các ion trong tinh thể muối ăn thực sự có một biên độ dao động rất nhỏ ở vị trí cân bằng của chúng. Các dao động này được gọi là dao động nhiệt động và liên quan đến năng lượng nhiệt độ của môi trường xung quanh.
Nếu nhiệt độ tăng lên, dao động nhiệt động cũng tăng, và nếu nhiệt độ giảm xuống, chúng giảm đi. Tuy nhiên, do tính chất của mạng lưới tinh thể và sự giữ chặt của lực tương tác giữa các ion, biên độ của các dao động này vẫn rất nhỏ, và các ion vẫn giữ ở vị trí cân bằng tương đối ổn định.
Lời giải:
Khi một chất chuyển từ thể rắn sang thể lỏng và từ thể lỏng sang thể khí, các phân tử của chất thường trải qua các thay đổi về cấu trúc và tương tác giữa chúng. Điều này có ảnh hưởng đến khoảng cách trung bình giữa các phân tử
- Thể rắn:
+ Các phân tử trong thể rắn thường sắp xếp cơ động hạn chế trong một cấu trúc tinh thể đều đặn.
+ Khoảng cách trung bình giữa các phân tử thường rất nhỏ do sự chặt chẽ của cấu trúc tinh thể.
- Thể lỏng:
+ Khi chất chuyển từ thể rắn sang thể lỏng, các liên kết giữa phân tử giảm, cho phép chúng di chuyển một cách tự do hơn.
+ Khoảng cách trung bình giữa các phân tử trong thể lỏng tăng lên so với thể rắn do sự di động và tự tổ chức giảm đi.
- Thể khí:
+ Trong thể khí, các phân tử di chuyển tự do và không giữ bất kỳ sự tự tổ chức cấu trúc nào.
+ Khoảng cách trung bình giữa các phân tử trong thể khí lớn hơn nhiều so với thể lỏng do sự tách rời và di động của chúng.
=> Khi chất chuyển từ thể rắn sang thể lỏng và từ thể lỏng sang thể khí, khoảng cách trung bình giữa các phân tử tăng lên do giảm sự tự tổ chức và tăng tính di động của chúng.
Câu hỏi 4 trang 9 Vật lí 12: Chất ở thể nào dễ bị nén nhất? Vì sao?
Lời giải:
Chất ở thể khí thường dễ bị nén nhất so với chất ở thể rắn và thể lỏng. Điều này có liên quan đến tính chất cấu trúc và tương tác giữa các phân tử, nguyên tử, hoặc ion trong từng thể. Quy luật Boyle cho thấy mối quan hệ giữa áp suất và thể tích của một khí: P1V1 = P2V2 (ở nhiệt độ không đổi). Khi áp suất tăng, thể tích của một khí có thể giảm đi và ngược lại. Điều này là do trong thể khí, có sự tách rời giữa các phân tử, cho phép chúng di chuyển dễ dàng và chất khí có khả năng thay đổi thể tích một cách linh hoạt khi áp suất thay đổi.
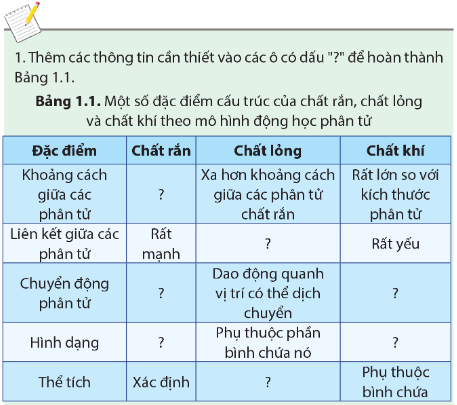
Lời giải:
|
Đặc điểm |
Chất rắn |
Chất lỏng |
Chất khí |
|
Khoảng cách giữa các phân tử |
Rất gần nhau |
Xa hơn khoảng cách giữa các phân tử chất rắn |
Rất lớn so với kích thước phân tử |
|
Liên kết giữa các phân tử |
Rất mạnh |
Nhỏ hơn trong chất rắn |
Rất yếu |
|
Chuyển động phân tử |
Dao động xung quanh vị trí cân bằng xác định |
Dao động quanh vị trí có thể dịch chuyển |
Chuyển động hỗn lợn, không ngừng về mọi phía |
|
Hình dạng |
Xác định |
Phụ thuộc phần bình chứa nó |
Phụ thuộc phần bình chứa nó |
|
Thể tích |
Xác định |
Xác định |
Phụ thuộc bình chứa |
Câu hỏi 5 trang 9 Vật lí 12: Biểu diễn bằng sơ đồ các quá trình chuyển đổi giữa ba thể: rắn, lỏng, khí.
Lời giải:
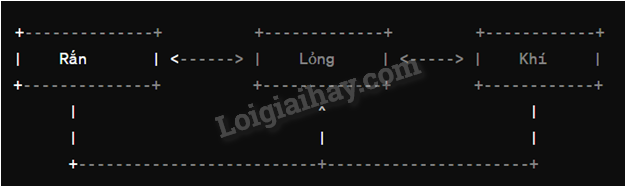
Lời giải:
Sự tăng mức nước biển do sự ấm lên toàn cầu chủ yếu xuất phát từ sự tan băng ở các vùng cực trên đất liền, chứ không phải do sự tan băng của băng nổi trên mặt nước.
Nước có một đặc điểm đặc biệt khi nhiệt độ giảm từ 4 °C đến nhiệt độ đông đặc 0 °C, thể tích của nước tăng lên thay vì giảm đi. Điều này là do cấu trúc phân tử đặc biệt của nước khi ở trong trạng thái lỏng gần điểm đông đặc. Khi nước ở dạng lỏng, cấu trúc phân tử tạo ra mạng lưới hydrogen liên kết, tạo nên một cấu trúc rỗng và giảm khả năng tự tự tổ chức của nước, làm tăng thể tích.
Vì vậy, khi nước ở nhiệt độ gần 0 °C, nó có thể trở nên có thể tăng thể tích và trở thành đặc điểm quan trọng trong việc giải thích sự tăng mực nước biển do sự tan băng ở các vùng cực. Khi băng trên đất liền tại các vùng cực tan ra, nước lỏng từ sự tan băng có thể làm tăng lên mức nước biển.
Tuy nhiên, sự tan băng của băng nổi trên mặt nước của các đại dương cũng đóng góp vào sự tăng mức nước biển, nhưng tỷ lệ này thường ít hơn so với sự tan băng của băng trên đất liền.
Lời giải:
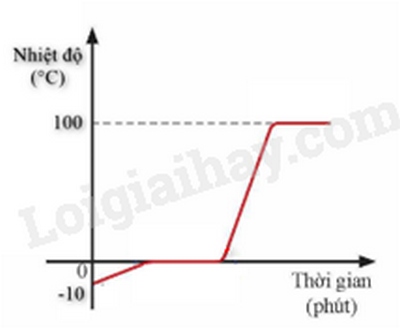
Lời giải:
Mở nắp bình nước sôi để nguội nhanh:
- Khi nước sôi và hóa thành hơi, nó sẽ mang theo một lượng lớn nhiệt độ năng lượng (enthalpy). Nếu nắp của bình nước đóng chặt, hơi nước sẽ bị giữ lại trong bình, và nó sẽ tiếp tục chứa đựng nhiệt độ năng lượng đó.
- Khi mở nắp, hơi nước có thể thoát ra, giúp chất lỏng nước nhanh chóng mất nhiệt và nguội. Việc thoát hơi nước giúp tăng cường quá trình nguội bằng cách loại bỏ nhiệt độ năng lượng khỏi hệ thống.
Lời giải:
Cảm giác lạnh khi xoa cồn vào da:
- Khi bạn xoa cồn lên da, cồn nhanh chóng bay hơi do có thể chuyển từ thể lỏng sang thể khí ở nhiệt độ phòng.
- Trong quá trình bay hơi, cồn cướp đi nhiệt độ từ cơ thể và da để chuyển đổi từ thể lỏng sang thể khí. Quá trình này tạo ra một cảm giác lạnh trên da.
- Ngoài ra, cần lưu ý rằng cồn có khả năng làm bay hơi nước từ da, làm mất đi nhiệt độ từ da, gây cảm giác lạnh và làm mát da.
Vận dụng trang 11 Vật lí 12: Giải thích sơ lược việc tách muối ra khỏi nước biển theo cách cổ truyền ở nước ta.
Lời giải:
Việc tách muối ra khỏi nước biển có thể được thực hiện theo cách cổ truyền thông qua một số phương pháp. Một trong những phương pháp cổ truyền phổ biến là sử dụng quá trình hòa tan muối trong nước biển và sau đó để muối tinh kết tinh từ dung dịch.
- Thu thập Nước Biển: Nước biển được thu thập từ biển hoặc đại dương.
- Hòa Tan Muối: Nước biển được đổ vào các bồn hoặc hồ chứa lớn để tạo thành dung dịch muối nước biển.
- Chưng Cất Nước: Dung dịch muối nước biển được đun nóng trong các bình chưng cất. Khi nước sôi, hơi nước bay lên và muối tinh kết lại ở dạng tinh thể ở trạng thái rắn.
- Thu Muối Tinh: Hơi nước bay lên được thu lại và ngưng tụ thành nước ngọt. Muối tinh kết lại trong bình chưng cất.
- Lọc và Rửa Muối: Muối tinh sau đó được lọc ra khỏi dung dịch và có thể được rửa sạch để loại bỏ các tạp chất khác.
- Thu Thập Muối: Muối tinh được thu thập và để khô trước khi được đóng gói và sử dụng.
Phương pháp này, tuy đã được thực hiện từ thời cổ đại, nhưng hiện nay, do sự tiện lợi và hiệu quả kinh tế, quá trình truyền thống này đã được thay thế bằng các phương pháp công nghiệp hiện đại như quá trình chưng cất nhiệt độ thấp, làm mát và sử dụng các loại lọc chất lượng cao để tách muối ra khỏi nước biển một cách hiệu quả và nhanh chóng.
Lời giải:
Mưa đá là hiện tượng khi các hạt đá có kích thước khác nhau rơi xuống từ đám mây. Quá trình hình thành mưa đá thường liên quan đến các sự chuyển thể của nước trong quá trình tạo ra tuyết và mưa
- Hình Thành Hạt Đá:
+ Ban đầu, nước trong đám mây có thể ở dạng hơi hoặc hạt nước siêu lạnh.
+ Khi có sự tăng lên của hạt bụi hoặc hạt đá nhỏ trong đám mây, nước có thể bắt đầu kết tinh xung quanh những hạt này, tạo thành những hạt đá nhỏ.
- Tăng Kích Thước của Hạt Đá:
+ Những hạt đá nhỏ có thể tiếp tục phát triển khi chúng va chạm và hấp thụ nước từ các giọt nước xung quanh hoặc từ hơi nước có sẵn trong đám mây.
- Rơi Xuống Đất:
+ Khi hạt đá đủ lớn, chúng không còn giữ được lên trên và rơi xuống đất dưới dạng mưa đá.
Quá trình này có thể thay đổi tùy thuộc vào điều kiện cụ thể của đám mây và môi trường xung quanh. Nếu nhiệt độ trong đám mây ở những tầng cao khá lạnh, hạt đá có thể duy trì kích thước lớn hơn khi chúng rơi xuống đất. Ngược lại, nếu có nhiều sự tan hơi và tái ngưng tụ, hạt đá có thể giữ kích thước nhỏ hơn.
Mưa đá thường xuất hiện trong cơn giông hoặc các loại đám mây phát triển dọc, nơi có sự chuyển động mạnh mẽ của không khí trong đám mây, tạo điều kiện cho sự hình thành và duy trì của hạt đá.
Lý thuyết Sự chuyển thể của các chất
I. Sơ lược cấu trúc của chất rắn, chất lỏng, chất khí
1. Mô hình động học phân tử
- Các chất được cấu tạo từ các hạt (phân tử, nguyên tử, ion)
- Các phân tử chuyển động không ngừng. Chuyển động của các phân tử được gọi là chuyển động nhiệt
- Các phân tử chuyển động càng nhanh thì nhiệt độ của vật do chúng tạo nên càng cao
- Giữa các phân tử có lực tương tác, bao gồm lực hút cà lực đẩy. Độ lớn của những lực này phụ thuộc vào khoảng cách giữa các phân tử
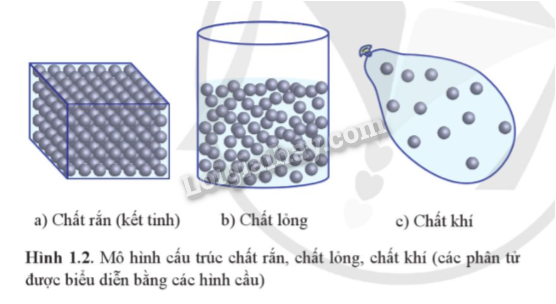
2. Sơ lược cấu tạo của các chất
|
Cấu trúc |
Thể rắn |
Thể lỏng |
Thể khí |
|
Khoảng cách giữa các phân tử |
Rất gần nhau (cỡ kích thước phân tử) |
Xa nhau |
Rất xa nhau (gấp hàng chục lần kích thước phân tử) |
|
Sự sắp xếp của các phân tử |
Trật tự |
Kém trật tự hơn |
Không có trật tự |
|
Chuyển động của các phân tử |
Chỉ dao động quanh vị trí cân bằng cố định |
Dao động quanh vị trí cân bằng luôn luôn thay đổi |
Chuyển động hỗn loạn |
II. Sự chuyển thể
1. Sự chuyển thể của chất
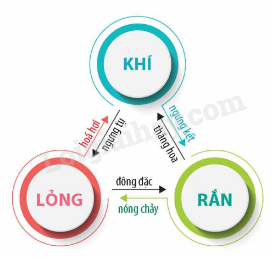
2. Giải thích sự nóng chảy
- Căn cứ vào cấu trúc sắp xếp của các hạt tạo nên chất rắn, người ta chia chất rắn thành hai loại: chất rắn kết tinh và chất rắn vô định hình
- Sự nóng chảy của chất rắn kết tinh
+ Khi nung nóng liên tục một vật rắn kết tinh nhiệt độ của vật tăng dần
+ Khi nhiệt độ đạt một giá trị xác định gọi là nhiệt độ nóng chảy thì vật bắt đầu chuyển sang thể lỏng và trong suốt quá trình này nhiệt độ của vật là không đổi
+ Khi toàn bộ chất rắn đã chuyển sang thể lỏng, tiếp tục cung cấp nhiệt lượng thì nhiệt độ của vật sẽ tiếp tục tăng
- Sự nóng chảy của chất rắn vô định hình
+ Khi nung nóng liên tục vật rắn vô định hình, vật rắn mềm đi và chuyển sang thể lỏng một cách liên tục, trong quá trình này nhiệt độ của vật tăng liên tục
+ Vật rắn vô định hình không có nhiệt độ nóng chảy xác định
→ Khi đun nóng đến một nhiệt độ nào đó, vật rắn bắt đầu chuyển trạng thái từ rắn sang lỏng (sự nóng chảy). Chất rắn kết tinh có nhiệt độ nóng chảy xác định (ở một áp suất cụ thể). Chất rắn vô định hình không có nhiệt độ nóng chảy xác định
3. Giải thích sự hóa hơi
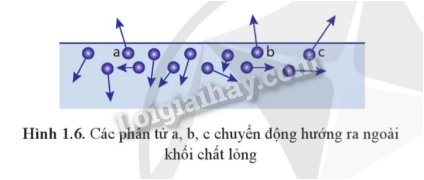
Khi các phân tử chất lỏng nhận được năng lượng, chúng sẽ chuyển động nhanh hơn làm nhiệt độ chất lỏng tăng dần. Một số phân tử chất lỏng ở gần bề mặt khối chất lỏng chuyển động hướng ra ngoài (Hình 1.6). Một số trong những phân ửt này có động năng đủ lớn, thắng được lực tương tác giữa các phân ửt thì có thể thoát ra ngoài khối chất lỏng. Ta nói chất lỏng bay hơi. Như vậy, có thể nói sự bay hơi là sự hóa hơi xảy ra ở mặt thoáng của khối chất lỏng.
Đồng thời, ở gần bề mặt khối chất lỏng, một số phân tử hơi chuyển động hỗn loạn va chạm vào chất lỏng và bị các phân tử chất lỏng hút vào khối chất lỏng. Ta gọi đó là sự ngưng ụt.
Nếu tiếp tục được cung cấp năng lượng, số phân tử chất lỏng nhận được năng lượng để bứt ra khỏi khối chất lỏng tăng dần, lớn gấp nhiều lần so với số phân tử khí (hơi) ngưng ụt. Khi đó, chất lỏng hóa hơi, chuyển dần thành chất khí. Trong quá trình đó, nhiệt độ chất lỏng tăng dần và nếu nhận đủ nhiệt lượng, chất lỏng sẽ sôi.
Ở áp suất tiêu chuẩn 1( atm), mỗi chất lỏng sôi ở một nhiệt độ xác định, nhiệt độ đó được gọi là nhiệt độ sôi của chất. Khi chất lỏng sôi, sự hóa hơi của chất lỏng xảy ra ở cả trong lòng và bề mặt chất lỏng.
Nhiệt độ nóng chảy và nhiệt độ sôi của một số chất được cho ở Bảng 1.2.
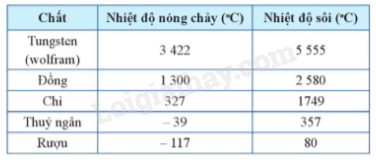
Trong quá trình hóa hơi, dù được cung cấp năng lượng liên tục nhưng khi đạt đến nhiệt độ sôi thì chất lỏng không tăng nhiệt độ suốt thời gian chuyển hoàn toàn thành chất khí. Lúc này, các phân tử nhận thêm năng lượng dùng để phá vỡ liên kết với các phân tử xung quanh, khiến phân tử chuyển động tự do. Chất lỏng chuyển thành chất khí.
Phần năng lượng nhận thêm để phá vỡ liên kết giữa các phân tử mà không làm tăng nhiệt độ của chất trong quá trình hóa hơi được gọi là ẩn nhiệt hóa hơi.
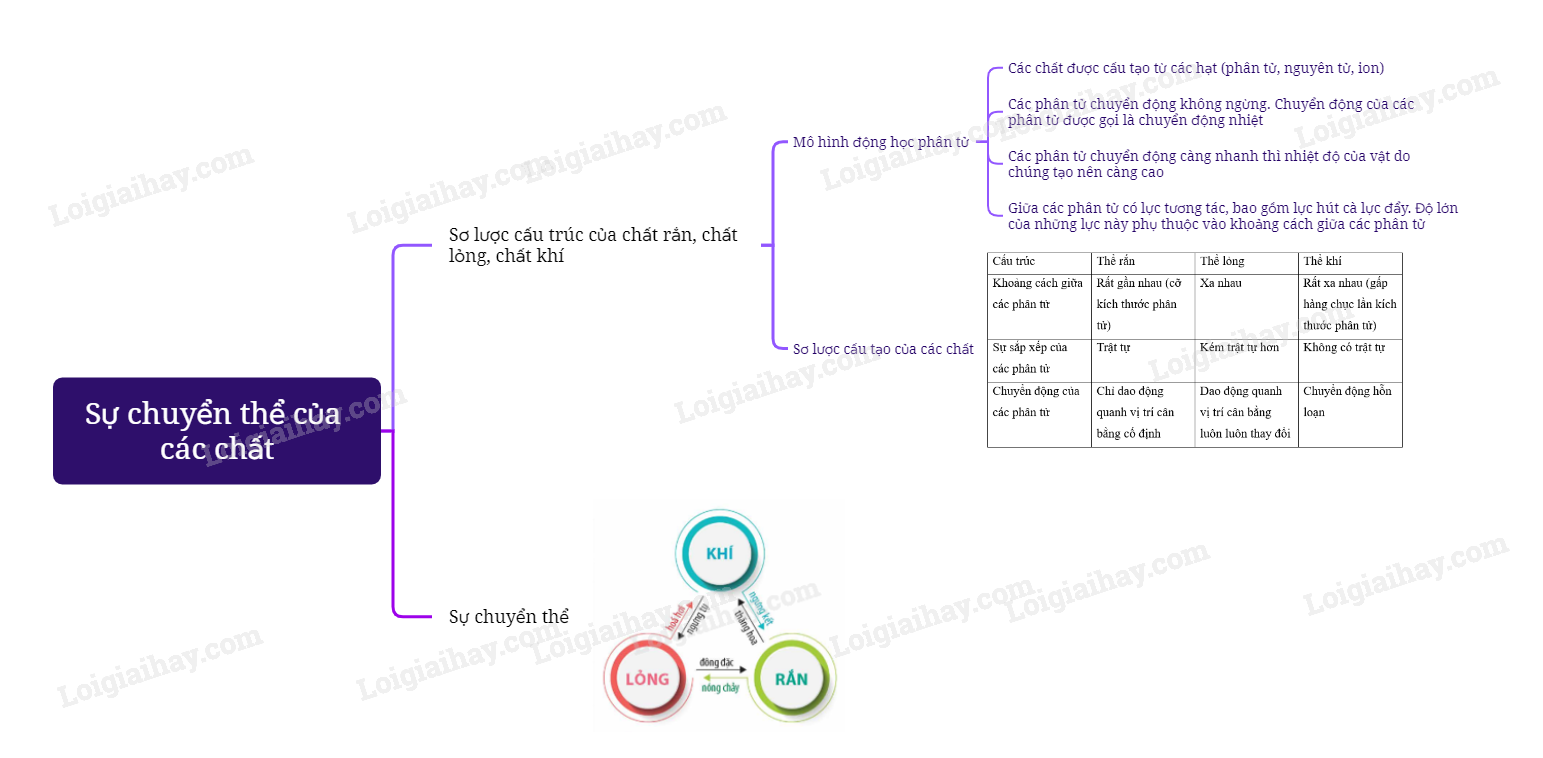
Sơ đồ tư duy Sự chuyển thể của các chất
Xem thêm các bài giải bài tập Vật Lí lớp 12 Cánh diều hay, chi tiết khác:
2. Định luật 1 của nhiệt động lực học
4. Nhiệt dung riêng, nhiệt nóng chảy riêng, nhiệt hoá hơi riêng
1. Mô hình động học phân tử chất khí