Tailieumoi.vn xin giới thiệu Trắc nghiệm Hóa học lớp 10 Bài 17: Nguyên tố và đơn chất halogen sách Cánh diều. Bài viết gồm 20 câu hỏi trắc nghiệm với đầy đủ các mức độ và có hướng dẫn giải chi tiết sẽ giúp học sinh ôn luyện kiến thức và rèn luyện kĩ năng làm bài trắc nghiệm Hóa học 10. Ngoài ra, bài viết còn có phần tóm tắt nội dung chính lý thuyết Bài 17: Nguyên tố và đơn chất halogen. Mời các bạn đón xem:
Trắc nghiệm Hóa học 10 Bài 17: Nguyên tố và đơn chất halogen
Phần 1: Trắc nghiệm Nguyên tố và đơn chất halogen
Câu 1. Khẳng định nào sau đây sai?
A. Xu hướng tạo liên kết khi phản ứng của nguyên tử các nguyên tố halogen là: nhận thêm một electron từ nguyên tử khác.
B. Xu hướng tạo liên kết khi phản ứng của nguyên tử các nguyên tố halogen là: góp chung electron hóa trị với nguyên tử khác
C. Hóa trị phổ biến của các halogen là II
D. Nhóm halogen có tính phi kim mạnh hơn các nhóm phi kim còn lại trong bảng tuần hoàn
Đáp án: C
Giải thích:
Hóa trị phổ biến của các halogen là II ⇒ sai. Vì hóa trị phổ biến của các halogen là I.
Câu 2. Đơn chất halogen có tính oxi hóa mạnh nhất là
A. F2
B. Cl2
C. Br2
D. I2
Đáp án: A
Giải thích:
Đơn chất halogen đều có tính oxi hóa mạnh và tính oxi hóa giảm dần từ F2 đến I2.
⇒ Đơn chất halogen có tính oxi hóa mạnh nhất là F2.
Câu 3. Đi từ F2 đến I2, khẳng định sai là
A. Nhiệt độ nóng chảy tăng dần
B. Nhiệt dộ sôi tăng dần
C. Màu sắc có xu hướng nhạt dần
D. Khối lượng phân tử tăng dần
Đáp án: C
Giải thích:
F2 màu lục nhạt, Cl2 màu vàng lục, Br2 mà nâu đỏ, I2 màu tím đen.
⇒ Đi từ F2 đến I2 màu sắc có xu hướng đậm dần.
Câu 4. Đơn chất halogen chỉ thể hiện tính oxi hóa, không thể hiện tính khử là
A. I2
B. Cl2
C. F2
D. Br2
Đáp án: C
Giải thích:
Đơn chất halogen chỉ thể hiện tính oxi hóa, không thể hiện tính khử là F2.
Các halogen còn lại thể hiện cả tính oxi hóa và tính khử trong các phản ứng hóa học. Tuy nhiên xu hướng thể hiện tính oxi hóa phổ biến hơn rất nhiều và trở nên đặc trưng hơn so với xu hướng thể hiện tính khử.
Câu 5. Phản ứng diễn ra mãnh liệt, nổ ngay cả trong bóng tối hoặc ở nhiệt độ thấp là
A. H2 (g) + F2 (g) ⟶ 2HF (g)
B. H2 (g) + I2 (g) ⇆ 2HI (g)
C. H2 (g) + Cl2 (g) ⟶ 2HCl (g)
D. H2 (g) + Br2 (g) ⟶ 2HBr (g)
Đáp án: A
Giải thích:
Phản ứng diễn ra mãnh liệt, nổ ngay cả trong bóng tối hoặc ở nhiệt độ thấp là:
H2 (g) + F2 (g) ⟶ 2HF (g)
Câu 6. Các nguyên tố nhóm VIIA gồm
A. fluorine, chlorine, bromine, iodine và hai nguyên tố phóng xạ astatine, tennessine
B. sulfur, chlorine, bromine, indium và hai nguyên tố phóng xạ astatine, tennessine
C. fluorine, chlorine, boron, iodine và hai nguyên tố phóng xạ astatine, tennessine
D. fluorine, calcium, boron, iodine và hai nguyên tố phóng xạ astatine, tennessine
Đáp án: A
Giải thích:
Các nguyên tố nhóm VIIA gồm: fluorine (F), chlorine (Cl), bromine (Br), iodine (I) và hai nguyên tố phóng xạ astatine (At), tennessine (Ts).
Câu 7. Cấu hình electron lớp ngoài cùng của nguyên tử nguyên tố nhóm halogen có dạng
A. ns1
B. ns2np1
C. ns2np6
D. ns2np5
Đáp án: D
Giải thích:
Các nguyên tố nhóm halogen thuộc nhóm VIIA trong bảng tuần hoàn, đều có 7 electron lớp ngoài cùng.
Cấu hình electron lớp ngoài cùng có dạng: ns2np5.
Câu 8. Trong tự nhiên, nguyên tố Cl có tồn tại trong
A. quặng fluorite
B. quặng cryolite
C. quặng fluorapatite
D. khoáng vật carnallite
Đáp án: D
Giải thích:
Quặng fluorite (CaF2); quặng cryolite (Na3AlF6); quặng fluorapatite (Ca5F(PO4)3); khoáng vật carnallite (KCl.MgCl2.6H2O)
⇒ nguyên tố Cl có tồn tại trong khoáng vật carnallite.
Câu 9. Đơn chất halogen ở trạng thái khí trong điều kiện thường, màu lục nhạt là
A. F2
B. Cl2
C. Br2
D. I2
Đáp án: A
Giải thích:
Đơn chất halogen ở trạng thái khí trong điều kiện thường, màu lục nhạt là F2.
Câu 10. Trong điều kiện thường, halogen tồn tại ở thể rắn là
A. F2
B. Cl2
C. Br2
D. I2
Đáp án: D
Giải thích:
Trong điều kiện thường, I2 tồn tại ở thể rắn.
Câu 11. Cho nước chlorine màu vàng rất nhạt vào dung dịch sodium bromide không màu thì hiện tượng xảy ra là
A. Không hiện tượng
B. Xuất hiện khí màu nâu đỏ
C. dung dịch chuyển màu vàng nâu
D. dung dịch chuyển màu xanh
Đáp án: C
Giải thích:
Cl2 (aq) + 2NaBr (aq) ⟶ 2NaCl (aq) + Br2 (aq)
Do có sự hình thành đơn chất bromine (màu vàng nâu) làm dung dịch chuyển màu vàng nâu.
Câu 12. Cho F2 tác dụng với nước, sản phẩm của phản ứng là
A. Không phản ứng
B. HF và HFO
C. HF và O2
D. OF2 và H2
Đáp án: C
Giải thích:
F2 (aq) + 2H2O (l) ⟶ O2 (g) + 4HF (aq)
Câu 13. Khẳng định đúng là
A. Các halogen đều thể hiện tính khử và tính oxi hóa
B. Tính oxi hóa tăng dần từ F2 đến I2
C. Mức độ tác dụng với H2, H2O tăng dần từ F2 đến I2
D. Trong dung dịch, fluorine không có phản ứng thế halogen
Đáp án: D
Giải thích:
Các halogen đều thể hiện tính khử và tính oxi hóa ⇒ sai. Vì fluorine không thể hiện tính khử.
Tính oxi hóa tăng dần từ F2 đến I2 ⇒ sai. Vì tính oxi hóa giảm dần từ F2 đến I2.
Mức độ tác dụng với H2, H2O tăng dần từ F2 đến I2 ⇒ sai. Vì mức độ tác dụng với H2, H2O giảm dần từ F2 đến I2.
Trong dung dịch, fluorine không có phản ứng thế halogen ⇒ đúng. Vì trong dung dịch, fluorine ưu tiên phản ứng với nước.
Câu 14. Cho thí nghiệm: nhỏ vào ống nghiệm chứa 2 ml dung dịch sodium iodine (có sẵn vài giọt hồ tinh bột) vài giọt nước chlorine rồi lắc nhẹ. Hiện tượng xảy ra là
A. Không xảy ra hiện tượng
B. Xuất hiện chất rắn màu đen tím
C. Dung dịch chuyển màu vàng nâu
D. Dung dịch chuyển màu xanh tím
Đáp án: D
Giải thích:
Cl2 (aq) + 2NaI (aq) ⟶ 2NaCl (aq) + I2 (aq)
I2 (aq) + hồ tinh bột ⟶ dung dịch có màu xanh tím.
Câu 15. Cho phản ứng điện phân NaCl trong công nghiệp:
NaCl (aq) + H2O (l) ⟶ A (aq) + X (g) + Y (g)
Biết Y tác dụng được với dung dịch A tạo hỗn hợp chất tẩy rửa phổ biến.
X tác dụng với Y tạo hydrogen chloride.
Công thức của A, X, Y lần lượt là
A. NaClO, HCl, HClO
B. NaOH, H2, Cl2
C. NaOH, Cl2, H2
D. NaClO3, HCl, HClO
Đáp án: B
Giải thích:
Chất tẩy rửa phổ biến là nước Javen là dung dịch chứa NaCl và NaClO
Cl2 + 2NaOH ⟶ NaCl + NaClO + H2O
⇒ Hai chất tác dụng với nhau tạo thành nước Javen là NaOH và Cl2.
Theo phương trình, A ở dạng dung dịch, Y ở dạng khí ⇒ A là NaOH, Y là Cl2
Để tạo hydrogen chloride (HCl) cần Cl2 và H2.
Cl2 + H2 2HCl
Mà Y là Cl2 ⇒ X là H2.
⇒ phản ứng điện phân NaCl trong công nghiệp:
2NaCl (aq) + 2H2O (l) ⟶ 2NaOH (aq) + H2 (g) + Cl2 (g)
Vậy A, X, Y lần lượt là NaOH, H2, Cl2.
Phần 2: Lý thuyết Nguyên tố và đơn chất halogen
I. Giới thiệu về nguyên tố nhóm VIIA
- Các nguyên tố nhóm VIIA gồm fluorine, chlorine, bromine, iodine và hai nguyên tố phóng xạ astatine, tennessine.
- Một số đặc điểm của nguyên tố halogen được thể hiện trong bảng sau:
Bảng 17.1. Một số đặc điểm của các nguyên tố halogen
|
Nguyên tố |
Số hiệu nguyên tử |
Cấu hình electron nguyên tử |
Độ âm điện |
Bán kính nguyên tử (pm) |
|
Fluorine (F) |
9 |
[He]2s22p5 |
3,98 |
42 |
|
Chlorine (Cl) |
17 |
[Ne]3s23p5 |
3,16 |
79 |
|
Bromine (Br) |
35 |
[Ar]3d104s24p5 |
2,96 |
94 |
|
Iodine (I)_ |
53 |
[Kr]4d105s25p5 |
2,66 |
115 |
|
Astatine (At) |
85 |
[Xe]4f145d106s26p5 |
2,20 |
127 |
|
Tennessine (Ts) |
117 |
[Rn]5f146d107s27p5 |
- |
- |
- Mỗi nguyên tử nguyên tố nhóm VIIA đều có 7 electron ở lớp ngoài cùng, dạng ns2np5. Vì vậy chúng là các phi kim.
- Một số dạng tồn tại của các nguyên tố halogen phổ biến trong tự nhiên được thể hiện trong bảng sau:
Bảng 17.2. Một số dạng tồn tại trong tự nhiên của các nguyên tố halogen
|
Nguyên tố |
Một số dạng tồn tại trong tự nhiên |
|
Fluorine |
- CaF2 là thành phần chính của quặng fluorite. - Na3AlF6 là thành phần chính của quặng cryolite. - Ca5F(PO4)3 là thành phần chính của quặng fluorapatite. |
|
Chlorine |
- NaCl trong mỏ muối. - Các hợp chất chloride (chứa Cl-) tan trong nước biển, nước sông, trong máu động vật. - KCl.MgCl2.6H2O là thành phần chính của khoáng vật carnallite. - NaCl.KCl là thành phần chính của khoáng vật sylvinite. - HCl trong dịch dạ dày. |
|
Bromine |
Các hợp chất bromide (chứa Br-) tan trong nước biển, nước sông. |
|
Iodine |
Các hợp chất iodide, iodate (chứa I-, ) có trong nước biển, nước sông, rong biển. |
II. Đơn chất halogen
Ở điều kiện thường, đơn chất halogen tồn tại ở dạng phân tử hai nguyên tử, được kí hiệu chung là X2.
1. Xu hướng biến đổi một số tính chất vật lí
- Một số tính chất vật lí của đơn chất halogen được thể hiện trong bảng sau:
Bảng 17.3. Một số tính chất vật lí của đơn chất halogen
|
Đơn chất (X2) |
Nhiệt độ nóng chảy (oC) |
Nhiệt độ sôi (oC) |
Thể ở điều kiện thường |
Màu sắc |
|
Fluorine (F2) |
-220 |
-188 |
Khí |
Lục nhạt |
|
Chlorine (Cl2) |
-102 |
-34 |
Khí |
Vàng lục |
|
Bromine (Br2) |
-7 |
59 |
Lỏng |
Nâu đỏ |
|
Iodine (I2) |
114 |
185 |
Rắn |
Tím đen |
- Nhận xét:
+ Nhiệt độ sôi, nhiệt độ nóng chảy của các đơn chất halogen tăng dần từ F2 đến I2.
Giải thích: Khi phân tử X2 có kích thước càng lớn và càng nhiều electron thì mức độ chuyển động hỗn loạn của các electron càng cao. Vì vậy, thường xuyên có sự phân bố không đều các electron tại một thời điểm nào đó, dễ làm xuất hiện các lưỡng cực tạm thời ở mỗi phân tử.
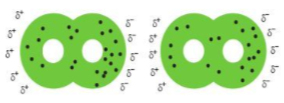
Hình 17.1. Minh họa tương tác van der Waals giữa hai phân tử iodine
→ Điều này sẽ làm tăng tương tác van der Waals giữa các phân tử halogen X2 với nhau. Dó đó, trong các đơn chất halogen, tương tác van der Waals tăng từ fluorine đến iodine. Điều này dẫn đến, nhiệt độ sôi, nhiệt độ nóng chảy của các đơn chất halogen tăng dần từ F2 đến I2.
+ Thể của các halogen ở điều kiện thường biến đổi từ khí (fluorine, chlorine) đến lỏng (bromine) và rắn (iodine), phù hợp với xu hướng tăng khối lượng phân tử và sự tương tác giữa các phân tử.
+ Màu sắc của các đơn chất halogen từ fluorine đến iodine cũng biến đổi theo xu hướng đậm dần.
2. Xu hướng tạo liên kết trong các phản ứng hóa học
Nguyên tử của các nguyên tố halogen đều có 7 electron hóa trị. Vì vậy, theo quy tắc octet, halogen thường có hai xu hướng tạo liên kết khi phản ứng với các chất khác.
- Xu hướng thứ nhất: nhận thêm 1 electron tử nguyên tử khác.
+ Xu hường này xảy ra khi khi đơn chất halogen phản ứng với nhiều kim loại khác nhau. Khi đó, mỗi nguyên tử X nhận thêm 1 electron từ nguyên tử kim loại để trở thành anion có điện tích 1-, đồng thời nguyên tử kim loại sẽ trở thành cation có điện tích n+. Cả cation và anion đều thỏa mãn quy tắc octet. Giữa chúng sẽ có tương tác tĩnh điện để tạo hợp chất có liên kết ion.
Ví dụ: Khi chlorine phản ứng với calcium, có sự nhường và nhận electron như sau:
Cl2 + 2e → 2Cl-
Ca → Ca2+ + 2e
Phương trình hóa học của phản ứng:
Ca(s) + Cl2(g) → CaCl2(s)
Lưu ý: Halogen kết hợp với nhiều kim loại tạo ra muối halide có công thức MXn như NaCl, KBr, KI, CaCl2, CuCl2, … Các muối halide của kim loại là hợp chất ion, nên hầu hết tan tốt trong nước (trừ AgCl, AgBr, AgI).
- Xu hướng thứ hai: góp chung electron hóa trị với nguyên tử nguyên tố khác
+ Khi đơn chất halogen phản ứng với một số phi kim thì mỗi nguyên tử X có thể góp chung electron hóa trị với nguyên tử phi kim đều cả hai nguyên tử đều đạt cấu hình electron thỏa mãn quy tắc octet. Giữa chúng hình thành chất có liên kết cộng hóa trị.
Ví dụ: Trong phản ứng giữa chlorine và hydrogen, nguyên tử của mỗi chất sẽ góp chung 1 electron độc thân để hình thành liên kết cộng hóa trị, Khi đó quanh nguyên tử H sẽ có 2 electron như khí hiếm helium, xung quanh chlorine sẽ có 8 electron như khí hiếm neon, với mô tả theo công thức electron như sau:
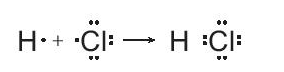
Phương trình hóa học của phản ứng:
H2(g) + Cl2(g) → 2HCl(g)
- Kết luận: để thỏa mãn quy tắc octet, nguyên tử halogen sẽ nhận thêm 1 electron của nguyên tử khác hoặc góp chung 1 electron với nguyên tử khác. Vì vậy:
+ Nhóm halogen có tính phi kim mạnh hơn các nhóm phi kim còn lại trong bảng tuần hoàn.
+ Hóa trị phổ biến của các halogen là 1.
3. Xu hướng thể hiện tính oxi hóa
- Ngoại trừ fluorine, các halogen còn lại thể hiện cả tính oxi hóa và tính khử trong các phản ứng hóa học. Tuy nhiên, xu hướng thể hiện tính oxi hóa phổ biến hơn rất nhiều và trở nên đặc trưng hơn so với xu hướng thể hiện tính khử.
- Các đơn chất halogen đều có tính oxi mạnh và tính oxi hóa giảm dần từ fluorine đến iodine
a) Phản ứng với hydrogen
- Các đơn chất halogen đều phản ứng với hydrogen tạo hydrogen halide nhưng trong các điều kiện phản ứng và điều kiện khác nhau.
Bảng 17.4. Điều kiện và mức độ phản ứng của đơn chất halogen với hydrogen, năng lượng liên kết H - X
|
Phản ứng tạo HX |
Điều kiện và mức độ phản ứng |
Năng lượng liên kết H – X (kJ mol-1) |
|
H2(g) + F2(g) → 2HF(g) |
Diễn ra mãnh liệt, nổ ngay cả trong bóng tối hoặc ở nhiệt độ thấp |
565 |
|
H2(g) + Cl2(g) → 2HCl(g) |
Nổ khi đun nóng. Hoặc nổ ngay ở nhiệt độ thường khi được chiếu tia tử ngoại |
431 |
|
H2(g)+ Br2(g) → 2HBr(g) |
Cần đun nóng để phản ứng diễn ra. Phản ứng diễn ra chậm |
364 |
|
H2(g)+ I2(g) 2HI(g) |
Cần đun nóng để phản ứng diễn ra. Phản ứng thuận nghịch, tạo hỗn hợp gồm HI sinh ra và lượng H2, I2 còn lại |
297 |
- Nhận xét:
+ Mức độ phản ứng với hydrogen giảm dần từ fluorine đến iodine, phù hợp với xu hướng giảm tính oxi hóa của dãy halogen tử fluorine đến iodine.
+ Các phản ứng đều tạo ra HX. Năng lượng liên kết H – X giảm dần làm cho độ bền nhiệt của các phân tử giảm dần từ HF đến HI. Trong đó, phân tử HI có độ bền nhiệt thấp, dễ bị phân hủy một phần để tái tạo lại iodine và hydrogen theo phản ứng:
2HI(g) H2(g)+ I2(g)
b) Phản ứng thế halogen
- Trong dung dịch, các halogen có tính oxi hóa mạnh hơn sẽ phản ứng với muối halide của halogen có tính oxi hóa yếu hơn để tạo ra các halogen có tính oxi hóa yếu hơn.
Lưu ý: Trong dung dịch thì fluorine không có phản ứng trên. Đó là do fluorine ưu tiên phản ứng với nước.
Ví dụ: Nguyên tố chlorine đã thay thế nguyên tố bromine trong muối sodium bromide.
Cl2(aq) + 2NaBr(aq) → 2NaCl(aq) + Br2(aq)
c) Phản ứng với nước, với dung dịch sodium hydroxide
- Trừ fluorine, các halogen còn lại khi phản ứng với nước hoặc dung dịch sodium hydroxide (NaOH) đều thể hiện tính oxi hóa và tính khử.
- Khi cho các halogen vào nước thì fluorine phản ứng mạnh, chlorine và bromine đều phản ứng thuận nghịch với nước, còn iodine tan rất ít và hầu như không phản ứng.
2(aq) + 2H2O(l) → O2(g) + 4(aq)
(aq) + H2O(l) (aq) + (aq)
(aq) + H2O(l) (aq) + (aq)
- Phản ứng giữa chlorine và nước là phản ứng thuận nghịch nên tạo ra dung dịch gồm nước, hydrochloric acid (HCl), hydrochlorous acid (HClO, còn được viết là HOCl). Dung dịch này còn được gọi là dung dịch nước chlorine, có tính sát khuẩn. Vì vậy, nước chlorine được sử dụng để xử lí vi khuẩn trong các nguồn nước cấp hoặc xử lí môi trường.
- Trong công nghiệp, sử dụng phản ứng giữa chlorine với sodium hydroxide lạnh (khoảng 15oC) để tạo ra nước Javel có tính oxi hóa mạnh phục vụ cho mục đích sát khuẩn, tẩy màu. Phương trình hóa học tạo nước Javel như sau:
(aq) + 2NaOH(aq) → (aq) + (aq)

Hình 17.1. Nước Javel dùng để sát khuẩn, tẩy rửa
- Ở 70oC, phản ứng giữa chlorine với sodium hydroxide xảy ra như sau:
3(aq) + 6NaOH(aq) 5(aq) + (aq) + 3H2O(l)
→ Phản ứng này thuộc loại phản ứng tự oxi hóa, tự khử. Đó là do chlorine vừa giảm số oxi hóa, vừa tăng số oxi hóa.
Xem thêm các bài trắc nghiệm Hóa học 10 Cánh diều hay, chi tiết khác:
Trắc nghiệm Hóa 10 Bài 14: Phản ứng hóa học và enthalpy
Trắc nghiệm Hóa 10 Bài 15: Ý nghĩa và cách tính biến thiên enthalpy phản ứng hóa học
Trắc nghiệm Hóa 10 Bài 16: Tốc độ phản ứng hóa học
Trắc nghiệm Hóa 10 Bài 17: Nguyên tố và đơn chất halogen
Trắc nghiệm Hóa 10 Bài 18: Hydrogen halide và hydrohalic acid