Với tóm tắt lý thuyết Hóa học lớp 10 Bài 7: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm sách Cánh diều hay, chi tiết cùng với bài tập trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 10.
Lý thuyết Hóa học lớp 10 Bài 7: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm
A. Lý thuyết Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm
I. Xu hướng biến đổi bán kính nguyên tử
1. Trong một chu kì
- Quy luật chung đối với các nguyên tố nhóm A: Trong một chu kì, theo chiều tăng dần điện tích hạt nhân, bán kính các nguyên tử có xu hướng giảm dần.
- Giải thích: Nguyên tử các nguyên tố trong cùng chu kì có cùng số lớp electron. Từ trái sang phải, điện tích hạt nhân nguyên tử tăng dần nên hạt nhân sẽ hút electron lớp ngoài cùng mạnh hơn, làm cho bán kính nguyên tử giảm.
Ví dụ: Trong chù kì 2, bán kính nguyên tử của các nguyên tố giảm dần theo thứ tự: Li, Be, B, C, N, O, F.
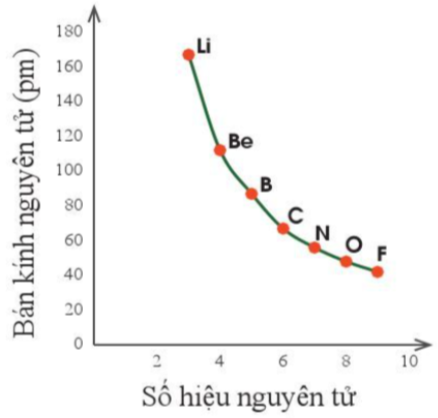
Hình 7.1. Sự thay đổi bán kính nguyên tử theo số hiệu nguyên tử của các nguyên tố chu kì 2
Lưu ý: Bán kính nguyên tử là khoảng cách từ hạt nhân đến electron ở lớp vỏ ngoài cùng.
2. Trong một nhóm A
- Quy luật chung đối với các nguyên tố nhóm A: Trong một nhóm, theo chiều tăng dần điện tích hạt nhân, bán kính các nguyên tử có xu hướng tăng dần.
- Giải thích: Trong một nhóm A, theo chiều từ trên xuống dưới, bán kính nguyên tử tăng dần, nguyên nhân chủ yếu là do số lớp electron tăng dần.
Ví dụ: Trong nhóm IIA, bán kính nguyên tử của các nguyên tố tăng dần theo thứ tự: Be, Mg, Ca, Sr, Ba.
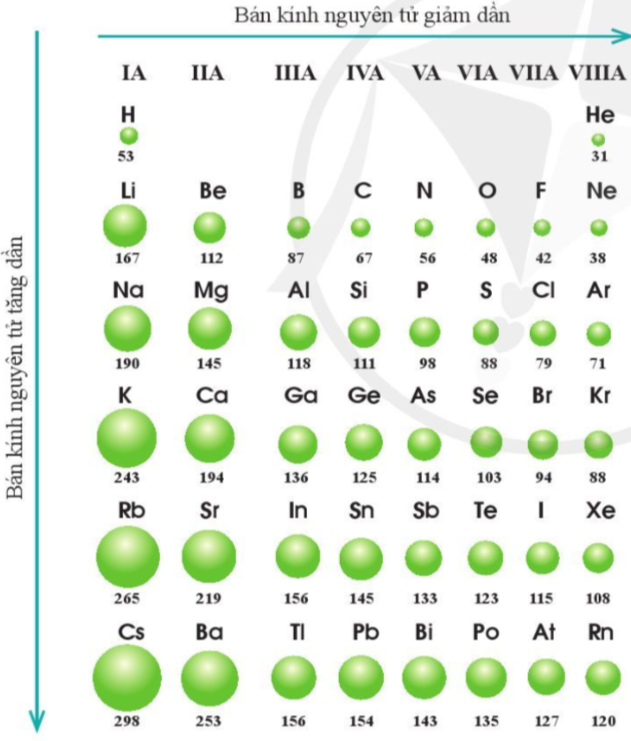
Hình 7.2. Bán kính nguyên tử (pm) của một số nguyên tố trong bảng tuần hoàn
II. Xu hướng biến đổi độ âm điện, tính kim loại và tính phi kim
1. Độ âm điện
- Độ âm điện (χ – đọc là khi) là đại lượng đặc trưng cho khả năng hút electron liên kết của nguyên tử.
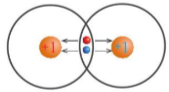
Hình 7.3. Cặp electron liên kết bị các nguyên tử hút về phía các hạt nhân của mỗi nguyên tử H
Lưu ý: Electron hóa trị đã tham gia hình thành liên kết hóa học thì gọi là electron liên kết.
- Độ âm điện được sử dụng rộng rãi là độ âm điện theo Pauling. Theo đó nguyên tử có độ âm điện lớn nhất là fluorine, χ(F) = 3,98.
- Quy luật chung đối với các nguyên tố nhóm A:
+ Trong một chu kì, theo chiều tăng điện tích hạt nhân, độ âm điện của các nguyên tử nguyên tố có xu hướng tăng dần.
+ Trong một nhóm, theo chiều tăng điện tích hạt nhân, độ âm điện của các nguyên tử nguyên tố có xu hướng giảm dần.

Hình 7.4. Giá trị độ âm điện của một số nguyên tố nhóm A và quy luật biến đổi độ âm điện
- Độ âm điện phụ thuộc đồng thời vào hai yếu tố: điện tích hạt nhân và bán kính nguyên tử.
- Giải thích:
+ Trong một chu kì, từ trái sang phải theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử giảm dần nên khả năng hút cặp electron liên kết càng tăng, dẫn tới độ âm điện càng tăng.
+ Trong một nhóm, từ trên xuống dưới theo chiều tăng dần của điện tích hạt nhân, bán kính nguyên tử tăng lên nên lực hút của hạt nhân tới cặp electron liên kết giảm, dẫn tới độ âm điện giảm.
Chú ý: Theo biểu thức , lực hút F giảm theo r2 và tăng theo Z, nghĩa là ảnh hưởng của r lớn hơn của Z tới lực hút của hạt nhân với electron.
2. Tính kim loại và tính phi kim
- Tính kim loại đặc trưng bởi khả năng nhường electron của nguyên tử.
- Tính phi kim đặc trưng bởi khả năng nhận electron của nguyên tử.
- Quy luật chung đối với các nguyên tố nhóm A:
+ Trong một chu kì, theo chiều tăng điện tích hạt nhân, tính kim loại của các nguyên tố có xu hướng giảm dần, tính phi kim của các nguyên tố có xu hướng tăng dần.
+ Trong một nhóm, theo chiều tăng điện tích hạt nhân, tính kim loại của các nguyên tố có xu hướng tăng dần, tính phi kim của các nguyên tố có xu hướng giảm dần.
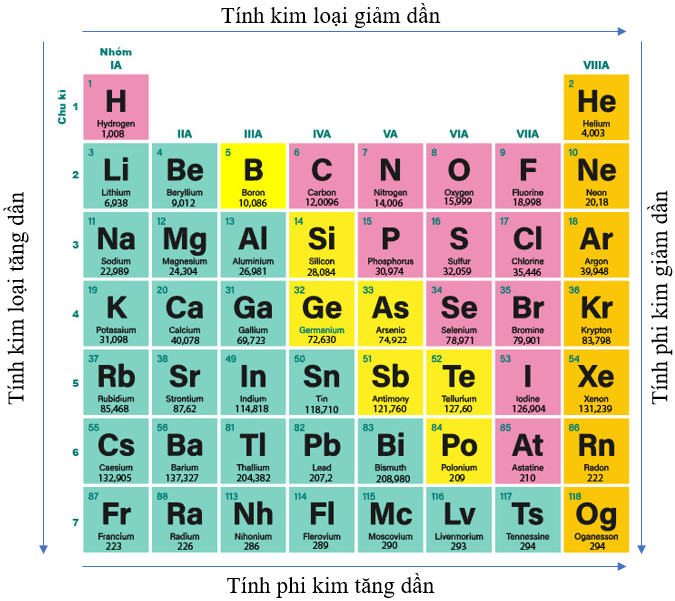
Hình 7.5. Quy luật biến đổi tính kim loại, tính phi kim
- Giải thích:
+ Trong một chu kì, từ trái sang phải, điện tích hạt nhân tăng dần, bán kính nguyên tử giảm dần nên lực hút của hạt nhân tới electron hóa trị tăng, làm giảm khả năng nhường electron, do đó tính kim loại của nguyên tố giảm.
+ Trong một nhóm A, mặc dù điện tích hạt nhân tăng dần nhưng do bán kính nguyên tử của các nguyên tố tăng nhanh, nên lực hút của hạt nhân tới electron hóa trị giảm dần, làm tăng khả năng nhường electron, do đó tính kim loại của nguyên tố tăng.
Lưu ý: Tính kim loại và tính phi kim luôn biến đổi ngược chiều nhau. Độ âm điện và tính phi kim của các nguyên tử của nguyên tố hóa học biến đổi cùng chiều trong một chu kì và trong một nhóm.
III. Xu hướng biến đổi thành phần và tính acid, tính base của các oxide và các hydroxide theo chu kì
1. Thành phần và tính acid, tính base của các oxide cao nhất trong một chu kì
- Oxide cao nhất của một nguyên tố là oxide mà trong đó, hóa trị của nguyên tố đó là cao nhất. Các nguyên tố thuộc các nhóm IA đến VIIA (trừ fluorine) có hóa trị cao nhất đúng bằng số thứ tự nhóm.
- Công thức oxide cao nhất và hóa trị của các nguyên tố nhóm A, chu kì 3 được thể hiện trong bảng 3.1.
Bảng 3.1. Công thức oxide cao nhất của các nguyên tố nhóm A, chu kì 3
|
Oxide cao nhất |
Na2O |
MgO |
Al2O3 |
SiO2 |
P2O5 |
SO3 |
Cl2O7 |
|
Hóa trị nguyên tố |
I |
II |
III |
IV |
V |
VI |
VII |
- Xu hướng biến đổi thành phần của các oxide cao nhất: Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tỉ số giữa số nguyên tử oxygen với số nguyên tử nguyên tố còn lại trong các oxide cao nhất có xu hướng tăng dần.
Ví dụ: Trong chu kì 3, theo chiều tăng dần của điện tích hạt nhân, tỉ số giữa số nguyên tử oxygen với số nguyên tử nguyên tố còn lại trong các oxide cao nhất tăng dần theo thứ tự , , , , , , .
- Xu hướng biến đổi tính acid, tính base của oxide cao nhất: Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính acid của oxide cao nhất có xu hướng tăng dần, tính base của chúng có xu hướng giảm dần.
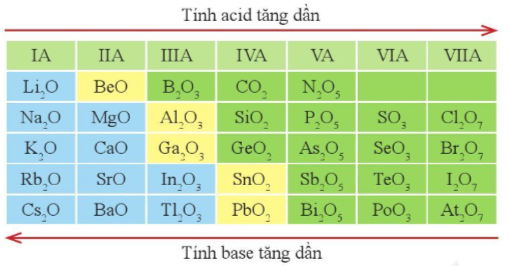
Hình 7.6. Xu hướng biến đổi tính acid, tính base của một số oxide cao nhất
Ví dụ: Trong chu kì 3, Cl2O7 có tính acid mạnh nhất, Na2O có tính base mạnh nhất và Al2O3 vừa có tính acid, vừa có tính base.
Lưu ý:
- Không tồn tại hợp chất F2O7, oxide thường gặp của F có công thức là F2O.
- Quy luật về sự biến đổi chung của tính acid và tính base của oxide cao nhất ngược chiều nhau trong mỗi chu kì và nhóm.
- Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân, nói chung tính base của oxide cao nhất tăng dần .
- Al2O3 có tính lưỡng tính: tác dụng được với cả dung dịch acid và dung dịch base.
2. Thành phần và tính acid, tính base của các hydroxide cao nhất trong một chu kì
- Hydroxide của nguyên tố kim loại M hóa trị n có dạng M(OH)n. Đối với nguyên tố phi kim hydroxide của nó ở dạng acid.
Bảng 3.2. Công thức hydroxide của các nguyên tố nhóm A, chu kì 3 (các nguyên tố ở hóa trị cao nhất)
|
Công thức hydroxide |
NaOH |
Mg(OH)2 |
Al(OH)3 |
H2SiO3 |
H3PO4 |
H2SO4 |
HClO4 |
|
Hóa trị nguyên tố |
I |
II |
III |
IV |
V |
VI |
VII |
- Xu hướng biến đổi tính acid, tính base của hydroxide: Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính acid của các hydroxide có xu hướng tăng dần, tính base của chúng có xu hướng giảm dần.
Ví dụ: Trong chu kì 3, NaOH là một base mạnh; Al(OH)3 vừa có tính acid, vừa có tính base; H2SiO3 là acid rất yếu; H3PO4 là acid trung bình; H2SO4 là acid mạnh; HClO4 là acid rất mạnh.
Lưu ý: Acid chứa oxygen có thể được coi là một dạng của hydroxide (không bền) bị mất nước.
Ví dụ: Si(OH)4 H2SiO3 + H2O
B. Trắc nghiệm Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm
Câu 1. Theo độ âm điện của Pauling, nguyên tử có độ âm điện lớn nhất trong bảng tuần hoàn là
A. F
B. H
C. He
D. O
Đáp án: A
Giải thích:
Theo độ âm điện của Pauling, nguyên tử có độ âm điện lớn nhất trong bảng tuần hoàn là
F.
Câu 2. Cho χ(H) = 2,2; χ(C) = 2,55; χ(N) = 3,04; χ(O) = 3,44; χ(F) = 3,98. Cặp electron liên kết bị lệch nhiều nhất trong phân tử nào dưới đây?
A. NH3
B. H2O
C. HF
D. CH4
Đáp án: C
Giải thích:
Trong phân tử NH3 nguyên tử N hút electron liên kết mạnh hơn H gấp 3,04 : 2,2 ≈ 1,38 lần.
Trong phân tử H2O nguyên tử O hút electron liên kết mạnh hơn H gấp 3,44 : 2,2 ≈ 1,56 lần.
Trong phân tử HF nguyên tử F hút electron liên kết mạnh hơn H gấp 3,98 : 2,2 ≈ 1,81 lần.
Trong phân tử CH4 nguyên tử C hút electron liên kết mạnh hơn H gấp 2,55 : 2,2 ≈ 1,16 lần.
Vậy cặp electron liên kết bị lệch nhiều nhất trong phân tử HF.
Câu 3. Khẳng định nào dưới đây sai khi nói về các nguyên tố nhóm A?
A. Theo chiều tăng dần của điện tích hạt nhân, tính kim loại của nguyên tử nguyên tố hóa học có xu hướng giảm trong cùng một nhóm và tăng trong cùng một chu kì.
B. Theo chiều tăng dần của điện tích hạt nhân, tính phi kim của nguyên tử nguyên tố hóa học có xu hướng giảm trong cùng một nhóm và tăng trong cùng một chu kì.
C. Theo chiều tăng dần của điện tích hạt nhân, tính acid của oxide và hydroxide có xu hướng tăng dần trong một chu kì.
D. Theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide có xu hướng giảm dần trong một chu kì.
Đáp án: A
Giải thích:
- Theo chiều tăng dần của điện tích hạt nhân, tính kim loại của nguyên tử nguyên tố hóa học có xu hướng tăng trong cùng một nhóm và giảm trong cùng một chu kì. ⇒ Khẳng định A sai.
- Theo chiều tăng dần của điện tích hạt nhân, tính phi kim của nguyên tử nguyên tố hóa học có xu hướng giảm trong cùng một nhóm và tăng trong cùng một chu kì.
- Theo chiều tăng dần của điện tích hạt nhân, tính acid của oxide và hydroxide có xu hướng tăng dần trong một chu kì.
- Theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide có xu hướng giảm dần trong một chu kì.
Câu 4. So sánh bán kính nguyên tử của X (Z = 11), Y (Z = 12) và T (Z = 14) đúng là
A. X < Y < T
B. X < T < Y
C. Y < T < X
D. T < Y < X
Đáp án: D
Giải thích:
Cấu hình electron của X (Z = 11): [Ar]3s1
Cấu hình electron của Y (Z = 12): [Ar]3s2
Cấu hình electron của T (Z = 14): [Ar]3s23p2
Vậy X, Y, T cùng thuộc chu kì 3. Mà điện tích hạt nhân của X < Y < T
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân bán kính nguyên có xu hướng giảm.
Vậy bán kính nguyên tử của T < Y < X.
Câu 5. Cho X (Z = 9), Y (Z = 17) và T (Z = 16). Sắp xếp các nguyên tố theo thứ tự độ âm điện giảm dần.
A. X, Y, T
B. T, Y, X
C. X, T, Y
D. Y, T, X
Đáp án: A
Giải thích:
Cấu hình electron của X (Z = 9): 1s22s22p5 ⇒ chu kì 2, nhóm VIIA
Cấu hình electron của Y (Z = 17): [Ne]3s23p5 ⇒ chu kì 3, nhóm VIIA
Cấu hình electron của T (Z = 16): [Ne]3s23p4 ⇒ chu kì 3, nhóm VIA
Y và T cùng thuộc chu kì 3 mà điện tích hạt nhân của T < Y.
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân độ âm điện có xu hướng tăng.
Do đó, độ âm điện của Y > T
X và Y cùng thuộc nhóm VIIA mà điện tích hạt nhân của X < Y.
Trong cùng một nhóm, theo chiều tăng dần của điện tích hạt nhân độ âm điện có xu hướng giảm.
Do đó, độ âm điện của X > Y
Vậy độ âm điện của X > Y > T.
Câu 6. Từ thích hợp điền vào chỗ trống là
“Trong một chu kì, theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử có xu hướng …….. , độ âm điện của các nguyên tố có xu hướng ………”
A. tăng dần, tăng dần
B. tăng dần, giảm dần
C. giảm dần, giảm dần
D. giảm dần, tăng dần
Đáp án: D
Giải thích: Quy luật chung đối với các nguyên tố nhóm A: Trong một chu kì, theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử có xu hướng giảm dần, độ âm điện của các nguyên tố có xu hướng tăng dần.
Câu 7. Nguyên tử có kích thước nhỏ nhất trong bảng tuần hoàn là
A. H
B. He
C. Cs
D. F
Đáp án: B
Giải thích:
Nguyên tử He thuộc chu kì 1, nguyên tử chỉ có 1 lớp electron nên có bán kính nhỏ hơn bán kính của nguyên tử nguyên tố thuộc các chu kì còn lại.
Trong chu kì 1 chỉ có hai nguyên tố H và He. Cùng có một lớp electron nhưng điện tích hạt nhân của He lớn hơn H nên hạt nhân sẽ hút electron lớp ngoài cùng mạnh hơn, làm cho bán kính nguyên tử của He nhỏ hơn H.
Vậy He là nguyên tử có kích thước nhỏ nhất trong bảng tuần hoàn.
Câu 8. Đại lượng đặc trưng cho khả năng hút electron liên kết của một nguyên tử trong phân tử là
A. bán kính nguyên tử;
B. độ âm điện;
C. năng lượng ion hóa;
D. điện tích hạt nhân.
Đáp án: B
Giải thích: Đại lượng đặc trưng cho khả năng hút electron liên kết của một nguyên tử trong phân tử là độ âm điện (χ).
Câu 9. Cho phân tử HCl, biết cặp electron liên kết bị lệch về phía nguyên tử Cl. Khẳng định nào sau đây đúng khi nói về độ âm điện của H và Cl?
A. χ(H) < χ(Cl)
B. χ(H) > χ(Cl)
C. χ(H) = χ(Cl)
D. χ(H) ≤ χ(Cl)
Đáp án: A
Giải thích: Trong phân tử HCl, cặp electron liên kết bị lệch về phía nguyên tử Cl nghĩa là nguyên tử Cl hút electron liên kết mạnh hơn nguyên tử H. Do đó χ(H) < χ(Cl).
Câu 10. Cặp electron liên kết trong nguyên tử nào dưới đây không bị lệch về phía nguyên tử nào?
A. NH3
B. H2O
C. H2
D. CO2
Đáp án: C
Giải thích:
Phân tử H2 được tạo nên từ hai nguyên tử H, đều có cùng độ âm điện.
Do đó lực hút electron liên kết của 2 nguyên tử H bằng nhau. Vậy trong phân tử H2 cặp electron liên kết không bị lệch về phía nguyên tử nào.
Câu 11. Sắp xếp các nguyên tố N, O, P theo chiều tính phi kim tăng dần.
A. N, O, P
B. P, N, O
C. P, O, N
D. N, P, O
Đáp án: B
Giải thích:
Theo chiều tăng dần của điện tích hạt nhân, tính phi kim của nguyên tử nguyên tố hóa học có xu hướng giảm trong cùng một nhóm và tăng trong cùng một chu kì.
N (Z = 7): chu kì 2, nhóm VA
O (Z = 8): chu kì 2, nhóm VIA
P (Z = 15): chu kì 3, nhóm VA
N và O cùng ở chu kì 2, theo chiều tăng dần của điện tích hạt nhân, tính phi kim của N < O.
N và P cùng ở nhóm VA, theo chiều tăng dần của điện tích hạt nhân, tính phi kim của N > P.
Vậy tính phi kim của P < N < O.
Câu 12. Công thức oxide cao nhất của nguyên tố X (Z = 7) là
A. X2O7
B. XO3
C. X2O5
D. XO2
Đáp án: C
Giải thích:
X (Z = 7): 1s22s22p3 ⇒ nhóm VA
Hóa trị cao nhất = số thứ tự nhóm ⇒ hóa trị cao nhất của X là V
Oxide cao nhất của X là: X2O5
Câu 13. Sắp xếp tính base của NaOH, Mg(OH)2, Al(OH)3 theo chiều giảm dần là
A. NaOH, Mg(OH)2, Al(OH)3
B. Al(OH)3, Mg(OH)2, NaOH
C. Mg(OH)2, Al(OH)3, NaOH
D. Mg(OH)2, NaOH, Al(OH)3
Đáp án: A
Giải thích:
Na, Mg, Al cùng thuộc chu kì 3 theo chiều tăng dần của điện tích hạt nhân, tính base của hydroxide có xu hướng giảm dần theo thứ tự NaOH, Mg(OH)2, Al(OH)3.
Do đó tính base
Câu 14. Cho các đặc trưng sau:
(1) Dễ nhường electron.
(2) Dễ nhận electron.
(3) Oxide cao nhất có tính base.
(4) Oxide cao nhất có tính acid.
Những đặc trưng thuộc về phi kim là
A. (1), (4)
B. (2), (4)
C. (2), (3)
D. (1), (3)
Đáp án: B
Giải thích:
(1) Dễ nhường electron. ⇒ Đặc trưng của kim loại nhóm A.
(2) Dễ nhận electron. ⇒ Đặc trưng của phi kim.
(3) Oxide cao nhất có tính base. ⇒ Đặc trưng của kim loại nhóm A.
(4) Oxide cao nhất có tính acid. ⇒ Đặc trưng của phi kim.
Câu 15. Cho các phản ứng sau:
(1) Al(OH)3 + NaOH ⟶ Na[Al(OH)4]
(2) Al(OH)3 + 3HCl ⟶ AlCl3 + 3H2O
Khẳng định đúng khi nói về tính chất của Al(OH)3 trong các phản ứng trên là
A. Cả hai phản ứng (1) và (2) đều thể hiện tính base của Al(OH)3
B. Cả hai phản ứng (1) và (2) đều thể hiện tính acid của Al(OH)3
C. Phản ứng (1) thể hiện tính base; phản ứng (2) thể hiện tính acid của Al(OH)3
D. Phản ứng (2) thể hiện tính base; phản ứng (1) thể hiện tính acid của Al(OH)3
Đáp án: D
Giải thích:
Al(OH)3 thể hiện tính acid khi tác dụng với base
(1) Al(OH)3 + NaOH ⟶ Na[Al(OH)4]
(2) Al(OH)3 + 3HCl ⟶ AlCl3 + 3H2O
Al(OH)3 thể hiện tính base khi tác dụng với acid.
Bài giảng Hóa học 10 Bài 7: Xu hướng biến đổi một số tính chất của đơn chất, biến đổi thành phần và tính chất của hợp chất trong một chu kì và trong một nhóm - Cánh diều
Xem thêm các bài tóm tắt lý thuyết Hóa học 10 Cánh diều hay, chi tiết khác:
Bài 6: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học
Bài 8: Định luật tuần hoàn và ý nghĩa của bảng tuần hoàn các nguyên tố hóa học