A. Na2HPO4.
B. NaHSO4.
C. KHCO3.
D. Na2SO4.
 Giải bởi Vietjack
Giải bởi Vietjack
Chọn đáp án D
Phương pháp giải:
Muối axit là muối chứa gốc axit còn có khả năng phân li ra H+.
Chú ý: Muối HPO3– và HPO2– không phải là muối axit.
→ Muối trung hòa là các muối còn lại: không có H+ hoặc là các muối có gốc HPO3– và HPO2–
Giải chi tiết:
A. Na2HPO4: Đây là muối axit do gốc PO4 còn chứa nguyên tử H có khả năng phân li ra ion H+.
B. NaHSO4: Tương tự, đây cũng là muối axit do gốc SO4 còn chứa nguyên tử H có khả năng phân li ra ion H+.
C. KHCO3: Đây cũng là muối axit do gốc CO3 còn chứa nguyên tử H có khả năng phân li ra ion H+.
D. Na2SO4: Gốc SO4 trong muối này không còn nguyên tử H nào nữa, do đó đây là muối trung hòa.
Ví dụ về phương trình điện li của Na2SO4:
Na2SO4 --> 2Na+ + SO42-
Hòa tan hoàn toàn 2,16 gam hỗn hợp X gồm Fe và Fe2O3 trong dung dịch HNO3 dư, thu được 0,224 lít khí NO (là sản phẩm khử duy nhất, ở đktc).
a. Viết phương trình hóa học của các phản ứng xảy ra.
b. Tính phần trăm khối lượng các chất trong X.
c. Tính số mol HNO3 phản ứng.
Thực hiện các thí nghiệm sau:
(a) Đốt cháy NH3 trong không khí;
(b) Cho NO tác dụng với O2 ở nhiệt độ thường;
(c) Đốt cháy P trong O2 dư;
(d) Cho kim loại Cu tác dụng với dung dịch HNO3 đặc, nóng.
Số thí nghiệm xảy ra phản ứng oxi hóa – khử là
Cho m gam hỗn hợp X gồm Na và Ca vào một lượng nước dư, thu được dung dịch Y. Sục từ từ cho đến dư khí CO2 vào Y, số mol kết tủa CaCO3 phụ thuộc vào số mol CO2 theo đồ thị sau:
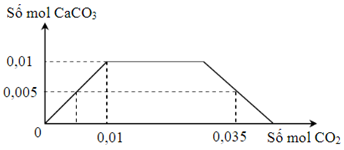
Khối lượng của Na trong m gam X là