Dãy chất nào sau đây, trong nước đều là chất điện li mạnh?
A. H2SO4, Cu(NO3)2, CaCl2, H2S
B. HCl, H3PO4, Fe(NO3)3, NaOH
C. HNO3, CH3COOH, BaCl2, KOH
D. H2SO4, MgCl2, Al2(SO4)3, Ba(OH)2
 Giải bởi Vietjack
Giải bởi Vietjack
Chọn đáp án D
Dãy chất trong nước đều là chất điện li mạnh là H2SO4, MgCl2, Al2(SO4)3, Ba(OH)2
A. Loại vì H2S là chất điện li yếu
B. Loại vì H3PO4 là chất điện li yếu
C. Loại vì CH3COOH là chất điện li yếu.
Lưu ý:
Độ điện li (α)
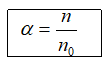
n: số phân tử hoà tan; n0: số phân tử ban đầu.
- Chất điện li yếu là chất khi tan trong nước chỉ có một số phân tử hoà tan phân li thành ion, phần còn lại vẫn tồn tại dưới dạng phân tử trong dung dịch (0 < α < 1, phương trình biểu diễn ⇋), gồm:
+ Các axit trung bình và yếu như: H2S, H2CO3, H3PO4, CH3COOH...
+ Các bazơ không tan như: Mg(OH)2, Fe(OH)2, Fe(OH)3...
- Chất điện li mạnh là chất khi tan trong nước, các phân tử hoà tan đều phân li ra ion (α = 1, phương trình biểu diễn →), gồm:
+ Các axit mạnh: HCl, HNO3, H2SO4, HBr, HI, HClO4, HClO3,...
+ Các dung dịch bazơ: NaOH, KOH, Ca(OH)2, Ba(OH)2,...
+ Hầu hết các muối.
- Cân bằng điện li:
Ví dụ: HF → H+ + F-
* Ảnh hưởng của sự pha trộn đến độ điện li α: Khi pha loãng → α tăng
Natri florua( NaF) trong trường hợp nào dưới đây không dẫn được điện?
Tính dẫn điện của các dung dịch axit, bazo, muối là do trong dung dịch của chúng có
Các dung dịch sau đây có cùng nồng độ 0,10 mol/l, dung dịch nào dẫn điện kém nhất?
Nước đóng vai trò gì trong quá trình điện li các chất tan trong nước?